
【题目】已知A的分子式为C4H4O3 ,根据图示填空。

(1)化合物A中含有的官能团是________(填名称)。
(2)1 mol A与2 mol H2反应生成1 mol E,写出该反应的方程式_______________________ ,该反应的反应类型为_________,
(3)与A具有相同官能团的A的同分异构体的结构简式是_______。
(4)B在酸性条件下与Br2反应得到D,D的结构简式是______________。
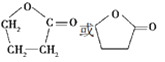
(5)F的结构简式是________;
【答案】 碳碳双键、醛基、羧基 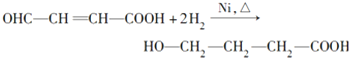 加成反应或还原反应
加成反应或还原反应 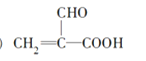
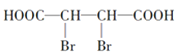
【解析】(1)A的分子式为C4H4O3,能与NaHCO3反应,则分子中必有羧基,能与银氨溶液反应,则分子中必有醛基,能与Br2反应,则分子中必有碳碳双键。故化合物A中含有的官能团是:碳碳双键、醛基、羧基。
(2)因为D的碳链没有支链,所以A的结构简式为:![]() ,又因为1 molA与2 molH2反应生成1 molE,所以该反应的方程式为:
,又因为1 molA与2 molH2反应生成1 molE,所以该反应的方程式为:![]()
![]() ;反应类型为:加成反应(或还原反应)。A与银氨溶液反应生成羧酸铵B,
;反应类型为:加成反应(或还原反应)。A与银氨溶液反应生成羧酸铵B,
(3)与A具有相同官能团的A的同分异构体,只能是醛基与羧基连在同一个碳上,结构简式是:![]() 。
。
(4)B为羧酸铵,在酸性条件下与Br2发生加成反应得到D,所以D的结构简式是:![]() 。
。
(5)E为![]() ,在一定条件下生成环状化合物F,F的分子式为:C4H6O2,所以F是一种环状的酯,结构简式为:
,在一定条件下生成环状化合物F,F的分子式为:C4H6O2,所以F是一种环状的酯,结构简式为: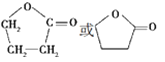 。
。


科目:高中化学 来源: 题型:
【题目】用下列实验装置进行相应的实验,不能达到实验目的是( )
A | B | C | D | |
装置 |
|
|
|
|
实验 | 结合秒表定量比较锌与不同浓度的稀硫酸反应的快慢 | 证明温度对化学平衡的影响 | 验证铁钉发生吸氧腐蚀 | 可证明非金属性 C>Si |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述正确的是 ( )
A. 原子晶体中共价键越强熔点越高
B. 晶体中分子间作用力越大分子越稳定
C. 冰融化时水分子中共价键发生断裂
D. 氧化钠熔化时离子键、共价键均被破坏
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】CO2和CH4是两种温室气体,研究它们具有重要的意义。
(1)已知CH4、H2和CO的燃烧热(△H)分别为-890.3 kJ· mol-1、-285.8 kJ· mol-1和-283.0 kJ·mol-1。则![]()
![]() △H=_________kJ·mol-1
△H=_________kJ·mol-1
(2)以CO2和NH3为原料合成尿素是利用CO2的成功范例。在尿素合成塔中的主要反应可表示为: ![]()
![]() △H=-86.98 kJ·mol-1
△H=-86.98 kJ·mol-1
反应中影响CO2平衡转化率的因素很多,右图为某特定条件下,不同水碳比[n(H2O/n(CO2)]和温度对CO2平衡转化率的影响曲线。

①为提高CO2的平衡转化率,生产中除控制温度外还可以采取的措施有___________________、____________________。
②当温度高于190℃后,CO2平衡转化率出现如图所示的变化趋势,其原因是_______________。
(3)向1.0 L密闭容器中通入0.2 mol NH3(g)和0.1 mol CO2(g),在一定温度下发生反应则![]()
![]() ,反应时间与气体总压强(p)的数据如下表:
,反应时间与气体总压强(p)的数据如下表:
![]() 用起始压强和总压强计算平衡时NH3的转化率为_________,0~80 min内CO2的平均反应速率是__________。
用起始压强和总压强计算平衡时NH3的转化率为_________,0~80 min内CO2的平均反应速率是__________。
(4)氨基甲酸铵(NH2COONH4)极易水解成碳酸铵,在酸性条件水解更彻底。将氨基甲酸铵粉末逐渐加入到1 L 0.1 mol·L-1的盐酸中直到pH=7(室温下,忽略溶液体积变化),共用去0.052 mol氨基甲酸铵,溶液中几乎不含碳元素。此时溶液中c(NH4+)=__________,NH4+水解平衡常数为__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】钒及其化合物广泛用于催化剂和新型电池等。工业上以富钒炉渣(主要成分V2O5、Fe2O3和SiO2等)为原料提取五氧化二钒的工艺流程如下图所示:

(1)该工艺流程中可以循环利用的物质有______________。
(2)焙烧炉中发生的主要反应化学方程式为___________________,焙烧炉中可用Na2CO3代替NaCl与富钒炉渣焙烧制得偏钒酸钠。用Na2CO3代替NaCl的优点是____________________。

(3)234g固体偏钒酸铵在煅烧过程中,固体的质量减少值(△W)随温度变化的曲线如图所示。其分解过程中_________。(NH4VO3相对分子质量为117)
a.先分解失去NH3,再分解失去H2O
b.先分解失去H2O,再分解失去NH3
c.同时失去H2O和NH3
d.同时失去H2、N2和H2O
(4)为测定该产品的纯度,兴趣小组同学准确称取产品V2O5 2.0 g,加入足量稀硫酸使其完全生成(VO2)2SO4并配成250 mL溶液。取25.00 mL溶液用0.1000 mol· L-1的H2C2O4。标准溶液滴定,滴定到终点时消耗标准液10.00 mL。反应的离子方程式为:2VO2++ H2C2O4+2H+==2VO2++2CO2↑+2H2O。该产品的纯度为__________。
(5)V2O5具有强氧化性,能与盐酸反应生成氯气和VO+。该反应的离子反应方程式为____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定温度和压强下,2体积AB2气体和1体积B2气体恰好化合成2体积的C气体,则C的化学式可能为
A.AB2 B. AB3 C.A3B D.A2B3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】由短周期前10号元素组成的物质T和X,存在如图所示的转化关系。X不稳定,易分解。下列有关说法正确的是

A. T分子中只含有极性键,X分子中既含有极性键又含有非极性键
B. 等物质的量的T、X分子中含有二键的数目均为NA
C. T、X分子中的![]() 原子分别采用sp2杂化和sP3杂化
原子分别采用sp2杂化和sP3杂化
D. 为使该转化成功进行,Y可以是酸性KMnO4溶液
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com