
【题目】把3molA和2.5molB混合与2L密闭容器中,发生反应:3A(g)+B(g)![]() xC(g)+2D(g),5min后达平衡,容器内压强变小,测得D的平均反应速率为0.1mol/(L·min)。求:
xC(g)+2D(g),5min后达平衡,容器内压强变小,测得D的平均反应速率为0.1mol/(L·min)。求:
(1)x= 。
(2)平衡时C的浓度为多少?(要求写出计算过程)
【答案】(1)x= 1;(2) 0.25mol·L-1。
【解析】
试题分析:(1)把3molA和2.5molB混合与2L密闭容器中,发生反应:3A(g)+B(g)![]() xC(g)+2D(g),5min后达平衡,容器内压强变小,说明该反应的正反应是气体体积减小的反应,故3+1>x+2,所以x<2,即x=1;(2) D的平均反应速率为0.1mol/(L.min),则△n(D)=0.1mol/(L·min) ×2L×5min=1mol,根据物质反应时的物质的量的比等于方程式的化学计量数的比可知反应消耗C的物质的量是△n(C)=1/2△n(D)= 0.5mol,则c(C)= 0.5mol/2L=0.25mol·L-1。
xC(g)+2D(g),5min后达平衡,容器内压强变小,说明该反应的正反应是气体体积减小的反应,故3+1>x+2,所以x<2,即x=1;(2) D的平均反应速率为0.1mol/(L.min),则△n(D)=0.1mol/(L·min) ×2L×5min=1mol,根据物质反应时的物质的量的比等于方程式的化学计量数的比可知反应消耗C的物质的量是△n(C)=1/2△n(D)= 0.5mol,则c(C)= 0.5mol/2L=0.25mol·L-1。


 寒假学与练系列答案
寒假学与练系列答案科目:高中化学 来源: 题型:
【题目】请按要求回答下列问题。
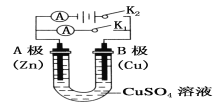
(1)根据上图回答①②:
①打开K2,闭合K1。
A电极可观察到的现象是________________________________;
B极的电极反应式为___________________________________。
②打开K1,闭合K2。
A电极可观察到的现象是__________________________________;
B极的电极反应式为_____________________________________。
(2)根据下图回答③④:
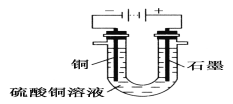
③将较纯净的CuSO4溶液放入上图所示的装置中进行电解,石墨电极上的电极反应式为___________________________________________________________,
电解反应的离子方程式为__________________________________________;
④实验完成后,铜电极增重a g,石墨电极产生标准状况下的气体体积________L。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列3种有机化合物A: CH2=CH-CH3B:![]() C:CH3CH2OH
C:CH3CH2OH
(1)写出化合物A、C中的官能团的名称 、 。
(2)A在催化剂加热条件下生成聚合物的反应方程式为 。
(3) B可以被酸性高锰酸钾氧化成苯甲酸,写出苯甲酸与C物质在浓硫酸中共热发生酯化反应的化学方程式: 。
(4) 草酸(乙二酸)与乙二醇按1:1生成聚乙二酸乙二酯的反应方程式为__________。
(5) 苯酚钠中通入二氧化碳的反应方程式为__________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】【化学-选修2:化学与技术】
氯化亚铜(CuCl)广泛应用于化工、印染、电镀等行业。CuCl难溶于醇和水,可溶于氯离子浓度较大的体系,在潮湿空气中易水解氧化。以海绵铜(主要成分是Cu和少量CuO)为原料采用硝酸铵氧化分解技术生产CuC1的工艺过程如下:
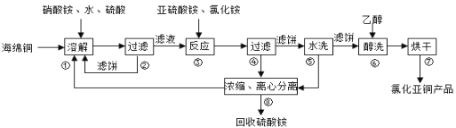
回答下列问题:
(1)步骤①中得到的氧化产物是___________,溶解温度应控制在60-70℃,原因是___________;
(2)写出步骤③中主要反应的离子方程式_________________;
(3)步骤⑤包括用pH=2的酸洗、水洗两步操作,酸洗采用的酸是__________(写名称)。
(4)上述工艺中,步骤⑥不能省略,理由是_________________;
(5)步骤②、④、⑤、⑧都要进行固液分离.工业上常用的固液分离设备有_______(填字母)
A、分馏塔 B、离心机 C、反应釜 D、框式压滤机
(6)准确称取所制备的氯化亚铜样品mg,将其置于过量的FeCl3溶液中,待样品完全溶解后,加入适量稀硫酸,用amol/L-1的K2Cr2O7溶液滴定到终点,消耗K2Cr2O7溶液bmL,反应中Cr2O72-被还原为Cr3+,样品中CuCl的质量分数为___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为了研究碳酸钙与稀盐酸反应的反应速率,一位同学通过实验测定反应中生成的CO2气体体积随反应时间变化的情况,绘制曲线.请分析讨论以下问题。
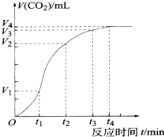
(1)碳酸钙与稀盐酸的反应是放热反应,这是由于反应物的总能量 (填“大于”或“小于”)生成物的总能量。
(2)在0~t1、t1~t2、t2~t3、t3~t4各相同的时间段里,收集到气体最多的是 时间段。反应速率最大的是 时间段,反应速率最小的是 时间段。
(3)t1~t2时间段里影响反应速率的主要外界因素 、t2~t3时间段里影响反应速率的主要外界因素是 (填“温度”或“浓度”或“压强”或“催化剂”)(提醒:多填不得分)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D、E、F、G七种短周期元素,其原子序数依次增大。A的原子中没有成对电子;B的基态原子中电子占据三种能量不同的原子轨道,且每种轨道中的电子总数相同;D原子最外层电子数是内层电子数的3倍;D与G处在同一族;F是地壳中含量最高的金属元素。请回答下列问题:
(1)元素F在周期表中的位置 。
(2)B、C、D三种元素的第一电离能由大到小的顺序是 (用元素符号表示)。
(3)配合物Ni(BD)4常温下为液态,易溶于CCl4、苯等有机溶剂,因此固态Ni(BD)4属于 (填晶体类型)。
(4)CA3分子的电子式为 。
(5)ED是优良的耐高温材料,其晶体结构与NaCl晶体相似。ED的熔点比NaCl高,其原因是 。
(6)由A、D、G中任两种元素构成甲、乙两种均含18个电子的分子,所含原子的数目依次为3、4。则甲分子的中心原子采取 杂化;1 mol乙分子含有 molσ键。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】按要求对下图中两极进行必要的联接并填空:

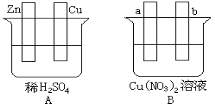
(1)在A图中,使铜片上冒H2气泡。对装置加以联接,则联接后的装置叫 。
电极反应式:锌板: ;铜板: 。
(2)在B图中,a、b两电极均为石墨,对装置加以联接,使a极析出铜,则b析出 。该装置叫 。电极反应式,a极: b极: 。经过一段时间后,停止反应并搅匀溶液,溶液的pH值 (升高、降低、不变),加入一定量的 (填化学式)后,溶液能恢复至与电解前完全一致。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列描述中不正确的是( )
A. CS2为Ⅴ形的极性分子 B. ClO3-的空间构型为三角锥形
C. SF6中有6对完全相同的成键电子对 D. SiF4和SO32-的中心原子均为sp3杂化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机物的结构可用“键线式”简化表示,如CH3-CH=CH-CH3可简写为![]() 。有机物X的键线式为
。有机物X的键线式为![]() ,Y是X的同分异构体,且属于芳香烃。下列有关Y的说法正确的是( )
,Y是X的同分异构体,且属于芳香烃。下列有关Y的说法正确的是( )
A.Y能使酸性KMnO4溶液褪色,所以是苯的同系物
B.Y能使溴水褪色,且静置后不分层
C.Y不能发生取代反应
D.Y能发生加聚反应生成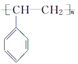
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com