
 开心试卷期末冲刺100分系列答案
开心试卷期末冲刺100分系列答案 双基同步导航训练系列答案
双基同步导航训练系列答案科目:高中化学 来源:不详 题型:填空题
| 元素代号 | W | R | X | Y | Z | Q |
| 原子半径/nm | 0.037 | 0.186 | 0.074 | 0.075 | 0.077 | 0.110 |
| 主要化合价 | +1 | +1 | -2 | -3,+5 | +2、+4 | -3、+5 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
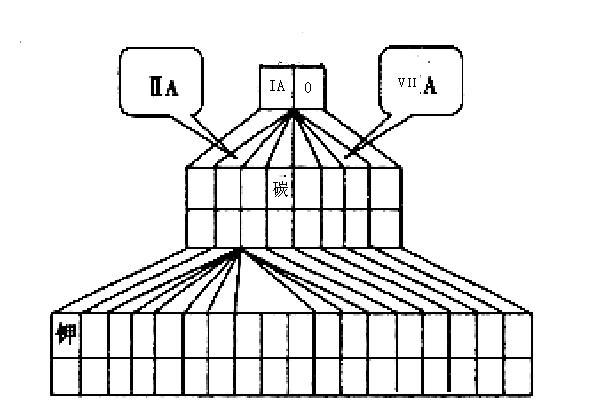
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题

查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.H2燃烧生成1molH2O(g)时,放出241.8kJ的热量 |
| B.H2的燃烧热为285.8kJ |
| C.O2前面的1/2表示参加反应的O2的物质的量 |
| D.1mol液态水变成水蒸气时吸收44kJ的热量 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.带相反电荷的离子之间的相互吸引作用称为离子键 |
B.质子数为1,中子数为1的一种氢原子可表示为: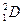 |
| C.某元素原子的最外层只有一个电子,它跟卤素结合时形成化学键不一定是离子键 |
| D.氧气和臭氧互为同位素 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com