
【题目】某种气体的摩尔质量为M g·mol-1,将标况下的该气体V L溶解在1000 g水中,该气体不与水反应,所得溶液密度为ρ g·cm-3,则所得溶液中溶质的物质的量浓度为 ( )mol·L-1
A.V/22.4B.V ρ/(MV+22400)
C.V ρ/22400D.1000V ρ/(MV+22400)
科目:高中化学 来源: 题型:
【题目】甲醇是一种新型燃料,甲醇燃料电池即将从实验室走向工业化生产。工业上一般以CO和H2为原料合成甲醇,该反应的热化学方程式为: CO(g)+ 2H2(g)![]() CH3OH(g) △H1=-116 kJ·mol-1
CH3OH(g) △H1=-116 kJ·mol-1
(1)已知:![]() △H2=-283 kJ·mol-1
△H2=-283 kJ·mol-1
![]() △H3=-242 kJ·mol-1
△H3=-242 kJ·mol-1
则表示1mol气态甲醇完全燃烧生成CO 2和水蒸气时的热化学方程式为:
_______________________________________________;
(2)在容积为1L的恒容容器中,分别研究在230℃、250℃、 270℃三种温度下合成甲醇的规律。右图是上述三种温度下不同的H2和CO的起始组成比(起始时CO的物质的量均为1mol)与CO平衡转化率的关系。请回答:
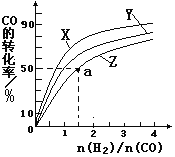
①在上述三种温度中,曲线Z对应的温度是__________
②利用图中a点对应的数据,计算出曲线Z在对应温度下CO(g)+ 2H2(g) ![]() CH3OH(g)的平衡常数K=_____________________。
CH3OH(g)的平衡常数K=_____________________。
(3)在某温度下,将一定量的CO和H2投入10L的密闭容器中,5min时达到平衡,各物质的物质的浓度(molL-1)变化如下表所示:
0min | 5min | 10min | |
CO | 0.1 | 0.05 | |
H2 | 0.2 | 0.2 | |
CH3OH | 0 | 0.04 | 0.05 |
若5min~10min只改变了某一条件,所改变的条件是_________________________;且该条件所改变的量是_______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用NA表示阿伏加德罗常数的值,下列说法正确的是
A. NA个氢氧化铁胶体粒子的质量为107g
B. 0.1 mol·L-1的NaHSO4溶液中,阳离子的数目之和为0.2NA
C. 100g质量分数为17%的H2O2水溶液中含O―O键数目为NA
D. 2.7g铝与足量的稀硫酸和氢氧化钠分别反应,得到氢气的体积在标况下均为3.36L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】分子式为C9H12O的某有机物与FeCl3溶液反应显色,又知其苯环上共有两个取代基,则该有机物的结构有( )
A.6种B.5种C.4种D.3种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各图均能表示甲烷的分子结构,按要求回答下列问题。
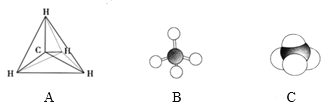
(1)甲烷的比例模型是______(填序号)。
(2)相对分子质量为100的烷烃的分子式是_____。
(3)甲烷与氯气的体积比为1:1,光照条件下在如图所示的装置中反应,则得到的产物为_____。
A.CH3Cl、HCl B.CCl4、HCl
C.CH3Cl、CH2Cl2 D.CH3Cl、CH2Cl2、CHCl3、CCl4、HCl

(4)甲烷最简单的同系物与氯气光照条件下反应,其生成物的化学式最多可能有_____种。
A.5 B.9 C.10 D.7
(5)经过几个小时的反应后,U形管右端的水柱变化是______。
A.升高 B.降低 C.不变 D.无法确定
(6)工业酒精含有甲醇,其结构简式为:CH3OH,可由甲烷经过一系列变化得到,写出甲醇与O2在铜作催化剂加热条件下的反应_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示,杠杆 AB 两端分别挂有体积相同、质量相等的空心铜球和空心铁球,调节杠 杆并使其在水中保持平衡,然后小心地向烧杯中央滴入浓 CuSO4 溶液,一段时间后,下列 有关杠杆的偏向判断正确的是(实验过程中,不考虑铁丝反应及两球的浮力变化)
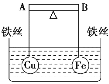
A. 杠杆为导体和绝缘体时,均为 A 端高 B 端低
B. 杠杆为导体和绝缘体时,均为 A 端低 B 端高
C. 当杠杆为绝缘体时,A 端低 B 端高;为导体时,A 端高 B 端低
D. 当杠杆为绝缘体时,A 端高 B 端低;为导体时,A 端低 B 端高
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某学生利用下面实验装置探究盐桥式原电池的工作原理(Cu 64)。
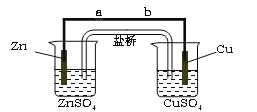
按照实验步骤依次回答下列问题:
⑴导线中电子流向为 (用a、b 表示)。
⑵写出装置中锌电极上的电极反应式: ;
⑶若装置中铜电极的质量增加0.64g,则导线中转移的电子数目为 ;
(不许用“NA”表示)
(4)装置中盐桥中除添加琼脂外,还要添加KCl的饱和溶液,电池工作时,对盐桥中的K+,Cl-的移动方向描述正确的是 。
A. 盐桥中的K+向左侧烧杯移动、Cl-向右侧烧杯移动
B. 盐桥中的K+向右侧烧杯移动、Cl-向左侧烧杯移动
C. 盐桥中的K+、Cl-都向右侧烧杯移动
D. 盐桥中的K+、Cl-几乎都不移动
⑸若ZnSO4溶液中含有杂质Cu2+,会加速Zn电极的腐蚀、还可能导致电流在较短时间内衰减。欲除去Cu2+,最好选用下列试剂中的 (填代号)。
A. NaOH B. Zn C. Fe D. H2SO4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于容量瓶的使用,下列操作正确的是
A. 使用前要检验容量瓶是否漏液
B. 用蒸馏水荡洗后必须要将容量瓶烘干
C. 为了便于操作,浓溶液稀释或固体溶解可直接在容量瓶中进行
D. 为了使所配溶液浓度均匀,定容结束后,手握瓶颈,左右振
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com