
����Ŀ��Ϊ�����Դ��ȱ���⣬��ҵ������Ӧ�������û�ѧ�ܡ�
��1��25�棬1.01��105Paʱ��ʵ���ã�4g������O2����ȫȼ������Һ̬ˮ���ų�572kJ�����������ʾH2��ȼ���ȵ��Ȼ�ѧ����ʽΪ________________________________��
��2����ͼ��ij�ʼDZ�����ʹ�õļ״�ȼ�ϵ�صĽṹʾ��ͼ���ŵ�ʱ�״�Ӧ��_________��ͨ�루�a����b����������ڲ�H+��_________������ҡ����ƶ���д����ظ����ĵ缫��Ӧʽ_________________________________��

��3���ӻ�ѧ���ĽǶȷ�������ѧ��Ӧ�Ĺ��̾��Ƿ�Ӧ��Ļ�ѧ�����ƻ���������Ļ�ѧ�����γɹ��̡�
��ѧ�� | H-H | N-H | N��N |
����/ kJ��mol-1 | 436 | a | 945 |
��֪��N2(g)+3H2(g)=2NH3(g) ��H=-93 kJ��mol-1���Ը��ݱ������м������ݼ���a����ֵ__________��
��4����֪��C��s��ʯī��+O2(g)=CO2(g) ��H1=-393.5 kJ��mol-1 ��
2H2(g)+O2(g)=2H2O(1) ��H2=-571.6 kJ��mol-1 ��
2C2H2(g)+5O2(g)=4CO2(g)+2H2O(1) ��H3=-2599 kJ��mol-1 ��
���ݸ�˹���ɣ����㷴Ӧ2C��s��ʯī��+H2(g)=C2H2(g)�ġ�H=_______________��
���𰸡� H2(g)+![]() O2(g)=H2O(1) ��H=-286kJ/mol a �� CH3OH+H2O-6e-=CO2+6H+ 391 +226.7kJ��mol-1
O2(g)=H2O(1) ��H=-286kJ/mol a �� CH3OH+H2O-6e-=CO2+6H+ 391 +226.7kJ��mol-1
��������(1)ȼ������1mol��ȼ����ȫȼ�������ȶ�������ų�������������n=![]() ����1mol������ȫȼ�շų�������������Ȼ�ѧ����ʽ����д����д���Ȼ�ѧ����ʽ��(2)���ݵ��������֪aΪ��������������������Ӧ��bΪ����������ԭ��Ӧ����Һ������������������(3)���ݷ�Ӧ�ȵ��ڷ�Ӧ����ܼ���-��������ܼ���������(4)���ø�˹���ɷ������
����1mol������ȫȼ�շų�������������Ȼ�ѧ����ʽ����д����д���Ȼ�ѧ����ʽ��(2)���ݵ��������֪aΪ��������������������Ӧ��bΪ����������ԭ��Ӧ����Һ������������������(3)���ݷ�Ӧ�ȵ��ڷ�Ӧ����ܼ���-��������ܼ���������(4)���ø�˹���ɷ������
(1)4g������2mol��O2����ȫȼ������Һ̬ˮ���ų�572kJ����������1mol������������ȼ������Һ̬ˮ���ų�286kJ�����������ʾH2��ȼ���ȵ��Ȼ�ѧ����ʽΪ��H2(g)+![]() O2(g)�TH2O(l)��H=-286kJ/mol���ʴ�Ϊ��H2(g)+
O2(g)�TH2O(l)��H=-286kJ/mol���ʴ�Ϊ��H2(g)+ ![]() O2(g)�TH2O(l)��H=-286kJ/mol��
O2(g)�TH2O(l)��H=-286kJ/mol��
(2)ԭ����е��ӴӸ��������·�������������ݵ��������֪a�缫Ϊ�������״��ڸ����Ϸ���������Ӧ���缫��ӦʽΪCH3OH+H2O-6e-�TCO2+6H+��bΪ�����������õ��ӷ�����ԭ��Ӧ���缫��ӦʽΪ3O2+12e-+12H+�T6H2O�����������������Ҳ࣬�ʴ�Ϊ��a���ң�CH3OH+H2O-6e-�TCO2+6H+��
(3)N2(g)+3H2(g)2NH3(g)��H=945kJmol-1+436kJmol-1��3-akJmol-1��6=-93kJmol-1��a=391 kJmol-1���ʴ�Ϊ��391��
(4)��C(s��ʯī)+O2(g)�TCO2(g)��H=-393.5kJmol-1����2H2(g)+O2(g)�T2H2O(l)��H=-571.6kJmol-1����2C2H2(g)+5O2(g)�T4CO2(g)+2H2O(l)��H=-2599kJmol-1�����ø�˹���ɽ�����2+����![]() -����
-����![]() �ɵã�2C(s��ʯī)+H2(g)=C2H2(g)��H=(-393.5kJ/mol)��2+
�ɵã�2C(s��ʯī)+H2(g)=C2H2(g)��H=(-393.5kJ/mol)��2+![]() ��(-571.6kJ/mol)-
��(-571.6kJ/mol)- ![]() ��(-2599 kJ/mol)=+226.7kJmol-1���ʴ�Ϊ��+226.7kJmol-1��
��(-2599 kJ/mol)=+226.7kJmol-1���ʴ�Ϊ��+226.7kJmol-1��


 Happy holiday���ּ��������ҵ�㶫���������ϵ�д�
Happy holiday���ּ��������ҵ�㶫���������ϵ�д� ���������������Բ��������ϵ�д�
���������������Բ��������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ijͬѧ���������װ��������ȡSO2����֤SO2�����ʡ���֪��1.0mol��L-1Fe(NO3)3��Һ��pH=1��
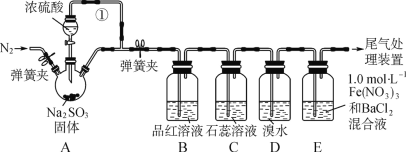
��1��װ��A����������Ũ�������������Ϊ___�����ܢٵ�������_______��
��2��B��C��D����װ�÷ֱ��Ⱥ���֤��SO2����Щ����_____(����ĸ)��
A. �����ԡ����ԡ���ԭ�� B. ��ԭ�ԡ����ԡ���ԭ��
C. Ư���ԡ����ԡ���ԭ�� D. Ư���ԡ����ԡ�������
��3��ʵ��ǰ����N2��Ŀ����________��
��4��װ��E�в����˰�ɫ��������ɷ���____(�ѧʽ)������E�в�����ɫ�����Ŀ���ԭ��(д����)�����ܢ٣�_____�����ܢڣ�______��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����һ�������18molL��1��Ũ�����м������ͭƬ�����ȣ�����ԭ����������ʵ���Ϊ0.9mol����Ũ�����ʵ�����Ϊ�� ��
A������50 mL B������50 mL C������100 mL D������100 mL
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���뵼����ҵ����һ�仰������ɳ̲���û����������оƬ�IJ����ǹ裬�����йع輰�仯����������ȷ���ǣ� ��
A. ˮ��������������� B. ���ά����Ҫ�ɷ��Ǹߴ���
C. ����ʯӢǯ�����������������ƹ��� D. �������費���κ��ᷴӦ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����и������ʵ�ϡ��Һ���Ӧ��������ǰ�ߵ�����ߣ����Ǻ��ߵ���ǰ�ߣ���Ӧ������ͬ����( )
A. AlCl3��NaOH B. H2SO4��Ba(OH)2
C. NaAlO2��H2SO4 D. Na2CO3��HCl
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���±���Ԫ�����ڱ���һ���֣���Ա��еĢ١�����Ԫ�أ���д���пհף�
���� ���� | I A | IIA | IIIA | IVA | VA | VIA | VIIA | 0�� |
�ڶ����� | �� | �� | �� | |||||
�������� | �� | �� | �� | �� | �� | |||
�������� | �� | �� |
(1)����ЩԪ���У���ѧ��������õ���:_____(�����Ԫ�ط��ţ���ͬ)��ԭ�ӽṹʾ��ͼΪ_______��Ԫ�آ�����Ϊ_________��
(2)������������Ӧ��ˮ�����У�������ǿ�Ļ�����ķ���ʽ��_________��������ǿ�Ļ�����ĵ���ʽ��:________________��
(3)�õ���ʽ��ʾԪ�آ���Ļ�������γɹ���:___________________���û���������_____(����ۡ������ӡ�)�����
(4)��ʾ����ߵĻ�����ĵ���ʽ________���û���������_______(����ԡ��Ǽ��ԡ�)���γɵġ�
(5)�ۡ��ޡ�������Ԫ���γɵ����ӣ����Ӱ뾶�ɴ�С��˳����_________(�û�ѧʽ��ʾ)��
(6)Ԫ�آ۵ļ��⻯��ĽṹʽΪ_____�����⻯�ﳣ���º�Ԫ�آߵĵ��ʷ�Ӧ�����ӷ���ʽΪ________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������MgCl2��AlCl3��CuCl2��FeCl3��NH4Cl������Һ��ֻ��һ���Լ����������������Լ���
A. ��ˮ B. AgNO3��Һ C. ŨNaOH��Һ D. NaCl��Һ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼ�Dz��ֶ�����Ԫ�ػ��ϼ���ԭ�������Ĺ�ϵͼ������˵������ȷ����

A. ��̬�⻯����ȶ��ԣ�R>W
B. X��Y�����γ�ԭ�Ӹ�����Ϊ1:1��1:2���������ӻ�����
C. ��X��Y��Z��W��R����Ԫ���γɵļ������а뾶��С����X2-
D. Y��Z��������������Ӧ��ˮ���������Ӧ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪a��b��c��d���ֶ���������Ԫ�أ������ڱ������λ������ͼ��ʾ������˵����ȷ���ǣ� ��

A. a��c��Ԫ�ص��������һ�����
B. d��ԭ��������������b��ԭ��������3��
C. ��cԪ������������Ӧ��ˮ������ǿ�ᣬ��dԪ�صĵ��ʾ���ǿ������
D. c������������Ӧ��ˮ���������d������������Ӧ��ˮ����
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com