
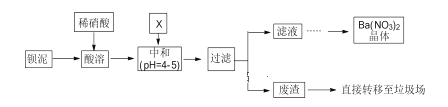
【题目】.Ba(NO3)2可用于生产烟花。某主要生产 BaCl2、BaCO3、BaSO4 的化工厂利用某种钡泥[主要含有 BaCO3、Ba(FeO2)2、极少量 CuCO3 等]制取 Ba(NO3)2 晶体,其部分工艺流程如下:
已知:Fe3+和Fe2+以氢氧化物形式沉淀完全时,溶液的 pH 分别为 3.2 和 9.7。
(1)酸溶时通常不使用浓硝酸的原因是__________。
(2)酸溶后溶液中pH=1,Ba(FeO2)2 与HNO3 的反应化学方程式为____________。
(3)该厂结合本厂实际,中和选用的 X 为__________(填化学式);中和使溶液中__________(填离子符号)的浓度减少(中和引起的溶液体积变化可忽略)。
(4)滤液得到 Ba(NO3)2 晶体的操作依次为_____、过滤。
(5)该厂生产的 Ba(NO3)2 晶体含有少量 Cu2+ ,可通过洗涤的方法除去。证明晶体已经洗涤干净的操作方法是_______________________。
(6)Ba2+致死量为355mg/kg。误食Ba2+可以服用MgSO4 溶液解毒,涉及到的离子反应方程式为___________; 为了减少环境污染,请对上述流程中不合理的设计进行改进,改进措施是___________。
【答案】浓HNO3易挥发、分解 Ba(FeO2)2+8HNO3=Ba(NO3)2+2Fe(NO3)3+4H2O BaCO3 Fe3+、H+ 蒸发浓缩、冷却结晶 取最后一次洗涤液 少许于试管中,滴加NaOH溶液无蓝色沉淀产出 Ba2+ + SO42-=BaSO4 ↓ 洗涤废渣并回收洗涤液
【解析】
BaCO3含少量CuCO3 ,Ba(FeO2)2、Ba(NO3)2等杂质,其中Ba(FeO2)2中钡元素为+2价,铁元素为+3价,加入硝酸,在容器中充分溶解得到溶液,此溶液中含有钡离子,铜离子,三价铁离子,可加入X是碳酸钡,调节溶液pH=4-5,使铁离子,铜离子水解生成氢氧化铁沉淀,氢氧化铜沉淀,过滤后废渣是氢氧化铁,氢氧化铜,滤液中主要含有硝酸,硝酸钡,经蒸发浓缩,冷却结晶,过滤可得硝酸钡晶体。
(1)酸溶时不使用的原因是浓硝酸易挥发,分解;
(2)酸溶后溶液中中pH=1,Ba(FeO2)2 与HNO3 的反应生成硝酸钡,硝酸铁和水,反应的化学方程式为Ba(FeO2)2+8HNO3=Ba(NO3)2+2Fe(NO3)3+4H2O;
(3)该厂结合本厂实际,中和选用的 X必须能消耗过量硝酸并使铁离子沉淀而除去,且不引人新的杂质,可为BaCO3;中和使溶液中Fe3+、H+浓度减少;
(4)滤液得到硝酸钡晶体的操作依次为蒸发浓缩、冷却结晶;
(5)晶体表面可能有Cu2+ ,如果洗涤干净,说明没有Cu2+ ,所以操作是取最后一次洗涤液 少许于试管中,滴加NaOH溶液无蓝色沉淀产出;
(6)误食Ba2+可以服用MgSO4 溶液解毒,涉及到的离子反应方程式为Ba2+ + SO42-=BaSO4 ↓;避免引起污染,改进措施是洗涤废渣并回收洗涤液;


科目:高中化学 来源: 题型:
【题目】研究表明,氮氧化物和二氧化硫在形成雾霾时与大气中的氨有关(如下图所示)。下列叙述错误的是

A. 雾和霾的分散剂相同
B. 雾霾中含有硝酸铵和硫酸铵
C. NH3是形成无机颗粒物的催化剂
D. 雾霾的形成与过度施用氮肥有关
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫酸亚铁铵受热分解的反应方程式为2(NH4)2Fe(SO4)2![]() Fe2O3+2NH3↑+N2↑+4SO2↑+5H2O,用NA表示阿伏加德罗常数的值。下列说法正确的是
Fe2O3+2NH3↑+N2↑+4SO2↑+5H2O,用NA表示阿伏加德罗常数的值。下列说法正确的是
A. 1 L 0.1 mol·L1 (NH4)2Fe(SO4)2溶液中Fe2+的数目为0.1NA
B. 将1 mol SO2和1 mol O2充分反应后,其分子总数为1.5NA
C. 标准状况下,每生成15.68 L气体转移电子数目为0.8NA
D. 常温常压下,3.0 g 15N2中含有的中子总数为1.4NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一体积可变密闭容器中,加入一定量的X、Y,发生反应mX(g)![]() nY(g) ΔH=Q kJ·mol-1。反应达到平衡时,Y的物质的量浓度与温度、气体体积的关系如下表所示:
nY(g) ΔH=Q kJ·mol-1。反应达到平衡时,Y的物质的量浓度与温度、气体体积的关系如下表所示:

下列说法正确的是
A.m<n
B.Q<0
C.温度不变,压强增大,Y的质量分数减少
D.体积不变,温度升高,平衡向逆反应方向移动
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】近年来,我国储氢碳管研究获得重大进展,电弧法合成碳纳米管,常伴有大量物质——碳纳米颗粒,这种碳纳米颗粒可用氧化气化法提纯,其反应的化学方程式为:
3C + 2K2Cr2O7 + 8H2SO4(稀)= 3CO2↑ + 2K2SO4 + 2Cr2(SO4)3 + 8 H2O
请回答下列问题。
(1)H2O的摩尔质量为___________,0.18g H2O的物质的量为_______________mol
(2)配制0.1mol/L H2SO4溶液500mL,则需要H2SO4的质量为_____________g
(3)在上述的反应中,若生成22g CO2
ⅰ.标准状况下,CO2的体积为_________L
ⅱ.转移电子的数目为________________
(4)标准状况下,由CO和CO2组成的混合气体为6.72 L,质量为12 g,则该混合气体的平均相对分子质量是_____________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定温度下,把1molN2和3molH2通入一个一定容积的密闭的容器里,发生如下反应:N2+3H2![]() 2NH3;当此反应进行到一定程度时,反应混和物就处于化学平衡状态。现在该容器中,维持温度不变,令a、b、c分别代表初始加入的N2、H2和NH3的物质的量(mol)。如果a、b、c取不同的数值,它们必须满足一定的相互关系,才能保证达到平衡时,反应混合物中三种气体的百分含量仍跟上述平衡时的完全相同。请填写下列空白:
2NH3;当此反应进行到一定程度时,反应混和物就处于化学平衡状态。现在该容器中,维持温度不变,令a、b、c分别代表初始加入的N2、H2和NH3的物质的量(mol)。如果a、b、c取不同的数值,它们必须满足一定的相互关系,才能保证达到平衡时,反应混合物中三种气体的百分含量仍跟上述平衡时的完全相同。请填写下列空白:
(1)若a=0,b=0,则c=__________。
(2)若a=0.5,则b=__________和c=__________。
(3)a、b、c取值必须满足的一般条件是:请用两个方程式表示,其中一个只含a和c,另一个只含b和c______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A.HCl和NaOH反应的中和热ΔH=-57.3 kJ/mol,则H2SO4和Ba(OH)2反应的中和热ΔH=2×(-57.3) kJ/mol
B.CO(g)的燃烧热是ΔH=-283.0 kJ/mol,则2CO2(g)=2CO(g)+O2(g)反应的ΔH=+2×283.0 kJ/mol
C.101kPa时,1mol碳燃烧所放出的热量为碳的燃烧热
D.反应物所具有的总能量小于生成物所具有的总能量时,△H<0
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图是由常见元素组成的一些单质及其化合物之间的转化关系图。各方框表示有关的一种反应物或生成物(部分物质已经略去)。其中A、B、D在常温下均为无色无味的气体,C是能使湿润的红色石蕊试纸变蓝的气体,M是最常见的无色液体。

(1)写出C→E的化学方程式: 。
(2)实验室常用加热两种固体混合物的方法制备物质C,其化学方程式为: ,干燥C常用 (填写试剂名称)。
(3)E物质遇到D物质时,会观察到 现象,若用排水法收集F,则最终集气瓶中收集到的气体为 (填写物质的化学式)。
(4)写出A→D的化学方程式: 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】H2C2O4为二元弱酸。20℃时,配制一组c(H2C2O4)+ c(HC2O4-)+ c(C2O42-)="0.100" mol·L-1的H2C2O4和NaOH混合溶液,溶液中部分微粒的物质的量浓度随pH的变化曲线如右图所示。下列指定溶液中微粒的物质的量浓度关系一定正确的是

A. pH=2.5的溶液中:c(H2C2O4)+ c(C2O42-)> c(HC2O4-)
B. c(Na+)="0.100" mol·L-1的溶液中:c(H+)+c(H2C2O4)=c(OH-)+ c(C2O42-)
C. c(HC2O4-)= c(C2O42-)的溶液中:c(Na+)>0.100 mol·L-1+ c(HC2O4-)
D. pH=7的溶液中:c(Na+)>2c(C2O42-)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com