
·ÖĪö £Ø1£©øł¾Żv=$\frac{”÷c}{”÷t}$¼ĘĖć·“Ó¦ĖŁĀŹ£»
£Ø2£©YµÄ×Ŗ»ÆĀŹĪŖ$\frac{±ä»ÆĮæ}{ĘšŹ¼Įæ}$£»
£Ø3£©øł¾ŻĪļÖŹµÄĮæµÄ±ä»ÆÓė»Æѧ¼ĘĮæŹż³ÉÕż±ČŹéŠ“»Æѧ·½³ĢŹ½£»
£Ø4£©ÓÉĶ¼ĻóæÉÖŖÕżÄę·“Ó¦ĖŁĀŹŌö“ó£¬Ę½ŗāĆ»ŅĘ¶Æ£®
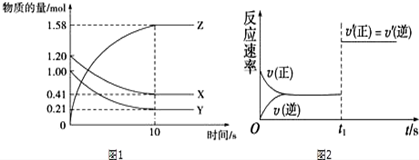
½ā“š ½ā£ŗ£Ø1£©¦Ķ£ØZ£©=$\frac{\frac{1.58mol}{2L}}{10s}$=0.079mol/£ØL•s£©£¬¹Ź“š°øĪŖ£ŗ0.079mol/£ØL•s£©£»
£Ø2£©YµÄ×Ŗ»ÆĀŹĪŖ$\frac{±ä»ÆĮæ}{ĘšŹ¼Įæ}$=$\frac{1-0.21}{1}$”Į100%=79%£¬¹Ź“š°øĪŖ£ŗ79%£»
£Ø3£©ÓÉĶ¼ĻóæÉŅŌ擳ö£¬·“Ó¦µ½10sŹ±£¬XµÄĪļÖŹµÄĮæ¼õŠ”£¬±ä»ÆÖµĪŖ1.20mol-0.41mol=0.79mol£¬
YµÄĪļÖŹµÄĮæ¼õŠ”£¬±ä»ÆÖµĪŖ1.0mol-0.21mol=0.79mol£¬ŌņX”¢YĪŖ·“Ó¦Īļ£¬
ZµÄĪļÖŹµÄĮæŌö¶ą£¬±ä»ÆÖµĪŖ1.58mol£¬ĪŖÉś³ÉĪļ£¬
øł¾ŻĪļÖŹµÄĮæµÄ±ä»ÆÓė»Æѧ¼ĘĮæŹż³ÉÕż±Č£¬
ŌņÓŠn£ØX£©£ŗn£ØY£©£ŗn£ØZ£©=0.79mol£ŗ0.79mol£ŗ1.58mol=1£ŗ1£ŗ2£¬
ĖłŅŌ·“Ó¦µÄ·½³ĢŹ½ĪŖX£Øg£©+Y£Øg£©?2Z£Øg£©£¬
¹Ź“š°øĪŖ£ŗX£Øg£©+Y£Øg£©?2Z£Øg£©£»
£Ø4£©ÓÉĶ¼ĻóæÉÖŖÕżÄę·“Ó¦ĖŁĀŹŌö“ó£¬Ę½ŗāĆ»ŅĘ¶Æ£»
A£®t1Ź±æĢ£¬Ōö“óĮĖXµÄÅØ¶Č£¬Ę½ŗāÕżŅĘ£¬²»·ūŗĻĢāŅā£¬¹ŹA“ķĪó£»
B£®t1Ź±æĢ£¬ÉżøßĮĖĢåĻµĪĀ¶Č£¬Ę½ŗāŅĘ¶Æ£¬²»·ūŗĻĢāŅā£¬¹ŹB“ķĪó
C£®t1Ź±æĢ£¬ĖõŠ”ĮĖČŻĘ÷Ģå»ż£¬ĖŁĀŹŌö“ó£¬ÓÉÓŚ·“Ó¦Ē°ŗó¼ĘĮæŹżĻąµČ£¬Ę½ŗā²»ŅĘ¶Æ£¬·ūŗĻĢāŅā£¬¹ŹCÕżČ·£»
D£®t1Ź±æĢ£¬Ź¹ÓĆĮĖ“߻ƼĮ£¬ĖŁĀŹŌö“ó£¬Ę½ŗā²»ŅĘ¶Æ£¬·ūŗĻĢāŅā£¬¹ŹDÕżČ·£»
¹Ź“š°øĪŖ£ŗCD£®
µćĘĄ ±¾Ģā漲鷓ӦĖŁĀŹµÄ¼ĘĖćĘ½ŗāĶ¼ĻóĪŹĢā£¬ĢāÄæÄŃ¶Č²»“ó£¬×¢Ņā°ŃĪÕĪļÖŹµÄĮæµÄ±ä»ÆÓė»Æѧ¼ĘĮæŹż³ŹÕż±Č£¬ŅŌ“ĖŹéŠ“»Æѧ·½³ĢŹ½£®


 Ó„ÅɽĢøØĻĪ½Ó½Ģ²ÄŗÓ±±½ĢÓż³ö°ęÉēĻµĮŠ“š°ø
Ó„ÅɽĢøØĻĪ½Ó½Ģ²ÄŗÓ±±½ĢÓż³ö°ęÉēĻµĮŠ“š°ø ³õÖŠŹīĘŚĻĪ½ÓĻµĮŠ“š°ø
³õÖŠŹīĘŚĻĪ½ÓĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
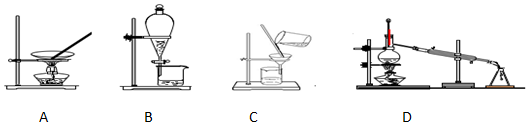
| A£® | Õō·¢”¢¹żĀĖ”¢·ÖŅŗ”¢ÕōĮó | B£® | Õō·¢”¢·ÖŅŗ”¢¹żĀĖ”¢ÕōĮó | ||
| C£® | Õō·¢”¢ÕōĮ󔢹żĀĖ”¢·ÖŅŗ | D£® | Õō·¢”¢ÕōĮ󔢷ÖŅŗ”¢¹żĀĖ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | 9.0g²ŻĖįÖŠ¹²ÓƵē×Ó¶ŌŹżÄæĪŖ0.9NA | |
| B£® | 9.0g²ŻĖį±»NaClOŃõ»ÆÉś³ÉCO2£¬×ŖŅʵĵē×ÓŹżĪŖ0.2NA | |
| C£® | 9.0g²ŻĖįČÜÓŚĖ®£¬ĘäÖŠC2O${\;}_{4}^{2-}$ŗĶHC2O${\;}_{4}^{-}$µÄĪ¢Į£ŹżÖ®ŗĶĪŖ0.1NA | |
| D£® | 9.0g²ŻĖįŹÜČČĶźČ«·Ö½āĪŖCO2”¢CO”¢H2O£¬±ź×¼×“æöĻĀ²āµĆÉś³ÉµÄĘųĢåĢå»żĪŖ4.48L |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŹµŃéĢā
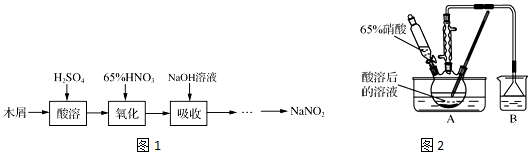
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | Ō×Ó°ė¾¶£ŗrW£¼rX£¼rY | |
| B£® | ĖÄÖÖŌŖĖŲŠĪ³ÉµÄµ„ÖŹ×ī¶ąÓŠ6ÖÖ | |
| C£® | ĖÄÖÖŌŖĖŲ¾łæÉÓėĒāŌŖĖŲŠĪ³É18µē×Ó·Ö×Ó | |
| D£® | ĖÄÖÖŌŖĖŲÖŠ£¬ZµÄ×īøß¼ŪŃõ»ÆĪļ¶ŌÓ¦Ė®»ÆĪļµÄĖįŠŌ×īĒæ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ¹ā»ÆѧŃĢĪķ | B£® | Ė®Ģåø»ÓŖŃų»Æ | C£® | ³ōŃõæÕ¶“ | D£® | ĖįÓź |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ĀČĘųČÜÓŚĖ®£ŗCl2+H2OØT2H++Cl-+ClO- | |
| B£® | µČĪļÖŹµÄĮæµÄBa£ØOH£©2ÓėNH4HSO4ŌŚĻ”ČÜŅŗÖŠ·“Ó¦£ŗBa2++2OH-+2H++SO42-ØTBaSO4”ż+2H2O | |
| C£® | NaOHČÜŅŗÓė×ćĮæCa£ØHCO3£©2ČÜŅŗ·“Ó¦£ŗCa2++2HCO3-+2OH-ØTCaCO3”ż+CO32-+2H2O | |
| D£® | ĻņAl2£ØSO4£©3ČÜŅŗÖŠ¼ÓČė¹żĮæ°±Ė®£ŗAl3++3NH3•H2OØTAl£ØOH£©3”ż+3NH4+ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ¶ąŃ”Ģā
| A£® | c£ØCO32-£©µÄ“󊔹ŲĻµĪŖ£ŗ¢Ś£¾¢Ż£¾¢Ū£¾¢Ü£¾¢Ł | |
| B£® | ½«ČÜŅŗÕōøÉ×ĘÉÕŗóÖ»ÓŠ¢Ł²»ÄܵƵ½¶ŌÓ¦µÄ¹ĢĢåĪļÖŹ | |
| C£® | ¢Ū¢Ü¢Ż¼ČÄÜÓėŃĪĖį·“Ó¦£¬ÓÖÄÜÓėNaOHČÜŅŗ·“Ó¦ | |
| D£® | c£ØHCO3-£©µÄ“󊔹ŲĻµĪŖ£ŗ¢Ü£¾¢Ū£¾¢Ż£¾¢Ś£¾¢Ł |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | C£Øs£©+O2£Øg£©=CO2£Øg£©”÷H=-393.5kJ/mol | B£® | 2SO2£Øg£©+O2£Øg£©=SO3£Øg£©”÷H=-196.6kJ/mol | ||
| C£® | H2£Øg£©+$\frac{1}{2}$O2£Øg£©=H2O£Øl£©”÷H=-285.8kJ/mol | D£® | 2H2£Øg£©+O2£Øg£©=2H2O£Øl£©”÷H=-517.6kJ/mol |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com