
温度一定时, 于密闭容器中发生可逆反应: mA(气) + nB(气)  pC(气), 达到平衡后,若将混合气体的体积压缩到原来的 1/2, 当再次达到平衡时, C的浓度为原平衡时C的浓度的 1.9 倍,则下列叙述中正确的是
pC(气), 达到平衡后,若将混合气体的体积压缩到原来的 1/2, 当再次达到平衡时, C的浓度为原平衡时C的浓度的 1.9 倍,则下列叙述中正确的是
A.平衡向逆反应方向移动
B.C气体的体积分数增大
C.气体A的转化率升高
D.m + n > p
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源:2014秋浙江省杭州地区六校高二上学期期中考试化学试卷(解析版) 题型:选择题
下图是用铜片、银片、Cu(NO3) 2溶液、AgNO3溶液、导线和盐桥(装有琼脂—KCl的U型管)构成的原电池。
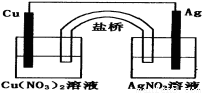
以下有关该原电池的叙述错误的是:
①电子由铜电极经外电路移到银电极,然后从内电路中移回铜电极
②正极反应为:Ag+ + e- = Ag
③实验中,用另外的银片替代盐桥,该原电池仍能继续工作
④将铜片浸入AgNO3溶液中发生的化学反应与该原电池反应相同
A.②④ B.②③ C.①④ D.①③
查看答案和解析>>
科目:高中化学 来源:2014秋河北省、临漳一中、永年二中高二上学期期中联考化学试卷(解析版) 题型:选择题
有一合金由X、Y、Z、W四种金属组成,若将合金放入盐酸中只有Z、Y能溶解;若将合金置于潮湿空气中,表面只出现Z的化合物;若将该合金做阳极,用X盐溶液作电解液,通电时四种金属都以离子形式进入溶液中,但在阴极上只析出X。这四种金属的活动性顺序是
A.Y>Z>W>X B.Z>Y>W>X
C.W>Z>Y>X D.X>Y>Z>W
查看答案和解析>>
科目:高中化学 来源:2014秋河北省、临漳一中、永年二中高二上学期期中联考化学试卷(解析版) 题型:选择题
下列电离方程式中正确的是
A.NH3·H2O===NH+OH-
B.KClO3===K++Cl-+3O2-
C.CH3COOH===CH3COO-+H+
D.NaOH===Na++OH-
查看答案和解析>>
科目:高中化学 来源:2014秋河北省高二上学期期中化学试卷(解析版) 题型:填空题
研究NO2、SO2 、CO等大气污染气体的处理具有重要意义。
(1)NO2可用水吸收,相应的化学反应方程式为 。利用反应6NO2+ 8NH3 7N2+12 H2O也可处理NO2。当转移1.2mol电子时,消耗的NO2在标准状况下是 L。
7N2+12 H2O也可处理NO2。当转移1.2mol电子时,消耗的NO2在标准状况下是 L。
(2)已知:2SO2(g)+O2(g) 2SO3(g) ΔH=?196.6 kJ·mol-1
2SO3(g) ΔH=?196.6 kJ·mol-1
2NO(g)+O2(g) 2NO2(g) ΔH =?113.0 kJ·mol-1
2NO2(g) ΔH =?113.0 kJ·mol-1
则反应NO2(g)+SO2(g) SO3(g)+NO(g)的ΔH = kJ·mol-1。
SO3(g)+NO(g)的ΔH = kJ·mol-1。
一定条件下,将NO2与SO2以体积比1:2置于密闭容器中发生上述反应,下列能说明反应达到平衡状态的是 。
a.体系压强保持不变
b.混合气体颜色保持不变
c.SO3和NO的体积比保持不变
d.每消耗1 mol SO3的同时生成1 molNO2
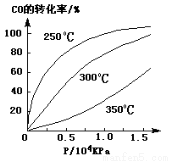
(3)CO可用于合成甲醇,反应方程式为CO(g)+2H2(g) CH3OH(g)。CO在不同温度下的平衡转化率与压强的关系如下图所示。该反应ΔH 0(填“>”或“ <”)。实际生产条件控制在250℃、1.3×104kPa左右,选择此压强的理由是 。
CH3OH(g)。CO在不同温度下的平衡转化率与压强的关系如下图所示。该反应ΔH 0(填“>”或“ <”)。实际生产条件控制在250℃、1.3×104kPa左右,选择此压强的理由是 。
查看答案和解析>>
科目:高中化学 来源:2014秋河北省高二上学期期中化学试卷(解析版) 题型:选择题
一定条件下的某密闭容器中,进行如下反应并建立平衡:2X(g)+Y(g) Z(g)+W(g);ΔH<0若改变某一条件,下列说法正确的是
Z(g)+W(g);ΔH<0若改变某一条件,下列说法正确的是
A.使用催化剂或缩小容器容积,平衡均不发生移动
B.升温既可以提高反应速率又可以提高X的转化率
C.向容器中加入少量Z,平衡后混合气体中Z的浓度变小
D.向容器中加入一定量的Y,上述反应的ΔH不变
查看答案和解析>>
科目:高中化学 来源:2014秋河北省高二上学期期中化学试卷(解析版) 题型:选择题
工业上制硫酸的第二步反应:2SO2(g)+O2(g) 2SO3(g) △H<0,反应达到平衡后,改变某一个条件,下列示意图曲线①~⑧中正确的是
2SO3(g) △H<0,反应达到平衡后,改变某一个条件,下列示意图曲线①~⑧中正确的是
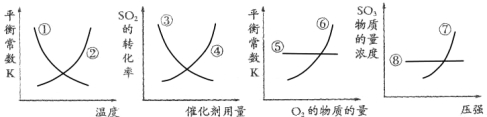
A.①⑥⑧ B.①⑤⑦ C.②③④ D.③⑥⑦
查看答案和解析>>
科目:高中化学 来源:2014秋江苏省东台市高二第一学期期中考试化学试卷(解析版) 题型:选择题
化合物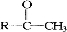 与NaOH溶液、碘水三者混和后可发生如下反应:
与NaOH溶液、碘水三者混和后可发生如下反应:
①I2 + 2NaOH  NaI + NaIO + H2O
NaI + NaIO + H2O
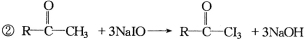
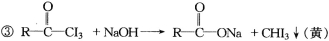
此反应称为碘仿反应,根据上述反应方程式,推断下列物质中能发生碘仿反应的有
A.CH3CH2COCH2CH3 B.CH3COCH2CH3
C.CH3CH2COOCH3 D.CH3OOCH
查看答案和解析>>
科目:高中化学 来源:2014秋广东省揭阳市高二第一学期期中考试化学试卷(解析版) 题型:填空题
(8分)已知FeCl3溶液能腐蚀铜板,生成CuCl2和FeCl2,请根据要求回答下列问题:
(1)写出该反应的离子方程式并用单线桥法标出电子转移的方向和数目:______________________
(2)向(1)中反应后的溶液中加入酸性KMnO4溶液(锰元素的化合价为+7),还原产物为Mn2+,则参与反应的氧化剂与还原剂的物质的量之比为_____________;判断Cu2+、MnO4-、Fe3+的氧化性由强到弱的顺序是(用离子符号表示)________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com