
(14分)据图回答下列问题: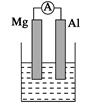
Ⅰ、(1)若烧杯中溶液为稀硫酸,则观察到的现象是 ___________________
负极反应式为:______________________________。
(2)若烧杯中溶液为氢氧化钠溶液,则负极为________(填Mg或Al),总反应化学方程式为____________________________________。
Ⅱ、由Al、Cu、浓硝酸组成原电池,其正极的电极反应式为
Ⅲ、中国科学院长春应用化学研究所在甲醇燃料电池技 术方面获得新突破,组装出了自呼吸电池及主动式电堆。甲醇燃料电池的工作原理如下图所示。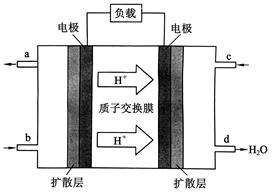
①该电池工作时,b口通入的物质为_______,
c口通入的物质为______。
②该电池负极的电极反应式为:_______
③工作一段时间后,当12.8 g甲醇完全反应生成CO2时,______________NA个电子转移。
(14分)I(1)Mg逐渐溶解 Al片上有气泡冒出 指针偏转(2分)
Mg-2e-=Mg2+(1分)
(2)Al (1分) 2Al+2NaOH+2H2O=2NaAlO2+3H2↑(2分)
II.NO3-+e-+H+=NO2↑+H2O(2分)
III. ①CH3OH(1分) O2或空气(1分)
②CH3OH-6e-+H2O=CO2+6H+(2分) ③2.4(2分)
解析试题分析:I、(1)若烧杯中溶液为稀硫酸,则Mg与稀硫酸反应,所以Mg作负极,Al作正极,实验现象是Mg逐渐溶解、Al片上有气泡冒出、指针偏转;负极的反应式为Mg-2e-=Mg2+;
(2)若烧杯中溶液为氢氧化钠溶液,则Al与氢氧化钠反应,所以Al作负极,总反应即是Al与NaOH的反应,化学方程式为2Al+2NaOH+2H2O=2NaAlO2+3H2↑;
II、Al与浓硝酸发生钝化,所以Cu与浓硝酸反应,则Cu作负极,正极是NO3-发生还原反应生成二氧化氮,电极反应式为NO3-+e-+H+=NO2↑+H2O;
III、①根据图中氢离子的移动方向判断右侧是正极,左侧是负极,负极通入甲醇,所以b口通入的物质是CH3OH,正极通入的是空气或氧气,所以c口通入的是空气或氧气;
②负极发生氧化反应,根据图中所给信息,甲醇发生氧化反应后生成二氧化碳和氢离子,电极反应式为CH3OH-6e-+H2O=CO2+6H+;
③12.8 g甲醇完全转化为二氧化碳时,转移电子的物质的量是12.8g/32g/mol×6=2.4mol。
考点:考查原电池反应原理,正负极的判断、电极反应式的书写,氧化还原反应的计算


科目:高中化学 来源: 题型:单选题
下列有关电池叙述正确的是
| A.化学电池的反应本质是复分解反应 |
| B.铅蓄电池放电时,是电能转变为化学能的过程 |
| C.锌电锰干池碳棒是负极,锌片是正极 |
| D.锌锰干电池工作一段时间后锌外壳逐渐变薄 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下图所示装置中,观察到电流计指针偏转,M棒变粗,N棒变细,由此判断下表中所列M、N、P物质,其中可以成立的是( )
| | M | N | P |
| A | 锌 | 铜 | 稀硫酸溶液 |
| B | 铜 | 铁 | 稀盐酸溶液 |
| C | 银 | 锌 | 硝酸银溶液 |
| D | 锌 | 铁 | 硝酸铁溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
如图所示是Zn和Cu形成的原电池,某实验兴趣小组做完实验后,在读书卡上的记录如下,则卡片上的描述合理的是 ( )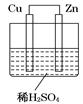
| 实验后的记录: ①Cu为负极,Zn为正极 ②Cu极上有气泡产生,发生还原反应 ③ 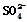 向Cu极移动 向Cu极移动④若有0.5mol电子流经导线,则可产生0.25mol气体 ⑤电子的流向是:Cu―→Zn ⑥正极反应式:Cu—2e-===Cu2+,发生氧化反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
(共10分)如图装置中,已知A、B两池溶液的体积均为200mL: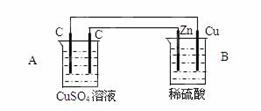
(1)判断装置的名称:A池为 ;
(2)A池中左边石墨棒为 极,
电极反应式为 ;
A池中总反应化学方程式为 ;
(3)若反应开始时,CuSO4溶液的浓度为1.0mol/L。工作一段时间后取出电极,测得导线上通过了0.04mole-。则反应后A池c(Cu2+)为 mol/L(体积变化忽略不计)。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
(10分)如图所示3套实验装置,分别回答下列问题。
(1)装置1中的Cu是 极(填“正”或“负”),该装置发生的总反应的离子方程式为 。
(2)装置2中甲烧杯盛放100 mL 0.2 mol/L的NaCl溶液,乙烧杯盛放100 mL 0.5 mol/L的CuSO4溶液。反应一段时间后,停止通电。向甲烧杯中滴入几滴酚酞,观察到右边石墨电极附近首先变红,左边石墨电极附近无明显现象。
① 电源的M端为 极
② 乙烧杯中电解反应的离子方程式 。
(3)可用阳离子交换膜法电解饱和食盐水制NaOH,其工作原理装置3所示。
①请写出A、B两处物质的名称:A___________________B____________________
②请写出电解食盐水的离子方程式__________________________________________
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
Li-SOCl2电池可用于心脏起搏器。该电池的电极材料分别为锂和碳,电解液是LiAlClx-SOCl2。电池的总反应可表示为:4Li+2SOCl2=4LiCl+S+SO2↑。请回答下列问题:
(1)电池的负极材料为 ,发生的电极反应为 。
(2)电池正极发生的电极反应为 。
(3)SOCl2易挥发,实验室中常用NaOH溶液吸收SOCl2,有Na2SO3和NaCl生成。如果把少量水滴到SOCl2中,实验现象是 ,反应的化学方程式为 。
(4)组装该电池必须在无水、无氧的条件下进行,原因是 。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
(1)甲醇可作为燃料电池的原料。以CH4和H2O为原料,通过下列反应来制备甲醇。
I:CH4 ( g ) + H2O ( g )=CO ( g ) + 3H2 ( g ) △H =+206.0 kJ·mol-1
II:CO ( g ) + 2H2 ( g )=CH3OH ( g ) △H=—129.0 kJ·mol-1
CH4(g)与H2O(g)反应生成CH3OH (g)和H2(g)的热化学方程式为 。
(2)甲醇对水质会造成一定的污染,有一种电化学法可消除这种污染,其原理是:通电后,将Co2+氧化成Co3+,然后以Co3+做氧化剂把水中的甲醇氧化成CO2而净化。实验室用右图装置模拟上述过程:
①写出阳极电极反应式 。
②写出除去甲醇的离子方程式 。
(3)写出以NaHCO3溶液为介质的Al—空气原电池的电极负极反应式,负极: 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com