
用Na2SO3溶液吸收硫酸工业尾气中的二氧化硫,将所得混合液进行电解循环再生,这种新工艺叫再生循环脱硫法。其中阴、阳离子交换膜组合循环再生机理如图所示,则下列说法中错误的是
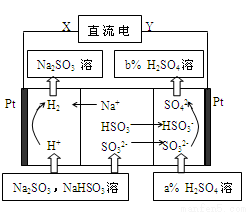
A.X为直流电源的负极,Y为直流电源的正极
B.图中两处硫酸的质量分数b>a
C.该过程中的产品主要为H2SO4和H2
D.阳极区pH增大
 怎样学好牛津英语系列答案
怎样学好牛津英语系列答案 导学教程高中新课标系列答案
导学教程高中新课标系列答案科目:高中化学 来源:2014-2015学年河北省高三12月月考化学试卷(解析版) 题型:选择题
短周期主族元素W、X、Y、Z的原子序数依次增大,W、X原子的最外层电子数之比为4:3,Z原子比X原子的核外电子数多4.下列说法正确的是
A.W、Y、Z的非金属性大小顺序一定是Z>Y>W
B.W、X、Y、Z的原子半径大小顺序可能是W>X>Y>Z
C.Y、Z形成的分子空间构型可能是正四面体
D.XZ3中含有离子键
查看答案和解析>>
科目:高中化学 来源:2014-2015学年广东省广州市高三上学期期中理综化学试卷(解析版) 题型:选择题
E~N等元素在周期表中的相对位置如下表。E与K的原子序数相差4,K的一种单质是空气中含量最多的物质,H与N属同周期元素,下列判断不正确的是
E | K | |||
F | G | M | L | |
H | N |
A.K的氢化物水溶液显碱性
B.F的单质与氧气反应只生成一种氧化物
C.H与N的原子核外电子数相差14
D.最高价氧化物的水化物酸性:K > L > M
查看答案和解析>>
科目:高中化学 来源:2014-2015学年甘肃省高三11月月考化学试卷(解析版) 题型:选择题
化学是以实验为基础的学科,下列有关实验的描述正确的是
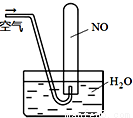
A.向两支分别装有碳酸钠和碳酸氢钠固体的试管中各加几滴水,前者温度降低,后者温度升高
B.向100mL容量瓶中加入4.0gNaOH固体,然后加水到刻度线,配制1.0mol/L的NaOH溶液
C.向酸性重铬酸钾溶液中加NaOH,溶液颜色由橙色慢慢变为黄色
D.如图所示,随着空气的通入,试管内液面会慢慢上升至充满整支试管,而后液面又下降。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年浙江省高二上学期期中化学试卷(解析版) 题型:填空题
已知草酸(H2C2O4)是一种二元弱酸,主要用作还原剂和漂白剂。
(1)草酸的电离方程式为 。
(2)将草酸溶液与酸性高锰酸钾溶液混合发生的反应为:
MnO4-+ H2C2O4+ → Mn2+ + CO2↑+ H2O
某合作小组同学在烧杯中进行上述反应时,发现刚开始一段时间,反应速率较慢,溶液褪色不明显,但不久后突然褪色,反应速率明显加快。
①配平上述离子方程式
②该实验不久后溶液突然褪色的原因最有可能是 。
A.体系压强增大 B.反应物接触面积增大
C.生成物对反应有催化作用 D.反应物浓度增大
(3)为研究该化学反应速率的影响因素,某同学进行了以下实验:
组别 | 温度/℃ | V(H2C2O4) /mL | V(KMnO4) /mL | V(H2O) /mL | KMnO4溶液 褪色时间/s |
1 | 30 | 10 | 10 | 20 | 40 |
2 | 30 | 20 | 20 | 0 | t |
3 | 30 |
|
| 15 |
①对比实验1和3要研究改变反应物浓度对化学反应速率的影响,请完成表格中横线。
②实验2中溶液褪色时间t 为
A.>40 B.=40 C.<40 D.无法判断
查看答案和解析>>
科目:高中化学 来源:2014-2015学年浙江省高二上学期期中化学试卷(解析版) 题型:选择题
分析下图所示的四个原电池装置,其中结论正确的是
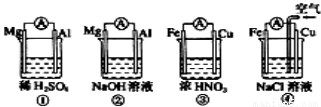
A.①②中Mg作为负极,③④中Fe作为负极
B.②中Mg作为正极,电极反应式为6H2O + 6e- ═ 6OH- + 3H2↑
C.③中Fe作为负极,电极反应为Fe-2e - ═Fe2+
D.④中Cu作为正极,电极反应式为2H+ + 2e - ═H2↑
查看答案和解析>>
科目:高中化学 来源:2014-2015学年浙江省高二上学期期中化学试卷(解析版) 题型:选择题
反应A(g)+3B(g) 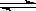 2C(g)的能量变化如图所示,
2C(g)的能量变化如图所示,
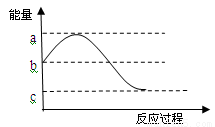
结合图像分析下列说法,其中正确的是
A.若升高温度,则平衡常数增大
B.该反应的焓变为b-a
C.达到平衡后,增大压强,平衡逆移
D.催化剂不影响反应的焓变,影响反应的活化能
查看答案和解析>>
科目:高中化学 来源:2014-2015学年浙江省高一上学期期中化学试卷(解析版) 题型:选择题
将等物质的量的金属Na、Mg、Al分别与100mL 2mol/L的盐酸反应,生成气体的体积均为VL(标准状况下),已知:2Na+2H2O=2NaOH+H2,下列说法错误的是
A.反应中,三种金属中有两种金属过量
B.参加反应的金属Na 、 Mg、 Al的物质的量之比为6:3:2
C.镁的物质的量为0.1mol
D.V=2.24
查看答案和解析>>
科目:高中化学 来源:2014-2015学年浙江省高二上学期期中化学试卷(解析版) 题型:选择题
在25℃时,密闭容器中X、Y、Z三种气体的初始浓度和平衡浓度如下表。下列说法错误的是
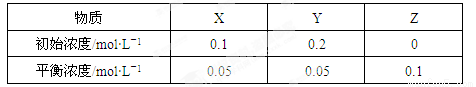
A.反应达到平衡时,X的转化率为50%
B.改变温度可以改变此反应的平衡常数
C.反应可表示为X+3Y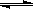 2Z,其平衡常数为1600
2Z,其平衡常数为1600
D.增大压强使平衡向生成Z的方向移动,平衡常数增大
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com