
| A. | 硝基苯 | B. | 环己烷 | C. | 苯酚 | D. | 溴苯 |
科目:高中化学 来源: 题型:选择题
 如图所示在密封容器中,一部分装入2.3g金属钠,另一部分装入HgO,同时加热两部分,若加热后容器内的空气成分未变,那么装入容器中的HgO是( )
如图所示在密封容器中,一部分装入2.3g金属钠,另一部分装入HgO,同时加热两部分,若加热后容器内的空气成分未变,那么装入容器中的HgO是( )| A. | 21.6 g | B. | 20.0g | C. | 1.6 g | D. | 10.8 g |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 欲使0.1mol/L的NaHCO3溶液中c(H+)、c(CO32-)、c(HCO3-)都减少,其方法是加入氢氧化钠固体 | |
| B. | 常温下,0.4 mol/LHB溶液和0.2 mol/LNaOH溶液等体积混合后溶液的pH=3,则混合溶液中离子浓度的大小顺序为: c(B-)>c(H+)>c(Na+)>c(OH-) | |
| C. | 某温度下纯水的c(H+)=1.0×10-6mol/L,在此温度下,将pH=8的Ba(OH)2溶液与pH=5的稀盐酸混合(溶液体积变化忽略不计).欲使混合溶液的pH=7,则氢氧化钡溶液与盐酸的体积比为2:9 | |
| D. | pH相等的下列溶液:a.CH3COOK、b.NaHCO3、c.Na2CO3、d.NaOH,其物质的量浓度由小到大顺序为:d<c<a<b |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 增加6.5 g | B. | 减少6.5 g | C. | 减少5.6 g | D. | 增加6.4 g |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Cu 2+ | B. | Fe 3+ | C. | Fe 2+ | D. | H + |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 欲用图装置进行实验,用以比较苯酚、盐酸、碳酸的酸性,图中标示的A、B、C三种药品(或试剂)依次是( )
欲用图装置进行实验,用以比较苯酚、盐酸、碳酸的酸性,图中标示的A、B、C三种药品(或试剂)依次是( )| A. | 盐酸、碳酸、苯酚 | B. | 盐酸、碳酸钠、苯酚钠 | ||
| C. | 盐酸、碳酸钠、苯酚 | D. | 氯化钠、碳酸钠、苯酚钠 |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
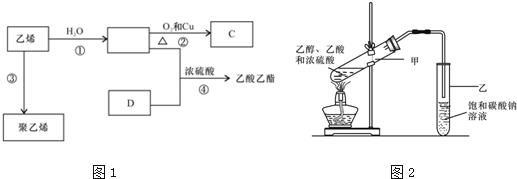
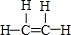 .
. CH3COOCH2CH3+H2O,反应类型:酯化反应或取代反应.
CH3COOCH2CH3+H2O,反应类型:酯化反应或取代反应.查看答案和解析>>
科目:高中化学 来源: 题型:实验题
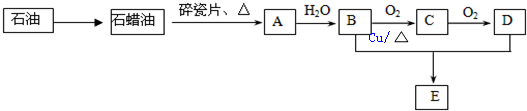
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 配位体是Cl-和NH3,配位数是8 | |
| B. | 中心离子是Co2+,配离子是Cl- | |
| C. | 内界和外界中的Cl的数目比是1:2 | |
| D. | 加入足量AgNO3溶液,所有Cl-一定被完全沉淀 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com