
����Ŀ��2015������������������Ű�ҹ��ж�����������������β������ɿ�����Ⱦ����Ҫԭ������β����������Ҫԭ��Ϊ��
2NO��g��+2CO��g�� ![]() 2CO2��g��+N2��g�������ܱ������з����÷�Ӧʱ��c��CO2�����¶ȣ�T���������ı������S����ʱ�䣨t���ı仯������ͼ1��ʾ��
2CO2��g��+N2��g�������ܱ������з����÷�Ӧʱ��c��CO2�����¶ȣ�T���������ı������S����ʱ�䣨t���ı仯������ͼ1��ʾ��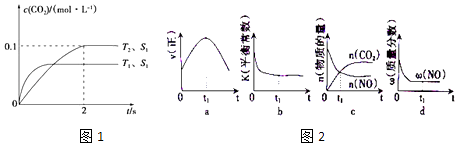
��1���÷�Ӧ�ġ�H0��ѡ�����������������
��2����T2�¶��£�0��2s�ڵ�ƽ����Ӧ����v��N2��= ��
��3�����������������һ��ʱ����������漴�����ѧ��Ӧ���ʣ��������ı����S1��S2 �� ��ͼ1�л���c��CO2����T1��S2�����´ﵽƽ������еı仯���ߣ�
��4�����÷�Ӧ�ھ��ȡ����ݵ��ܱ���ϵ�н��У�ͼ2��ʾ��ͼ��ȷ����˵����Ӧ��t1ʱ�̴��ڻ�ѧƽ��״̬����������ţ���
���𰸡�
��1����
��2��0.025mol/��L?s��
��3��
��4��bd
���������⣺��1�����ݡ��ȹ���ƽ��ֵ��֪��T1��T2�������¶ȶ�����̼�������ͣ�˵��ƽ�������ƶ��������¶�ƽ�������ȷ����ƶ�����������Ӧ�Ƿ��ȷ�Ӧ����H��0��
�ʴ�Ϊ������
��2����T2�¶��£�0��2s�ڣ���c��CO2��=��0.1��0��mol/L=0.1mol/L�����ݷ���ʽ֪����c��N2��= ![]() ��c��CO2����v��N2��=
��c��CO2����v��N2��= ![]() =
= ![]() =0.025mol/��Ls����
=0.025mol/��Ls����
�ʴ�Ϊ��0.025mol/��Ls����
��3�������Ӵ����Խ��Ӧ����Խ�죬�����̷�Ӧ�ﵽƽ���ʱ�䣬��������̼ת���ʲ��䣬������ͼ��Ϊ  ���ʴ�Ϊ��
���ʴ�Ϊ��  ��
��
��4��a������ƽ���������������ȣ����ٱ仯��t1ʱ��V�����֮���淴Ӧ�������ʷ����仯��δ����ƽ�⣬��a����
b���÷�Ӧ����ӦΪ���ȷ�Ӧ���淴Ӧ�����¶����ߣ���ѧƽ�ⳣ����С������ƽ����¶�Ϊ��ֵ������ߣ�ƽ�ⳣ�����䣬Ϊ��С��ͼ����ʵ�ʷ��ϣ���b��ȷ��
c��t1ʱ�̺������̼��NO�����ʵ��������仯��t1ʱ��δ����ƽ��״̬����c����
d��NO����������Ϊ��ֵ��t1ʱ�̴���ƽ��״̬����d��ȷ��
�ʴ�Ϊ��bd��
��1�������¶ȶԻ�ѧƽ���Ӱ������ʱ䣻
��2�����ݻ�ѧ��Ӧ���ʵĶ������2s�ڵķ�Ӧ���ʣ�
��3������ֻ�ܸı䷴Ӧ���ʣ������ܸı仯ѧƽ�⣻
��4�����ݿ��淴Ӧ�ﵽƽ��״̬����ֵİٷֺ������䡢���淴Ӧ������Ƚ����жϼ���.



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��
�л���F(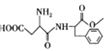 )��һ��Ӧ�ù㷺��ʳ�õ���ζ�����׳Ƶ����ǣ�����һ�ֺϳ�·����ͼ��ʾ��
)��һ��Ӧ�ù㷺��ʳ�õ���ζ�����׳Ƶ����ǣ�����һ�ֺϳ�·����ͼ��ʾ��
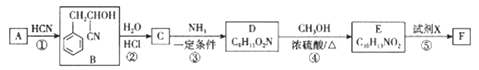
��֪����.A�ܷ���������Ӧ
��. ![]()
��ش��������⣺
(1)D�й����ŵ�����Ϊ_______________��F�ķ���ʽΪ___________________��
(2)A������Ϊ__________����Ӧ�� �ķ�Ӧ����Ϊ________________��
(3)��Ӧ�ܵĻ�ѧ����ʽΪ_______________________��
(4)��Ӧ���е���һ����������ˮ����X�Ľṹ��ʽΪ__________________��
(5)D�ж��ַ�����ͬ���칹�壬���з���������������_________��(�����������칹)��
����D������ͬ�Ĺ����� �ڱ�������2 ��ȡ����
���к˴Ź�������Ϊ6����ҷ������Ϊ2��2��2��2��2��1�Ľṹ��ʽΪ____________(д��һ�ּ���)��
(6)��ϩ������Ҫ���л��ϳ�ԭ�ϼ��ϳ���֬���壬��д����CH3CHOΪԭ�Ϻϳɱ�ϩ��ĺϳ�·��________________________ (�����Լ���ѡ)��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ں����ܱ������У����淴ӦC(s)+CO2(g)![]() 2CO(g)���ﵽƽ��״̬�ı�־��
2CO(g)���ﵽƽ��״̬�ı�־��
A. ��λʱ��������nmolCO2��ͬʱ����2nmolCO
B. ��λʱ��������nmolCO2��ͬʱ����nmolC
C. ���������ܶȲ��ٸı��״̬
D. ��������ѹǿ���ٸı��״̬
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����ڷ�ӦaA+bB=dD+eE������֪40g A��ǡ����21g B��ȫ��Ӧ����28g D����B��E��Ħ��������Ϊ
A.7a:10dB.10a:7dC.10b:7eD.7e:11b
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���±���Ԫ�����ڱ���һ���֣��ش������й����⣺

(1)д������Ԫ������:��_________��___________��
(2)����ЩԪ���У���������ǿ��Ԫ����______(��Ԫ�ط��ű�ʾ)��Ԫ�آ���Ԫ�آ���ȣ��ǽ����Խ�ǿ����___________(��Ԫ�ط��ű�ʾ)�����б�������֤����һ��ʵ����______________��
a.�����¢�ĵ��ʺ͢�ĵ���״̬��ͬ
b. ����⻯��Ȣ���⻯���ȶ�
c.һ�������¢�͢�ĵ��ʶ���������������Һ��Ӧ
(3)�ߵ�����������Ӧˮ������������������Ӧˮ���ﷴӦ�����ӷ���ʽΪ��______��
(4)�ڵ���̬�⻯����HC1�ڿ����������а������ɣ�д�����̶�Ӧ���ʵĵ���ʽ_________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������ֽ�������A��B��C������A����ɫ��ӦΪ��ɫ��B��C�dz������������ֽ�������A��B��C��������ס��ҡ���������D��E��F��G��H֮�䷢������ת����ϵ��ͼ����Щ��Ӧ�IJ���ͷ�Ӧ������û��ȫ���������
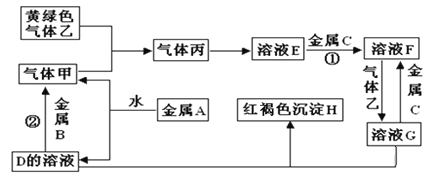
�����������Ϣ�ش��������⣺
��1��д���������ʵĻ�ѧʽ��H_______________����______________��
��2��д�����з�Ӧ�����ӷ���ʽ
��Ӧ��_________________________________________________________________
��Ӧ��_________________________________________________________________
��3��������ҺG�е������ӣ���ȡ������ҺG���Թ��У��μ�KSCN��Һ��������____________��������ҺG�е������ӣ�����ȡ������ҺG���Թ��У��μ�__________���ѧʽ����Һ�������Dz�����ɫ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����������18��A��M����Ԫ�أ���֪A2����M+�ĵ�����֮��Ϊ8��������˵����ȷ���ǣ� ��
A.A��Mԭ�ӵ�����������֮�һ��Ϊ5
B.A��Mԭ�ӵ�����������֮��һ��Ϊ7
C.A��Mԭ�ӵĵ�����֮��һ��Ϊ11
D.A��M��ԭ������֮�һ��Ϊ5
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��A��B��Ϊ������Ԫ���е�һ�֣���֪A��ԭ������Ϊn��A2�����ӱ�B2��������8�����ӣ���B��ԭ������Ϊ
A. n��4B. n��6C. n��8D. n��10
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����и���ʵ�����������,��ȷ����
A. Ϊ�˼ӿ�п��ϡ���ᷴӦ������,������ϡ�����м�����������ͭ![]()
B. �����к͵ζ�ʵ��ʱ��ϴ�ζ��ܺ�ֱ��װҺ�ζ�
C. Ϊ�˼ӿ�����ٶ�,�ò���������������е�Һ��
D. Ϊ��ʹ���Ƶ��Ȼ�����Һ���ֳ���,�����������Ƭ
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com