
【题目】下列为元素周期表的一部分,表中阿拉伯数字(1、2……)是元素周期表中行或列的序号。请参照元素A~I在表中的位置,回答下列问题。
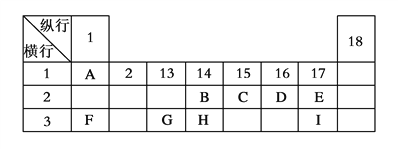
(1)B、C、H三元素中非金属性最强的是________(写出元素名称),写出AF化合物的电子式__________,若AF与水反应产生2.24L气体(标准状况下),则转移电子数目为_______。
(2)表中某元素能形成两性氧化物,写出该氧化物溶于氢氧化钠溶液的离子方程式: ____________。
(3)表中某元素的单质在常温下为气态,该元素能与A~I中的一种元素构成原子个数比为1:1和1:2的两种共价化合物X和Y,该元素还能与A~I中的另一种元素构成原子个数比为1:1和1:2的两种离子化合物Z和M。写出Z与Y反应的化学方程式:_____________________________________。
【答案】 氮 Na+[:H]- 6.02×1022 Al2O3+2OH-===2AlO2—+H2O 2Na2O2+2H2O===4NaOH+O2↑
【解析】根据元素A~I在表中的位置可判断它们分别是H、C、N、O、F、Na、Al、Si、Cl。则
(1)同周期自左向右非金属性逐渐增强,同主族从上到下非金属性逐渐减弱,则B、C、H三元素中非金属性最强的是氮,AF是NaH,含有离子键的离子化合物,电子式为![]() ,NaH与水反应生成氢氧化钠和氢气:NaH+H2O=NaOH+H2↑,反应时水中氢元素化合价从+1价降低到0价,NaH中氢元素化合价从-1价升高到0价,即产生1分子氢气,转移1个电子,所以若与水反应产生2.24L气体(标准状况下)即0.1mol氢气时转移电子数目为0.1NA。(2)表中某元素能形成两性氧化物,该氧化物是氧化铝,溶于氢氧化钠溶液的离子方程式为Al2O3+2OH-=2AlO2-+H2O。(3)表中某元素的单质在常温下为气态,该元素能与A~I中的一种元素构成原子个数比为1:1和1:2的两种共价化合物X和Y,该元素还能与A~I中的另一种元素构成原子个数比为1:1和1:2的两种离子化合物Z和M,因此该元素是O,X是双氧水,Y是水,Z是过氧化钠,M是氧化钠,所以Z与Y反应的化学方程式为2Na2O2+2H2O=4NaOH+O2↑。
,NaH与水反应生成氢氧化钠和氢气:NaH+H2O=NaOH+H2↑,反应时水中氢元素化合价从+1价降低到0价,NaH中氢元素化合价从-1价升高到0价,即产生1分子氢气,转移1个电子,所以若与水反应产生2.24L气体(标准状况下)即0.1mol氢气时转移电子数目为0.1NA。(2)表中某元素能形成两性氧化物,该氧化物是氧化铝,溶于氢氧化钠溶液的离子方程式为Al2O3+2OH-=2AlO2-+H2O。(3)表中某元素的单质在常温下为气态,该元素能与A~I中的一种元素构成原子个数比为1:1和1:2的两种共价化合物X和Y,该元素还能与A~I中的另一种元素构成原子个数比为1:1和1:2的两种离子化合物Z和M,因此该元素是O,X是双氧水,Y是水,Z是过氧化钠,M是氧化钠,所以Z与Y反应的化学方程式为2Na2O2+2H2O=4NaOH+O2↑。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】两种气态烃以一定比例混合,在105℃时1L该混合烃与9L氧气混合,充分燃烧后恢复到原状态,所得气体体积仍是10L.下列各组混合烃中不符合此条件的是( )
A.CH4 C2H4
B.CH4 C3H6
C.C2H4 C3H4
D.C2H2 C3H6
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】《本草经集注》中记载有关于区别硝石(KNO3)和朴硝(Na2SO4) 的方法:“强烧之,紫青烟起,…,云是真硝石也。”文中区别的方法是利用了下列中的( )
A. 焰色反应 B. 萃取 C. 丁达尔效应 D. 蒸馏
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在密闭容器中进行反应:X(g)+3Y(g)2Z(g),有关下列图像说法正确的是( )

A. 依据图甲可判断正反应为吸热反应
B. 在图乙中,虚线可表示压强增大
C. 若正反应的△H<0,图丙可表示升高温度使平衡向逆反应方向移动
D. 由图丁中气体平均相对分子质量随温度的变化情况,可推知正反应的△H>0
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组物质中,物质之间通过一步反应就能实现如图所示转化的是( )
a | b | c | |
A | N2 | NO | NO2 |
B | S | SO2 | SO3 |
C | Si | SiO2 | H2SiO3 |
D | Fe | FeCl2 | FeCl3 |

A.A
B.B
C.C
D.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某学生以 0.1000 mol·L-1 的 NaOH 溶液滴定 20.00mL 未知浓度的稀盐酸,滴定操作可分解为如下几步(所用的仪器已检漏且刚用蒸馏水洗净):
A.用酸式滴定管向锥形瓶里注入 20.00mL 待测稀盐酸溶液,并加入 2~3 滴酚酞;
B.用标准 NaOH 溶液润洗碱式滴定管 2~3 次;
C.把盛有标准溶液的碱式滴定管固定好,调节滴定管尖嘴使之充满溶液,使管内无气泡;
D.将标准 NaOH 溶液注入碱式滴定管至刻度 0 以上 2~3cm ;
E.调节液面至 0 或 0 刻度以下,记下读数;

F.把锥形瓶放在滴定管的下面,用标准 NaOH 溶液滴定至终点并记下滴定管液面的刻度。
(1)正确操作步骤的顺序是(用序号字母填写)B_______F ;
(2)滴定达到终点的现象_________。
(3)用标准 NaOH 溶液滴定时,应将标准 NaOH 溶液注入_____(右图“甲”或“乙”)中。
(4)滴定时边滴边摇动锥形瓶,眼睛应观察_______。
(5)据下列数据计算,待测盐酸溶液的浓度为 ____mol·L-1 (计算结果保留小数点后四位)
实验编号 | 待测盐酸体积(m L) | 滴定前 NaOH 溶液的体积读数(mL) | 滴定后 NaOH 溶液 的体积读数(mL) |
1 | 20.00 | 1.20 | 23.22 |
2 | 20.00 | 2.21 | 24.21 |
3 | 20.00 | 1.50 | 23.48 |
(6)下列操作会导致测定结果偏低的是____。
A.碱式滴定管未用标准 NaOH 溶液润洗就装标准液滴定
B.读取标准液读数时,滴前仰视,滴定到终点后俯视
C.滴定前碱式滴定管尖嘴处有气泡未排除,滴定后气泡消失
D.酸式滴定管没有用待测盐酸润洗,直接装入待测盐酸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ga、As、Al、C的相关化合物在化工和医学领域有着广泛的应用。回答下列问题:
(1)写出基态Ga原子的核外电子排布式:_________,有_____个未成对电子。
(2)合金砷化镓在现代工业中被广泛应用,Ga、As电负性由大到小排序为______________。
(3)1个丙二烯分子中σ键总数为___个,C原子的杂化方式为______。分子中的大π键可以用符号пmn表示,其中m代表参与形成大π键的原子数,n代表参与形成大π键的电子数(如苯分子中的大π键可表示为п66),则丙二烯中的大π键应表示为____________。
(4)氮化镓是第三代半导体材料,其晶体结构和单晶硅相似,晶胞结构如图所示:

①原子坐标参数是表示晶胞内部各原子的相对位置,其中原子坐标参数A为(0, 0, 0);B为(1/2,1/2,0);C为(1,0,1)。则D原子的坐标参数为_________________。
②已知氮化镓晶胞的边长为a nm,其密度为d g/cm3,则阿伏加德罗常数NA =____(用a、d表示)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A.所有不锈钢都只含有金属元素
B.我国流通的硬币材质是金属单质
C.广东正在打捞的明代沉船上存在大量铝制餐具
D.镁合金的硬度和强度均高于纯镁
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com