
【题目】利用待测溶液和指定的试剂设计实验,不能达到实验目的的是
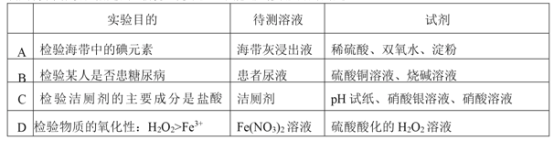
A.AB.BC.CD.D
【答案】D
【解析】
A.向海带灰浸出液中加入稀硫酸酸化,再加入双氧水,溶液由无色变为黄色,可初步判断海带中含有碘元素,再加入淀粉,溶液变蓝色,可确定海带中含有碘元素,故A正确;
B.先用硫酸铜溶液与过量烧碱溶液反应,得到新制的氢氧化铜悬浊液。将其与患者尿液混合,加热,若产生砖红色沉淀则说明患糖尿病,反之则不是,故B正确;
C.用pH试纸测得洁厕剂显强酸性,取少量洁厕剂滴入硝酸钡溶液中,无明显现象,再加入硝酸银溶液,若有白色沉淀生成则说明洁厕剂中含有氯离子,综上可检验洁厕剂的主要成分是盐酸,故C正确;
D.硝酸的氧化性强于过氧化氢,用硫酸酸化的过氧化氢溶液和硝酸亚铁反应时,硝酸作为氧化剂,故不能说明过氧化氢的氧化性强于铁离子,故D错误;
故答案选:D。


 举一反三单元同步过关卷系列答案
举一反三单元同步过关卷系列答案科目:高中化学 来源: 题型:
【题目】以NA表示阿伏加德罗常数的值,下列说法不正确的是( )
A.18g冰(图1)中含O—H键数目为2NA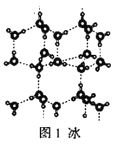
B.28g晶体硅(图2)中含有Si—Si键数目为2NA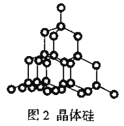
C.44g干冰(图3)中含共用电子对2NA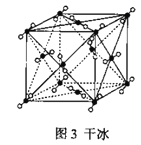
D.石墨烯(图4)是碳原子单层片状新材料,12g石墨烯中含C—C键数目为1.5NA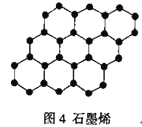
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某项目学习小组在实验失室制取漂白粉,并探究氯气与石灰乳反应的条件和产物。已知:
①二氧化锰与浓盐酸反应可制备氯气,同时生成MnCl2。
②氯气和碱的反应为放热反应.温度较高时,氯气和碱还能发生如下反应:3Cl2+6OH-![]() 5Cl-+ClO3-+3H2O。
5Cl-+ClO3-+3H2O。
该项目小组设计了下列实验装置,进行实验。
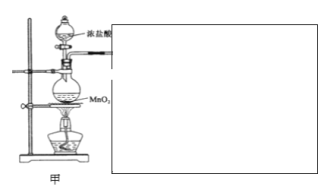
请回答下列问题:
(1)甲装置用于制备氯气。
①请你将装置在图中方框中补充完整___(并标明所加药品)
②该项目小组用100mL12mol/L盐酸与8.7gMnO2制备氯气,并将所得氯气与过量的石灰乳反应,则理论上最多可制得Ca(ClO)2的物质的量为___。
(2)小组成员发现,产物中Ca(ClO)2的质量明显小于理论值。他们讨论后认为,原因有二:
①部分氯气未与石灰乳反应而逸出;
②___。
(3)为了探究反应条件对产物的影响,他们另取一定量的石灰乳,缓慢匀速地通入足量氯气,得出了ClO-、ClO3-两种离子的物质的量(n)与反应时间(t)的关系曲线,粗略表示为如图(不考虑氯气和水的反应)。
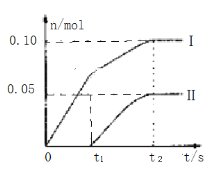
①图中曲线I表示___离子的物质的量随反应时间变化的关系。
②所取石灰乳中含有Ca(OH)2的物质的量为___。
③另取一份与②等物质的量的石灰乳,以较大的速率通入足量氯气,反应后测得产物中Cl-的物质的量为0.37mol,则产物中![]() =___(填比值)。
=___(填比值)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用酸性氢氧燃料电池电解苦卤水(含Cl-、Br-、Na+、Mg2+)的装置如下图所示(a、b为石墨电极).下列说法中,正确的是
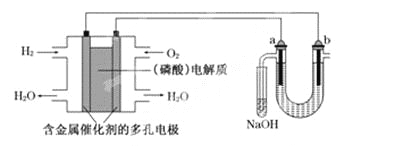
A. 电池工作时,正极反应式为: O2+2H2O+4e-===4OH-
B. 电解时,a电极周围首先放电的是Br-而不是Cl-,说明当其他条件相同时前者的还原性强于后者
C. 电解时,电子流动路径是:负极→外电路→阴极→溶液→阳极→正极
D. 忽略能量损耗,当电池中消耗0.02 g H2时,b极周围会产生0.04 g H2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】精炼铜工业中阳极泥的综合利用具有重要意义。一种从铜阳极泥(主要含有铜、银、金、少量的镍)中分离提取多种金属元素的工艺流程如下:

已知:ⅰ分金液中含金离子主要成分为[AuCl4]-;分金渣的主要成分为AgCl;
ⅱ分银液中含银离子主要成分为[Ag(SO3)2]3-,且存在[Ag(SO3)2]3—![]() Ag++2SO
Ag++2SO![]()
ⅲ“分铜”时各元素的浸出率如下表所示。

(1)由表中数据可知,Ni的金属性比Cu______。分铜渣中银元素的存在形式为(用化学用语表示)______。“分铜”时,如果反应温度过高,会有明显的放出气体现象,原因是_______。
(2)“分金”时,单质金发生反应的离子方程式为________。
(3)Na2SO3溶液中含硫微粒物质的量分数与pH的关系如图所示。

“沉银”时,需加入硫酸调节溶液的pH=4,分析能够析出AgCl的原因为_______。调节溶液的pH不能过低,理由为______(用离子方程式表示)。
(4)已知Ksp[Ag2SO4]=1.4×10-5,沉银时为了保证不析出Ag2SO4,应如何控制溶液中SO42—浓度(假定溶液中Ag+浓度为0.1mol/L)。________。
(5)工业上,用镍为阳极,电解0.1 mol/L NiCl2溶液与一定量NH4Cl组成的混合溶液,可得高纯度的球形超细镍粉。当其他条件一定时,NH4Cl的浓度对阴极电流效率及镍的成粉率的影响如图所示:

为获得髙纯度的球形超细镍粉,NH4Cl溶液的浓度最好控制为_______g/L,当NH4Cl溶液的浓度大于15g/L时,阴极有无色无味气体生成,导致阴极电流效率降低,该气体为_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是Zn和Cu组成的原电池示意图,某小组做完该实验后,在读书卡片上作了如下记录,其中合理的是 ( )
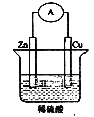
实验记录:①导线中电流方向:锌→铜②铜极上有气泡产生③锌片变薄
实验结论:④Zn为正极,Cu为负极⑤铜比锌活泼⑥H+向铜片移动
A.①②③B.④⑤⑥C.③④⑤D.②③⑥
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】环丁基甲酸(![]() )是有机合成中一种重要的中间体。实验室以链状分子A为原料合成环丁基甲酸的路线如下:
)是有机合成中一种重要的中间体。实验室以链状分子A为原料合成环丁基甲酸的路线如下:
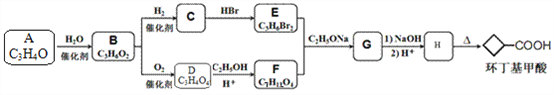
已知: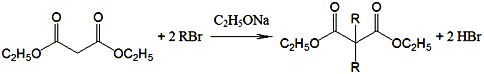
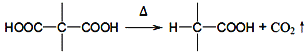
请回答下列问题:
(1)化合物A的化学名称是______,由A生成B的反应类型是_______。
(2)化合物B中所含官能团的名称为___________。
(3)化合物C和D反应所形成高聚物的结构简式是___________。
(4)写出E+F→G的化学方程式: ___________。
(5)X是环丁基甲酸的同分异构体,能与饱和碳酸氢钠溶液反应放出气体,且能使溴水褪色,X共有______种;其中核磁共振氢谱为三组峰,峰面积比为6:1:1的结构简式为___________。
(6)写出用1,3一丁二烯和化合物F为原料制备环戊基甲酸的合成路线___________。(其他试剂任选)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室利用废弃旧电池的铜帽(主要成分为Zn和Cu)回收Cu并制备ZnO的部分实验过程如图所示:

下列叙述错误的是( )
A. “溶解”操作中可用酸性条件下不断鼓入O2代替H2O2
B. 铜帽溶解后,将溶液加热至沸腾以除去溶液中过量的H2O2
C. 与加入锌粉反应的离子为Cu2+、H+
D. “过滤”操作后,将滤液蒸干、高温灼烧即可制取纯净的ZnO
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,在新制氯水中滴加NaOH溶液,溶液中水电离出的的c(H+)与NaOH溶液的体积之间的关系如图所示,下列推断正确的是( )
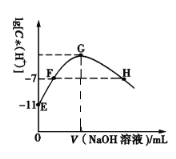
A. 可用pH试纸测定E点对应溶液,其pH=3
B. G点对应溶液中:c(Na+)>c(Cl-)>c(ClO-)>c(OH-)>c(H+)
C. H、 F点对应溶液中都存在:c(Na+)=c(Cl-)+c(ClO-)
D. 常温下加水稀释H点对应溶液,溶液的pH增大
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com