
近年来发现铊(Tl)是高温超导材料的成分之一,已知铊与铝是同族元素,关于铊的下列性质判断中,可能错误的是()
A. 是银白色、质软的金属 B. 能形成+3价的化合物
C. Tl(OH)3是两性氢氧化物 D. 能与硝酸反应生成硝酸盐
考点: 元素周期律和元素周期表的综合应用.
专题: 元素周期律与元素周期表专题.
分析: 铊与铝是同族元素,则具有金属的共性,化合物中元素的化合价为+3价,且金属性Tl>Al,以此来解答.
解答: 解:A、铊与铝是同族元素,属于金属元素,则是银白色、质软的金属,故A正确;
B、Al的最外层电子数为3,则Tl的最外层电子数为3,化合物中元素的化合价为+3价,故B正确;
C、同主族从上到下金属性在增强,Al(OH)3是两性氢氧化物,但Tl(OH)3是碱性氢氧化物,故C错误;
D、Tl较活泼,则该金属能与硝酸反应生成硝酸盐,故D正确;
故选C.
点评: 本题考查同主族元素的性质,明确元素周期律是解答本题的关键,注意性质的相似性和递变性来解答即可,难度不大.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
区别下列各组物质的方法错误的是( )
A.甲烷和乙烯:分别通入酸性KMnO4溶液
B.乙醇和乙酸:分别滴加NaOH溶液
C.苯和四氯化碳:分别与水混合、振荡、静置
D.区别甲醇和乙醛:用新制的Cu(OH)2悬浊液加热来鉴别
查看答案和解析>>
科目:高中化学 来源: 题型:
普通玻璃中,Na2SiO3、CaSiO3、SiO2的物质的量之比是Na2SiO3∶CaSiO3∶SiO2=1∶1∶4。
(1)若以aNa2O·bCaO·mSiO2形式表示此玻璃的组成,则a∶b∶m=____________。
(2)若要制备1 000 kg上述玻璃,需要原料各多少千克?共可产生标准状况下的CO2气体多少升?
查看答案和解析>>
科目:高中化学 来源: 题型:
2011年为“国际化学年”,其主题是“化学 我们的生活 我们的未来”.下列对化学学科的认识错误的是
()
A. 我们应该珍爱生命,化学是研究、接触有毒有害物质,我们应该远离化学
B. 化学学科主要是在微观层面上研究物质的一门以实验为基础的自然科学
C. 化学学科肩负着开发和研究新材料、新能源等领域的重要责任
D. 化学学科的发展对人类物质文明的进步有着重要作用
查看答案和解析>>
科目:高中化学 来源: 题型:
关于化学键的下列表述中,正确的是()
A. 共价化合物可能含有离子键
B. 离子化合物中可能含有共价键
C. 离子化合物中只含有离子键
D. 硫酸中含有离子键
查看答案和解析>>
科目:高中化学 来源: 题型:
工业制硫酸中的一步重要反应是SO2在400~600℃下的催化氧化:2SO2+O2⇌2SO3,这是一个正反应放热的可逆反应.若反应在密闭容器中进行,下述有关说法中错误的是()
A. 达到平衡时,SO2的浓度与SO3的浓度相等
B. 使用催化剂是为了加快反应速率,提高生产效率
C. 为了提高SO2的转化率,应适当提高O2的浓度
D. 在上述条件下,SO2不可能100%转化为SO3
查看答案和解析>>
科目:高中化学 来源: 题型:
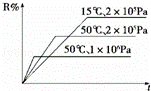
密闭容器中进行下列反应:M(g)+N(g)⇌R(g)+2L,如图所示R%是R的体积分数,t是时间,下列关于该反应的分析正确的是( )
|
| A. | 正反应吸热,L为气体 |
|
| B. | 正反应吸热,L为固体或纯液体 |
|
| C. | 正反应放热,L为气体 |
|
| D. | 正反应放热,L为固体或纯液体 |
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法不正确的是()
①将CO2通入BaCl2溶液中,始终无白色沉淀生成
②将盐酸、KSCN溶液和Fe(NO3)2溶液三种溶液混合,混合溶液显红色
③向某溶液中滴入盐酸酸化的BaCl2溶液产生白色沉淀,证明溶液中一定含有SO42﹣
④将两小块质量相等的金属钠,一块直接投入水中,另一块用铝箔包住,在铝箔上刺些小孔,然后投入水中,两者放出的氢气质量相等
⑤将SO2通入溴水中,证明SO2具有漂白性
⑥在滴有酚酞的Na2CO3溶液中,加入BaC12溶液后红色逐渐褪去,证明Na2CO3溶液中存在水解平衡
⑦因为SiO2能和CaCO3反应生成CO2,所以H2SiO3酸性强于H2CO3.
A. ②④⑥⑦ B. ①③④⑤ C. ③④⑤⑦ D. ②③④⑤⑦
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com