
����Ŀ����300mL2.0 mol/L�����м��뼸С�����ʯ����������������ʱ��ı仯��������ͼ��ʾ(��������ڱ�״���²ⶨ)�Իش��������⣺

(1)���Է�Ӧ�����ĵ�HCl��ʾ��Ӧ���ʣ���OE�εķ�Ӧ����Ϊv1��EF�εķ�Ӧ����Ϊv2��FG�εķ�Ӧ����Ϊv3����v1��v2��v3�Ӵ�С��˳��Ϊ_______���������v1��v2��С��ϵ����Ҫԭ����__________��
(2)Ϊ�˼���������Ӧ�����ʣ��������Һ�м����������ʣ�����Ϊ���е���_____(����)
A.Ũ���� B.Na2CO3 C.����ˮ D.Ũ����
(3)����Ӧ��������Һ����ı仯���Բ��ƣ��������ʾ�Ļ�ѧ��Ӧ����v(HCl)=________mol/(Lmin)��.
���𰸡�v2>v1>v3 ��Ӧ����ʹ��Һ�¶����ߡ�����ʯ������С C 1
��������
(1)��λʱ����������������Խ��Ӧ����Խ��
(2)������Ӧ���ʣ�Ӧ��С��Һ��Ũ�ȣ�
(3)��v(HCl)=![]() ���㡣
���㡣
(1)��ͼ���֪����λʱ�������ɵ�����EF�Σ�OE�Σ�FG�Σ���λʱ����������������Խ��Ӧ����Խ����v2��v1��v3���������v1��v2��С��ϵ����Ҫԭ���Ƿ�Ӧ����ʹ��Һ�¶����ߣ��¶����ߣ���Ӧ���ʼӿ죻����ʯ������С���������ԽС�������Խ��Ӧ����Խ�죻
(2)A.����Ũ���ᣬʹ��Һ��c(H+)����Ӧ��������A����
B.����̼���ƣ���Һ��c(CO32-)����Ӧ��������B����
C.��������ˮ����Һ��c(H+)��С����Ӧ���ʼ�С��C��ȷ��
D.����Ũ���ᣬ�����Ũ��������Һ��c(H+)����Ӧ��������D����
�ʺ���ѡ����C��
(4)EF�η�Ӧ����CO2�����V(CO2)=4.48L-1.12L=3.36L��n(CO2)=![]() =0.15mol�����ݷ�Ӧ����ʽCaCO3+2HCl=CaCl2+CO2��+H2O
=0.15mol�����ݷ�Ӧ����ʽCaCO3+2HCl=CaCl2+CO2��+H2O
��֪n(HCl)=2n(CO2)=0.3mol����Ӧ���������Ũ��Ϊc(HCl)=![]() =1mol/L��
=1mol/L��


 ��������һ���þ�ϵ�д�
��������һ���þ�ϵ�д� Сѧ��10����Ӧ����ϵ�д�
Сѧ��10����Ӧ����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����.��1����һ�鴿����пƬ����ʢ��ϡ������ձ��У��ɹ۲쵽пƬ���ܽ⣬�������ݲ�����ƽ�еز���һ��ͭƬ(��ͼ��װ����ʾ)���ɹ۲쵽ͭƬ��___ (��С���û�С�)���ݲ��������õ��߰�пƬ��ͭƬ��������(��ͼ��װ����ʾ)���ɹ۲쵽ͭƬ��____ (��С���û�С�)���ݲ�����
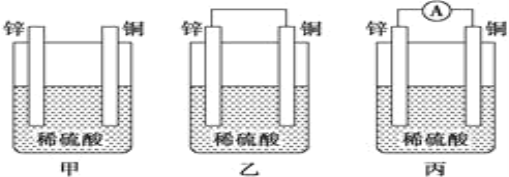
��2���ҡ���װ���ǽ�_____��ת��Ϊ____�ܵ�װ�ã����ǰ�������________��
��.��������ȵ�пƬ��ͭƬ�õ���������������500 mL����ͭ��Һ�й�����ͼ��ʾ��װ�á�

��1����װ�����ܷ�Ӧ�����ӷ���ʽΪ____________��ͭƬ��Χ��Һ�����_________������
��2����2 min����пƬ��������1.3 g�������������ĵ���Ϊ________mol��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������ֲ�ﻨ�۹ܵ��쳤����Ҫ���ã����ȱ��ֲ����ֳ���������ʵ�������ֲ�֢��ֻҪ��ֲ���Ҷ������ʩһ��Ũ�ȵĺ�����Һ���ò�֢����ʧ�����������ʵ����˵������
A. ����Ԫ�� B. ��Ԫ��
C. ����Ԫ�� D. ����Ԫ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������Ԫ��Q��R��T��W��Ԫ�����ڱ��е�λ����ͼ��ʾ������T������.������������������ȡ�
![]()
��ش��������⣺
(1)W�����ڱ��е�λ����____________________________________��Q��R��T����Ԫ��ԭ�Ӱ뾶�ɴ�С��˳��Ϊ____________________________________________________________________��(��Ԫ�ط��ű�ʾ)��QO2�ĵ���ʽΪ________________________��R�����������Ļ�ѧʽ____________________________��
(2)T������NaOH ��Һ��Ӧ�����ӷ���ʽΪ____________________________________________________________________ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����ΪԪ�����ڱ���һ���֣�
̼ | �� | Y | |
X | �� | Z |
�ش��������⣺
��1��ZԪ�������ڱ��е�λ��Ϊ______________________��
��2������Ԫ��ԭ�Ӱ뾶�����ǣ�дԪ�ط��ţ�_____________��
��3��������ʵ��˵��YԪ�صķǽ����Ա�SԪ�صķǽ�����ǿ����___________��
a��Y������H2S��Һ��Ӧ����Һ�����
b����������ԭ��Ӧ�У�1molY���ʱ�1molS�õ��Ӷ�
c��Y��S��Ԫ�صļ��⻯�����ȷֽ⣬ǰ�ߵķֽ��¶ȸ�
��4��̼��þ���ɵ�1mol������Q��ˮ��Ӧ����2mol Mg(OH)2��1mol��������������̼��������Ϊ9��1�����ĵ���ʽΪ_________��Q��ˮ��Ӧ�Ļ�ѧ����ʽΪ____��
��5��ͭ��һ��Ũ�ȵ����������Ļ���ᷴӦ�����ɵ���ֻ������ͭ��ͬʱ���ɵ�������������ϱ�������Ԫ����ɣ��������Է���������С��50��Ϊ��ֹ��Ⱦ����������������ȫת��Ϊ��ۺ������Σ�����1L 2.2molL-1NaOH��Һ��1mol O2������������ķ���ʽ�����ʵ����ֱ�Ϊ____________����������ͭ���ʵ���Ϊ_____________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��M���ճ������в���ȱ�ٵĵ�ζƷ����֪C����D��ȼ�շ�����ɫ���档M���������ʼ��ת����ϵ����ͼ��ʾ�����ֲ�������ȥ��

��1����A�ǵ؉��к������Ľ���Ԫ�أ���A���Ȼ�����Һ������������Һ�������ϣ��õ��ij�������AԪ������Һ��AԪ�ص�������ȣ���A�ĸ��Ȼ�����Һ������������Һ�����ʵ���Ũ��֮�ȿ���Ϊ____________��
��2����A��CO2���壬A��B��Һ��Ӧ�����õ���Һ�������ᷴӦ���ų���������ʵ����������������֮��Ĺ�ϵ��ͼ��ʾ:��A��B��Һ��Ӧ����Һ�е�����Ϊ___________���ѧʽ�������ʵ���֮��Ϊ_______��

��3����A��һ�����Σ�A�ֱܷ���B��F��Һ��Ӧ������ɫ�Ҿ��д̼�����ζ�����壬��A�Ļ�ѧʽΪ_____________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������йص�����;��˵������ȷ����
A.�����������ĸ�ѹ�ƵƳ����ڵ�·�㳡������
B.��ԭ���ۿ�����ʳƷ���ڵĿ�������
C.þ��һ����Ҫ�Ľ������ϣ������ʵ����²���
D.��������������ˮ��������ҩ��ĺϳ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������⻯������࣬�����������ֳ��£�N2H4����ɫ��״Һ�壩��һ��Ӧ�ù㷺�Ļ���ԭ�ϣ����������ȼ�ϣ��ش��������⣺
��1���������ӵĵ���ʽΪ__________________�����е��Ļ��ϼ�Ϊ _________��
��2�� ��2O2(g)+N2(g)=N2O4(l) ��H1
��N2(g)+2H2(g)=N2H4(l) ��H2
��O2(g)+2H2(g)=2H2O(g) ��H3
��2 N2H4(l) + N2O4(l)= 3N2(g)+ 4H2O(g) ��H4=-1048.9kJ/mol
������Ӧ��ЧӦ֮��Ĺ�ϵʽΪ��H4=____________________��������N2O4����Ϊ����ƽ�������Ҫԭ��Ϊ_________________________________________��
��3��������һ�ֳ��õĻ�ԭ������װ������AgBr���Թ��м���������Һ���۲쵽�������ǹ�����ڣ����������ݲ�����д���÷�Ӧ�Ļ�ѧ����ʽ__________________��
��4���������������ڴ�����ѹ��¯ˮ�е�������ֹ��¯����ʴ��������1kg�������ɳ�ȥˮ���ܽ��O2_____kg����ʹ��Na2SO3����ˮ���ܽ��O2��ȣ��������ŵ���__________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪A��B��C��D��E�������ڱ���ǰ�����ڵ�Ԫ�أ����ǵĺ˵����A��B��C��D��E������A��B��C��ͬһ���ڵķǽ���Ԫ�ء�������DC�ľ���Ϊ���Ӿ��壬D�Ķ�����������C�������Ӿ�����ͬ�ĵ��Ӳ�ṹ��AC2Ϊ�Ǽ��Է��ӡ�B��C���⻯��ķе������ͬ����������Ԫ���⻯��ķе�ߡ�E��ԭ������Ϊ24��ECl3����B���⻯���γ�����λ������������������λ����硣
���������������ش��������⣺������ʱ��A��B��C��D��E������Ӧ��Ԫ�ط��ű�ʾ��
��1��A��B��C�ĵ�һ��������С�����˳��Ϊ____��
��2��B���⻯��ķ��ӿռ乹����____��
��3��д��AC2�ĵ���ʽ____��������ԭ�Ӳ�ȡ____�ӻ���
��4��ECl3�γɵ������Ļ�ѧʽΪ____��1mol��������ЦҼ���ĿΪ____mol��
��5��B���⻯����Һ����ԭ����____��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com