
ijĢ½¾æŠŌѧĻ°Š”×éÄāĶعżŠæÓėŃĪĖįµÄ·“Ӧъ¾æÓ°Ļģ·“Ó¦ĖŁĀŹµÄŅņĖŲ”£
øĆĢ½¾æŠŌѧĻ°Š”×éÓĆĻąĶ¬ÖŹĮæµÄŠæŗĶĻąĶ¬ÅØ¶ČµÄ×ćĮæµÄĻ”ŃĪĖį·“Ó¦µĆµ½ŹµŃ鏿¾ŻČēĻĀ±ķĖłŹ¾£ŗ
ŹµŃ鱹ŗÅ | ŠæµÄדĢ¬ | ·“Ó¦ĪĀ¶Č/”ę | ŹÕ¼Æ100mLĒāĘųĖłŠčŹ±¼ä/s |
¢ń | ±”ʬ | 15 | 200 |
¢ņ | ±”ʬ | 25 | 90 |
¢ó | ·ŪÄ© | 25 | 10 |
£Ø1£©øĆŹµŃéµÄÄæµÄŹĒĢ½¾æ ”¢ ¶ŌŠæŗĶĻ”ŃĪĖį·“Ó¦ĖŁĀŹµÄÓ°Ļģ£»
£Ø2£©ŹµŃé¢ńŗĶ¢ņ±ķĆ÷ £¬»Æѧ·“Ó¦ĖŁĀŹŌ½“ó£»
£Ø3£©ÄܱķĆ÷¹ĢĢåµÄ±ķĆ껿¶Ō·“Ó¦ĖŁĀŹÓŠÓ°ĻģµÄŹµŃ鱹ŗÅŹĒ ŗĶ £¬ŹµŃé½įĀŪŹĒ £»
£Ø4£©ĒėÉč¼ĘŅ»øöŹµŃé·½°øÖ¤Ć÷ŃĪĖįµÄÅØ¶Č¶ŌøĆ·“Ó¦µÄĖŁĀŹµÄÓ°Ļģ£ŗ
ӣ

| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2016½ģŗžÄĻŹ”µČĖÄŠ£øßČżĮŖæ¼»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
Ņ»¶ØĢõ¼žĻĀŗĻ³ÉŅŅĻ©6H2(g) + 2CO2(g) CH2=CH2(g) + 4H2O(g)£»ŅŃÖŖĪĀ¶Č¶ŌCO2µÄĘ½ŗā×Ŗ»ÆĀŹŗĶ“߻ƼĮ“߻Ɗ§ĀŹµÄÓ°ĻģČēĶ¼£¬ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ
CH2=CH2(g) + 4H2O(g)£»ŅŃÖŖĪĀ¶Č¶ŌCO2µÄĘ½ŗā×Ŗ»ÆĀŹŗĶ“߻ƼĮ“߻Ɗ§ĀŹµÄÓ°ĻģČēĶ¼£¬ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ
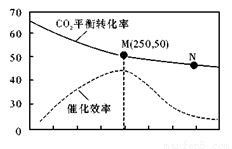
A£®Éś³ÉŅŅĻ©µÄĖŁĀŹ£ŗ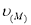 £¾
£¾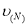
B£®Ę½ŗā³£Źż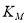 £¼
£¼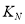
C£®“߻ƼĮæÉÄÜ»įÓ°ĻģCO2µÄĘ½ŗā×Ŗ»ÆĀŹ
D£®ČōĶ¶ĮĻ±Čn(H2):n(CO2)=3:1£¬ŌņĶ¼ÖŠMµćŹ±£¬CO2µÄĢå»ż·ÖŹżŌ¼ĪŖ15.4%
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2015-2016Ń§ÄźÉ½Ī÷Ź”øßŅ»ĻĀĘŚÖŠ»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗĢīæÕĢā
ĪåÖÖ¶ĢÖÜĘŚŌŖĖŲµÄ²æ·ÖŠŌÖŹŹż¾ŻČēĻĀ£ŗ
ŌŖĖŲ | T | X | Y | Z | W |
Ō×Ó°ė¾¶£Ønm£© | 0.037 | 0.075 | 0.099 | 0.102 | 0.143 |
×īøß»ņ×īµĶ»ÆŗĻ¼Ū | +1 | +5£3 | +7£1 | +6£2 | +3 |
£Ø1£©ZĄė×ӵĽį¹¹Ź¾ŅāĶ¼ĪŖ ”£
£Ø2£©¹ŲÓŚY”¢ZĮ½ÖÖŌŖĖŲ£¬ĻĀĮŠŠšŹöÕżČ·µÄŹĒ £ØĢīŠņŗÅ£©”£
a£®¼ņµ„Ąė×ӵİė¾¶ Y > Z
b£®ĘųĢ¬Ēā»ÆĪļµÄĪČ¶ØŠŌY±Č ZĒæ
c£®×īøß¼ŪŃõ»ÆĪļ¶ŌÓ¦Ė®»ÆĪļµÄĖįŠŌZ±ČYĒæ
£Ø3£©¼×ŹĒÓÉT”¢XĮ½ÖÖŌŖĖŲŠĪ³ÉµÄ10 e£·Ö×Ó£¬ŅŅŹĒÓÉY”¢WĮ½ÖÖŌŖĖŲŠĪ³ÉµÄ»ÆŗĻĪļ”£Ä³Ķ¬Ń§Éč¼ĘĮĖĻĀĶ¼ĖłŹ¾×°ÖĆ£Ø¼Š³ÖŅĒĘ÷Ź”ĀŌ£©½ųŠŠŹµŃ飬½«¼×µÄÅØČÜŅŗÖšµĪ¼ÓČėµ½NaOH¹ĢĢåÖŠ£¬ÉÕĘæÖŠ¼“ÓŠ¼×·Å³ö£¬ŌŅņŹĒ ”£Ņ»¶ĪŹ±¼äŗ󣬹Ū²ģµ½ŹŌ¹ÜÖŠµÄĻÖĻóŹĒ £¬·¢Éś·“Ó¦µÄĄė×Ó·½³ĢŹ½ŹĒ ”£
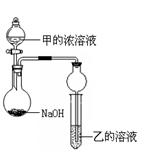
£Ø4£©T”¢XĮ½ÖÖŌŖĖŲŠĪ³ÉXT5¹ĢĢ壬ĖüµÄĖłÓŠŌŗ×ÓµÄ×īĶā²ć¶¼·ūŗĻĻąÓ¦Ļ”ÓŠĘųĢåŌ×ÓµÄ×īĶā²ć½į¹¹£¬ŌņĘäµē×ÓŹ½ĪŖ_____”£
£Ø5£©XO2ŹĒµ¼ÖĀ¹ā»ÆѧŃĢĪķµÄ”°×ļæż»öŹ×”±Ö®Ņ»”£Ėü±»ĒāŃõ»ÆÄĘČÜŅŗĪüŹÕµÄ»Æѧ·½³ĢŹ½ŹĒ£ŗ2XO2 + 2NaOH = M + NaXO3 + H2O£ØŅŃÅäĘ½£©£¬²śĪļMÖŠŌŖĖŲXµÄ»ÆŗĻ¼ŪĪŖ ”£
£Ø6£©³£ĪĀĻĀ£¬Z2Y2ŹĒŅ»ÖÖ³Č»ĘÉ«ŅŗĢ壬¹ć·ŗÓĆÓŚĻš½ŗ¹¤ŅµµÄĮņ»Æ»ś£¬Ęä·Ö×Ó½į¹¹ÓėĖ«ŃõĖ®·Ö×ÓĻąĖĘ”£ŹŌŠ“³öĘä½į¹¹Ź½_____”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2015-2016Ń§ÄźÉ½Ī÷Ź”øßŅ»ĻĀĘŚÖŠ»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
ĻĀĮŠĖµ·ØÖŠÕżČ·µÄŹĒ
A£®ĪļÖŹ·¢Éś»Æѧ·“Ó¦¶¼°éĖę×ÅÄÜĮæ±ä»Æ
B£®°éÓŠÄÜĮæ±ä»ÆµÄĪļÖŹ±ä»Æ¶¼ŹĒ»Æѧ±ä»Æ
C£®ŌŚŅ»øöČ·¶ØµÄ»Æѧ·“Ó¦¹ŲĻµÖŠ£¬·“Ó¦ĪļµÄ×ÜÄÜĮæ×ÜŹĒøßÓŚÉś³ÉĪļµÄ×ÜÄÜĮæÓŠæÉÄÜĻąĶ¬
D£®Čē¹ū¾É»Æѧ¼ü¶ĻĮŃĪüŹÕµÄÄÜĮæ“óÓŚŠĀ»Æѧ¼üŠĪ³ÉŹĶ·ÅµÄÄÜĮ棬ŌņøĆ·“Ó¦ĪŖ·ÅČČ·“Ó¦
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2015-2016Ń§ÄźÉ½Ī÷Ź”øßŅ»ĻĀĘŚÖŠ»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
øł¾ŻŌŖĖŲÖÜĘŚ±ķŗĶŌŖĖŲÖÜĘŚĀÉ·ÖĪöĻĀĆęµÄĶʶĻ£¬ĘäÖŠ“ķĪóµÄŹĒ
A£®īė£ØBe£©µÄŌ×ÓŹ§µē×ÓÄÜĮ¦±ČĆ¾Čõ
B£®ķĮ£ØAt£©ĪŖÓŠÉ«¹ĢĢ壬AgAtÄŃČÜÓŚĖ®Ņ²²»ČÜÓŚĻ”ĻõĖį
C£®ĒāŃõ»ÆļČ[Sr(OH)2]±ČĒāŃõ»ÆøĘµÄ¼īŠŌĒæ
D£®Īų£ØSe£©»ÆĒā±ČĮņ»ÆĒāĪȶØ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2015-2016ѧğĞĻÄÓż²Å֊ѧøßŅ»ĻĀĘŚÖŠ»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
ĪĀ¶ČĪŖ500”ꏱ£¬·“Ó¦4NH3+5O2 4NO+6H2OŌŚ5LµÄĆܱÕČŻĘ÷ÖŠ½ųŠŠ£¬°ė·ÖÖÓŗóNOµÄĪļÖŹµÄĮæŌö¼ÓĮĖ0.3mol£¬Ōņ“Ė·“Ó¦µÄĘ½¾łĖŁĀŹ
4NO+6H2OŌŚ5LµÄĆܱÕČŻĘ÷ÖŠ½ųŠŠ£¬°ė·ÖÖÓŗóNOµÄĪļÖŹµÄĮæŌö¼ÓĮĖ0.3mol£¬Ōņ“Ė·“Ó¦µÄĘ½¾łĖŁĀŹ (x)ĪŖ ( )
(x)ĪŖ ( )
A£® £ØO2£©=0.01mol/£ØL•s£© B£®
£ØO2£©=0.01mol/£ØL•s£© B£® £ØNO£©=0.08mol/£ØL•s£©
£ØNO£©=0.08mol/£ØL•s£©
C£® £ØH2O£©=0.0013mol/£ØL•s£© D£®
£ØH2O£©=0.0013mol/£ØL•s£© D£® £ØNH3£©=0.002mol/£ØL•s£©
£ØNH3£©=0.002mol/£ØL•s£©
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2015-2016ѧğĞĻÄÓż²Å֊ѧøßŅ»ĻĀĘŚÖŠ»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
ĻĀĮŠ¹ŲÓŚ³äµēµē³ŲµÄŠšŹö£¬²»ÕżČ·µÄŹĒ £Ø £©
A£®³äµēµē³ŲæÉŅŌĶعż·Åµē”¢³äµēŹµĻÖ»ÆѧÄÜŗĶµēÄܵÄĻą»„×Ŗ»Æ
B£®·ÅµēŹ±øŗ¼«·¢ÉśŃõ»Æ·“Ó¦£¬³äµēŹ±øƵē¼«ÉĻÓŠĪļÖŹ·¢ÉśµĆµē×ӵķ“Ó¦
C£®ĻÖ“ś¼¼ŹõŹ¹µĆµē³ŲÉč¼Ę±Č½ĻĻČ½ų£¬µē³Ų·ĻĘśŗó²»±ŲŌŁ½ųŠŠĪŽ¶¾»Æ“¦Ąķ
D£®³äµēµē³ŲµÄ»Æѧ·“Ó¦ŌĄķŹĒŃõ»Æ»¹Ō·“Ó¦
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2016½ģÕć½Ź”Äž²ØŹŠµČŹ®Š£øßČż3ŌĀĮŖæ¼Ąķ×Ū»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗĢīæÕĢā
¹¤ŅµÉĻŅ»°ćŅŌCOŗĶH2ĪŖŌĮĻŗĻ³É¼×“¼£¬øĆ·“Ó¦µÄČČ»Æѧ·½³ĢŹ½ĪŖ£ŗ
CO(g)+ 2H2(g) CH3OH(g) ”÷H
CH3OH(g) ”÷H
£Ø1£©ŅŃÖŖCO(g)”¢H2(g)µÄ±ź×¼Č¼ÉÕČČ·Ö±šĪŖ-285.8kJ•mol-1£¬-283.0kJ•mol-1£¬
ĒŅCH3OH(g)+3/2O2(g)  CO2(g)+2H2O(l) ”÷H=£761kJ/mol£»
CO2(g)+2H2O(l) ”÷H=£761kJ/mol£»
ŌņCO(g)+ 2H2(g) CH3OH(g)µÄ”÷H= ”£
CH3OH(g)µÄ”÷H= ”£
£Ø2£©Čō½«µČĪļÖŹµÄĮæµÄCOŗĶH2»ģŗĻĘųĢå³äČėŗćĪĀŗćČŻĆܱÕČŻĘ÷ÖŠ½ųŠŠÉĻŹö·“Ó¦£¬ĻĀĮŠŹĀŹµÄÜĖµĆ÷“Ė·“Ó¦ŅŃ“ļµ½Ę½ŗāדĢ¬µÄŹĒ ”£
A£®ČŻĘ÷ÄŚĘųĢåĆܶȱ£³Ö²»±ä B£®»ģŗĻĘųĢåµÄĘ½¾łĻą¶Ō·Ö×ÓÖŹĮæ²»±ä
C£®Éś³ÉCH3OHµÄĖŁĀŹÓėÉś³ÉH2µÄĖŁĀŹĻąµČ D£®COµÄĢå»ż·ÖŹż±£³Ö²»±ä
£Ø3£©ĻĀĮŠ“ėŹ©ÖŠ¼ČÓŠĄūÓŚŌö“óøĆ·“Ó¦µÄ·“Ó¦ĖŁĀŹÓÖÄÜŌö“óCO×Ŗ»ÆĀŹµÄŹĒ ”£
A£®½«CH3OH¼°Ź±“Ó»ģŗĻĪļÖŠ·ÖĄė
B£®½µµĶ·“Ó¦ĪĀ¶Č
C£®ŗćȯװÖĆÖŠ³äČėH2
D£®Ź¹ÓĆøߊ§“߻ƼĮ
£Ø4£©ŌŚČŻ»żĪŖ2LµÄŗćČŻČŻĘ÷ÖŠ£¬·Ö±šŃŠ¾æ·“Ó¦ŌŚ300”ę”¢350”ęŗĶ400”ęČżÖÖĪĀ¶ČĻĀŗĻ³É¼×“¼µÄ¹ęĀÉ”£ÓŅĶ¼ŹĒÉĻŹöČżÖÖĪĀ¶ČĻĀ²»Ķ¬µÄH2ŗĶCOµÄĘšŹ¼×é³É±Č(ĘšŹ¼Ź±COµÄĪļÖŹµÄĮæ¾łĪŖ1mol)ÓėCOĘ½ŗā×Ŗ»ÆĀŹµÄ¹ŲĻµ”£Ēė»Ų“š£ŗ
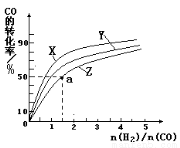
¢ŁŌŚÉĻŹöČżÖÖĪĀ¶ČÖŠ£¬ĒśĻßX¶ŌÓ¦µÄĪĀ¶ČŹĒ
¢ŚĄūÓĆĶ¼ÖŠaµć¶ŌÓ¦µÄŹż¾Ż£¬¼ĘĖć³öĒśĻßZŌŚ¶ŌÓ¦ĪĀ¶ČĻĀ
CO(g)+ 2H2(g)  CH3OH(g) µÄĘ½ŗā³£ŹżK = ”£
CH3OH(g) µÄĘ½ŗā³£ŹżK = ”£
£Ø5£©ĘäĖūĢõ¼žĻąĶ¬Ź±£¬Ä³Ķ¬Ń§ŃŠ¾æøĆ¼×“¼ŗĻ³É·“Ó¦ŌŚ²»Ķ¬“߻ƼĮ¢ń»ņ¢ņ×÷ÓĆĻĀ·“Ó¦ĻąĶ¬Ź±¼äŹ±£¬COµÄ×Ŗ»ÆĀŹĖę·“Ó¦ĪĀ¶ČµÄ±ä»ÆĒéæö”£ĒėŌŚÓŅĶ¼ÖŠ²¹³ät”ęŗóµÄ±ä»ÆĒéæö”£

²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2016½ģ¼ŖĮÖŹ”øßČżµŚ¶ž“ĪÄ£ÄāĄķ×Ū»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŹµŃéĢā
ĪŖĮĖŌ¤·Ąµāȱ·¦Ö¢£¬¹ś¼Ņ¹ę¶ØĆæĒ§æĖŹ³ŃĪÖŠÓ¦ŗ¬ÓŠ40”«50 mgµāĖį¼Ų”£µāĖį¼Ų¾§Ģå¾ßÓŠ½ĻøßµÄĪČ¶ØŠŌ£¬µ«ŌŚĖįŠŌČÜŅŗÖŠ£¬µāĖį¼ŲŹĒŅ»ÖÖ½ĻĒæµÄŃõ»Æ¼Į£¬ÄÜøśÄ³Š©»¹Ō¼Į·“Ӧɜ³Éµā£»ŌŚ¼īŠŌČÜŅŗÖŠ£¬µāĖį¼ŲÄܱ»ĀČĘų”¢“ĪĀČĖįµČøüĒæµÄŃõ»Æ¼ĮŃõ»ÆĪŖøüøß¼ŪµÄµāµÄŗ¬ŃõĖįŃĪ”£¹¤ŅµÉś²śµāĖį¼ŲµÄĮ÷³ĢČēĶ¼ĖłŹ¾”£
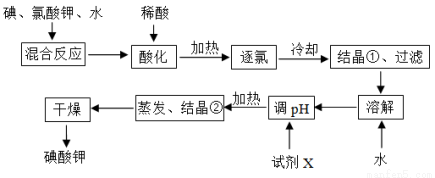
£Ø1£©µāŌŚÖÜĘŚ±ķÖŠµÄĪ»ÖĆĪŖ__________________£»
£Ø2£©µā”¢ĀČĖį¼Ų”¢Ė®»ģŗĻ·“Ó¦Ź±£¬ČōĮ½ÖÖ»¹Ō²śĪļĖłµĆµē×ӵďżÄæĻąĶ¬£¬ĒėÅäĘ½øĆ·“Ó¦µÄ»Æѧ·½³ĢŹ½£ŗ____I2+____KClO3+____H2O=____KH(IO3)2+____KCl+____Cl2”ü£»
£Ø3£©»ģŗĻ·“Ó¦ŗó£¬ÓĆĻ”ĖįĖį»ÆµÄ×÷ÓĆŹĒ___________________________£¬ŌŚĻ”ŃĪĖįŗĶĻ”ĻõĖįÖŠ²»ÄÜŃ”ÓƵÄĖįŹĒ_________£¬ĄķÓÉŹĒ__________________________________£»
£Ø4£©ŹŌ¼ĮXµÄ»ÆѧŹ½ĪŖ__________£¬Š“³öÓĆŹŌ¼ĮXµ÷pHµÄ»Æѧ·½³ĢŹ½__________________£»
£Ø5£©Čē¹ūŹ”ĀŌ”°Ėį»Æ”±”¢”°ÖšĀČ”±”¢”°½į¾§¢Ł”¢¹żĀĖ”±ÕāČż²½²Ł×÷£¬Ö±½ÓÓĆŹŌ¼ĮXµ÷Õū·“Ó¦»ģŗĻĪļµÄpH£¬¶ŌÉś²śµāĖį¼ŲÓŠŹ²Ć“Ó°Ļģ£æ________________________________________”£
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com