
【题目】用相对分子质量为 43 的烷基取代甲苯上的一个氢原子,所得芳香烃产物的数目为( )
A.3 种B.4 种C.6 种D.8 种
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】二水氯化钡晶体(BaCl22H2O)在工业上主要用于制造各种钡盐、颜料和有机染料,某研究小组以重晶石(主要成分 BaSO4)制备BaCl22H2O 流程如下图。
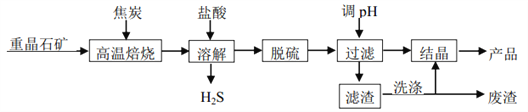
(1)已知:
① BaSO4(s)+ 4C(s)= 4CO(g) + BaS(s) △H1 = 571.2kJmol﹣1
② C(s)+ CO2(g)= 2CO(g) △H2 = 172.5 kJmol﹣1
反应 BaSO4(s)+ 2C(s)= 2CO2(g)+ BaS(s)的△H = _____ kJmol﹣1
(2)高温焙烧须加入过量的炭,同时还要通入空气,其目的是_____、_____。
(3)脱硫过程中分为两步, 第一步是物理脱硫, 第二步是化学脱硫。
① 物理脱硫是直接用蒸汽升温,并用空气“爆气法”除去的物质是_____。
② 下列物质不宜用作脱硫剂的是_____ (填字母)。
A. 高锰酸钾 B. 次氯酸钠 C. 双氧水 D.氯气
(4)上述流程中洗涤滤渣的主要目的是_____。
(5)溶解时产生的 H2S 可用 80~85 ℃时的石灰氮料浆(CaCN2的浆水混合物)吸收并制得更有价值的产品——硫脲[CS(NH2)2]和熟石灰。请写出制备硫脲的化学方程式_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A. 碱金属的单质中,锂的还原性最强
B. 第ⅠA族元素比第ⅡA族元素的金属性强
C. 随核电荷数递增,第三周期元素的氧化物对应的水化物酸性逐渐增强
D. 随着核电荷数的递增,卤族元素的气态氢化物的稳定性逐渐减弱
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知3.01×1023个X气体分子的质量为16 g,则X气体的摩尔质量是
A. 16 g B. 32 g C. 64 g /mol D. 32 g /mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用零价铁(Fe)去除水体中的硝酸盐(NO3-)已成为环境修复研究的热点之一。
(1)Fe还原水体中NO3-的反应原理如图所示。

①作负极的物质是__________。
②正极的电极反应式是__________。
(2)将足量铁粉投入水体中,经 24小时测定 NO3-的去除率和pH,结果如下:
初始 pH | pH=2.5 | pH=4.5 |
NO3-的去除率 | 接近 100% | <50% |
24 小时 pH | 接近中性 | 接近中性 |
铁的最终物质 形态 |
|
|
pH=4.5 时,NO3-的去除率低,其原因是_____________。
(3)实验发现:在初始 pH=4.5 的水体中投入足量铁粉的同时,补充一定量的 Fe2+可以明显提高NO3-的去除率。对Fe2+的作用提出两种假设:
Ⅰ.Fe2+直接还原NO3-;
Ⅱ.Fe2+破坏 FeO(OH)氧化层。
①做对比实验,结果如图所示,可得到的结论是________。

②同位素示踪法证实 Fe2+能与 FeO(OH)反应生成 Fe3O4。结合该反应的离子方程式,解释加入 Fe2+提高NO3-去除率的原因:_____________。
(4) 其他条件与(2)相同,经 1小时测定NO3-的去除率和 pH,结果如下:
初始 pH | pH=2.5 | pH=4.5 |
NO3-的去除率 | 约10% | 约3% |
1小时pH | 接近中性 | 接近中性 |
与(2)中数据对比,解释(2)中初始 pH不同时,NO3-去除率和铁的最终物质形态不同的原因:_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如下图所示,其中甲池的总反应式为2CH3OH+3O2+4KOH=2K2CO3+6H2O。下列说法正确的是()。
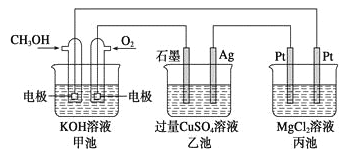
A. 甲池是电能转化为化学能的装置,乙、丙池是化学能转化为电能的装置
B. 甲池通入CH3OH的电极反应式为CH3OH-6e-+2H2O=CO32-+8H+
C. 反应一段时间后.向乙池中加入一定量Cu(OH)2固体能使CuSO4溶液恢复到原浓度
D. 甲池中消耗280mL(标准伏况下)O2,此时丙池中理论上最多产生1.45g固体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据表中信息,判断下列叙述中正确的是( )
序号 | 氧化剂 | 还原剂 | 其他反应物 | 氧化产物 | 还原产物 |
① | Cl2 | FeBr2 | / | Fe3+、Br2 | |
② | KClO3 | 浓盐酸 | / | Cl2 | |
③ | KMnO4 | H2O2 | H2SO4 | O2 | Mn2+ |
A. 由表中①组的信息可知通入Cl2的量不同,氧化产物可能不同
B. 反应①中,当只有少量Cl2时,反应可表示为Cl2+ Fe2+===Fe3++ 2Cl-
C. 表中②组反应的还原产物是KCl,电子转移数目是6e-
D. 表中③组反应的离子方程式为2MnO![]() + 3H2O2+6H+===2Mn2++ 4O2↑+ 6H2O
+ 3H2O2+6H+===2Mn2++ 4O2↑+ 6H2O
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com