

| 温度(℃) | 20 | 30 | 40 | 50 | 60 | 70 | 80 |
| 铜的平均溶解速率 (×10-3mol•L-1•min-1) | 7.34 | 8.01 | 9.25 | 7.98 | 7.24 | 6.73 | 5.76 |
分析 (1)X、Y、Z三种短周期元素,其单质在常温下均为无色气体,短周期中形成无色气体单质的只有H2、N2、O2(稀有气体除外),H、N、O原子序数之和为16,故三种元素为H、N、O,三种气体单质相互反应生成H2O、NH3、NO,一个B分子中含有的Z元素的原子个数比一个C分子中少一个,则B为H2O,C为NH3,Z为氢元素.由关系图可知:Z单质与X单质反应生成B(H2O),故X为氧元素;Z单质与Y单质反应生成C(NH3),故Y为氮元素,所以A为NO;
(2)原电池负极发生氧化反应,氨气在负极放电,碱性条件下生成氮气与水;溶液中阴离子向负极移动;
(3)H分别与O、N两元素可以构成18个电子分子甲和乙,则甲为H2O2,乙为N2H4.
①根据电子转移计算N元素在产物中的化合价,确定产物,据此书写;
②温度升高H2O2的分解速率加快,导致H2O2的浓度降低从而使铜的溶解速率慢;
③H2O2在二氧化锰作催化剂分解生成氧气,反应不需要加热.
解答 解:(1)X、Y、Z三种短周期元素,其单质在常温下均为无色气体,短周期中形成无色气体单质的只有H2、N2、O2(稀有气体除外),H、N、O原子序数之和为16,故三种元素为H、N、O,三种气体单质相互反应生成H2O、NH3、NO,一个B分子中含有的Z元素的原子个数比一个C分子中少一个,则B为H2O,C为NH3,Z为氢元素.由关系图可知:Z单质与X单质反应生成B(H2O),故X为氧元素;Z单质与Y单质反应生成C(NH3),故Y为氮元素,所以A为NO.
由 H、N、O三种元素共同组成的三种不同种类化合物的化学式为:NH4NO3、NH3•H2O、HNO3,硝酸铵溶液中铵根离子的水解,溶液呈酸性,一水合氨溶液呈碱性,硝酸是强电解质,故相同浓度上述水溶液中,由水电离出的c(H+)由大到小的顺序是NH4NO3、NH3•H2O、HNO3,
故答案为:NH4NO3、NH3•H2O、HNO3;HNO3;
(2)原电池负极发生氧化反应,氨气在负极放电,碱性条件下生成氮气与水,电极反应式为:4NH3+12OH--12e-=2N2+12H2O,溶液中阴离子向负极移动,
故答案为:4NH3+12OH--12e-=2N2+12H2O;负;
(3)H分别与O、N两元素可以构成18个电子分子甲和乙,则甲为H2O2,乙为N2H4,
①令N元素在氧化产物的化合价为x,由电子转移守恒可知,2[x-(-2)]=4,解得x=0,故生成氮气,根据原子守恒可知,还生成水,故方程式为:N2H4+4CuO=N2↑+2Cu2O+2H2O,
故答案为:N2H4+4CuO=N2↑+2Cu2O+2H2O;
②温度升高H2O2的分解速率加快,导致H2O2的浓度降低从而使铜的溶解速率慢,
故答案为:温度升高H2O2的分解速率加快,导致H2O2的浓度降低从而使铜的溶解速率慢;
③H2O2在二氧化锰作催化剂分解生成氧气,反应不需要加热,D装置不能收集氧气,故选C装置,
故答案为:C.
点评 本题考查元素及无机物的推断、原电池、氧化还原反应、影响化学反应速率的因素、化学实验等,难度中等,题目较为综合,是对学生综合能力的考查,推断元素是解题的关键.


科目:高中化学 来源: 题型:选择题
| A. | 阳极发生氧化反应,其电极反应式主要是:Ni-2e-=Ni2+ | |
| B. | 电解过程中,阳极质量的减少与阴极质量的增加不相等 | |
| C. | 电解后,溶液中存在的金属阳离子只有Fe2+、Ni2+和Zn2+ | |
| D. | 电解后,电解槽底部的阳极泥中只有Pt |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ③⑤⑥ | B. | ①② | C. | ③⑤ | D. | ①③④ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

 .
. .
.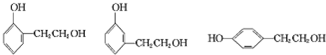 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 海水$\stackrel{NaOH}{→}$Mg(OH)2$\stackrel{电解}{→}$Mg | |
| B. | 海水$\stackrel{HCl}{→}$MgCl2溶液→MgCl2(熔融)$\stackrel{电解}{→}$Mg | |
| C. | 海水$\stackrel{石灰乳}{→}$Mg(OH)2$\stackrel{灼烧}{→}$MgO$\stackrel{电解}{→}$Mg | |
| D. | 海水$\stackrel{石灰乳}{→}$ Mg(OH)2$\stackrel{BCl}{→}$ MgCl2溶液→MgCl2(熔融)$\stackrel{电解}{→}$Mg |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氧化还原反应均为放热反应 | B. | 放热反应中,反应后体系能量降低 | ||
| C. | 断开化学键的过程会放出能量 | D. | 加热才能发生的反应均为吸热反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 粒子 | A+ | B2- | C | D | E | F |
| 组成特点 | 单核离子 | 化合物, 双核分子 | 单质, 双核分子 | 化合物, 三核分子 | 化合物, 四核分子 | |
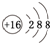 .
.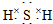 ;F的水溶液常用于消毒剂,F的化学式是H2O2.
;F的水溶液常用于消毒剂,F的化学式是H2O2.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

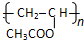 .
.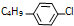 ,则R有4种.
,则R有4种.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com