
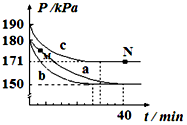
 臭氧是理想的烟气脱硝试剂,原理为:2NO2(g)+O3(g)?N2O5(g)+O2(g).若在容积为10L的密闭容器中进行该反应,起始时充入0.4molNO2、0.2molO3,反应分别在a、b、c三种不同条件下进行,反应体系总压强随时间的变化如图所示.
臭氧是理想的烟气脱硝试剂,原理为:2NO2(g)+O3(g)?N2O5(g)+O2(g).若在容积为10L的密闭容器中进行该反应,起始时充入0.4molNO2、0.2molO3,反应分别在a、b、c三种不同条件下进行,反应体系总压强随时间的变化如图所示.分析 ①实验c中,反应前压强与反应前后压强变化量之比等于反应前气体的物质的量与反应前后气体的物质的量变化量之比=190pKa:(190-171)pKa=10:1,反应前气体的总物质的量=(0.4+0.2)mol=0.6mol,则前后气体减少的物质的量为0.06mol,参加反应的二氧化氮物质的量是反应前后减少的物质的量的2倍,为0.12mol,
二氧化氮转化率=$\frac{参加反应的二氧化氮物质的量}{二氧化氮初始物质的量}$;
②与实验a相比,b中缩短到达平衡的时间,但平衡时压强不变,说明改变条件只改变反应速率但不影响平衡移动;
解答 解:①验c中,反应前压强与反应前后压强变化量之比等于反应前气体的物质的量与反应前后气体的物质的量变化量之比=190pKa:(190-171)pKa=10:1,反应前气体的总物质的量=(0.4+0.2)mol=0.6mol,则前后气体减少的物质的量为0.06mol,参加反应的二氧化氮物质的量是反应前后减少的物质的量的2倍,为0.12mol,
二氧化氮转化率=$\frac{参加反应的二氧化氮物质的量}{二氧化氮初始物质的量}$=$\frac{0.12mol}{0.4mol}$×100%=30%,故答案为:30%;
②与实验a相比,b中缩短到达平衡的时间,但平衡时压强不变,说明改变条件只改变反应速率但不影响平衡移动,所以改变的条件是使用催化剂;
故答案为:使用催化剂.
点评 本题考查化学平衡计算及化学平衡影响因素,为高频考点,侧重考查学生图象分析及计算能力,比较容易.


科目:高中化学 来源: 题型:解答题
 、O=C=O.
、O=C=O.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 编号 | 化学反应 | 离子方程式 | 评价 |
| A | 把MgSO4溶液滴入Ba(OH)2溶液 | Mg2++2OH-═Mg(OH)2↓ | 正确 |
| B | 氧化铜与稀盐酸反应 | CuO+2H+═Cu2++H2O | 错误,不反应 |
| C | 向FeCl2溶液中通入氯气 | Fe2++Cl2═Fe3++2Cl- | 错误, 电荷不守恒 |
| D | 向沸水滴入饱和氯化铁溶液 | Fe3++3H2O$\frac{\underline{\;△\;}}{\;}$Fe(OH)3↓+3H+ | 正确 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | pH=6的某电解质的溶液 | B. | c(OH-)>1×10-7mol/L | ||
| C. | 溶液中含有OH- | D. | 溶液中c(OH-)>c(H+) |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 使用滤纸称量氢氧化钠固体 | B. | 溶解后未冷却直接定容 | ||
| C. | 容量瓶不干燥,存有少量蒸馏水 | D. | 胶头滴管加水定容时俯视刻度 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 化学式 | CH3COOH | HA | HNO2 | H2CO3 |
| Ka | Ka=1.8×10-5 | Ka=4.9×10-10 | Ka=4.6×10-4 | Ka1 =4.1×10-7 Ka2 =5.6×10-11 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1.6gCH4中含有的分子数 | |
| B. | 1molH2SO4中含有的H+ 数 | |
| C. | 2.4gMg中含有的原子数 | |
| D. | 标准状况下22.4LCO气体中含有的分子数 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com