
【题目】将足量铁粉投入一定浓度的氯化铁和氯化铜的混合溶液中,充分反应后,溶液中剩余固体的质量与加人铁粉的质量相同,则原溶液中氯化铁和氯化铜的浓度之比为
A.2:7 B.3;4 C.4:7 D.2:3
科目:高中化学 来源: 题型:
【题目】1mol某烃A和1 mol苯完全燃烧,在相同条件下,生成CO2体积相同,烃A比苯多消耗1.5mol O2,试回答:
(1)烃A的分子式是__________ 。
(2)若烃A不能使溴水褪色,但在一定条件下能与Cl2发生取代反应,其一氯代物只有一种,则烃A的结构简式为_______________ 。
(3)若烃A能使溴水褪色,且分子中所有碳原子共平面,则A的结构简式为____________________________ 。
(4)比A少2个碳原子的A的烯烃的同系物的同分异构体(包括立体异构)共有__________种。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学在生产和日常生活中有着重要的应用,下列叙述正确的是
A. 白酒中混有少量的塑化剂,少量饮用对人体无害,可以通过过滤的方法除去
B. 将猕猴桃和苹果放在一起,猕猴桃更容易成熟。是因为苹果释放的乙烯具有催熟作用
C. 氨气可以做制冷剂,是因为氨气有一定的还原性
D. 大分子化合物油脂在人体内水解为氨基酸和甘油等小分子,才能被人体吸收
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表是元素周期表的一部分,针对表中的①~⑦种元素,根据题意回答以下问题:

(1)在③~⑦五种元素中,原子半径最大的是____________(填元素符号);
(2)②的原子结构示意图为__________;
(3)①~⑦对应元素中最高价氧化物对应的水化物酸性最强的是________(填化学式,下同),呈两性的是________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】碱土金属指II A族的铍(Be)、镁(Mg)、钙(Ca)、锶(Sr)、钡(Ba)等元素,它们的单质及其化合物有着广泛的用途。
(1)Be基态原子的轨道表示式为_________________________;
镁和铝的笫二电离能:I2(Mg)_____I2(Al) (填“>”“ <”或“=”)。
(2)在500~600℃气相中,氯化铍以二聚体Be2Cl4, ( )的形式存在,在1000 ℃,氯化铍则以BeCl2形式存在。
)的形式存在,在1000 ℃,氯化铍则以BeCl2形式存在。
①在二聚体Be2Cl4中Be的杂化方式为___________,1mol Be2Cl4中含有_________mol 配位键。
②MgCl2的熔、沸点比BeCl2高的原因是____________________。
(3)根据巴索洛规则:一般来讲,盐中阴、阳离子半径相差较大时,其溶解度较大。则在水中溶解度 S(SrF2)____S(BaF2) (填“>” “<””或“=”)。
(4)石灰氮(CaCN2)—种碱性肥料,可用作除草剂、杀菌剂、杀虫剂等。
①CaCN2中阴离子为CN22-,与CN22-互为等电子体的分子有N2O和________(填化学式),写出CN22-的电子式___________。
②CaCN2与水反应生成CaCO3和NH3两种物质,则1mol CaCN2与水反应的过程中,反应物断裂的σ键总数_______________。
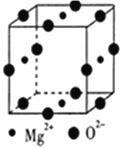
(5) Mg2+与Ni2+、 O2-形成晶体的晶胞结构如图所示(Ni2+未画出),则该晶体的化学式为_________。已知该品胞参数a pm.则该晶体的密度为_________g·cm-3(用a和NA表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】香豆素是广泛存在于植物中的一类芳香化合物,大多具有光敏性,有的还具有抗菌和消炎作用。它的核心结构是芳香内酯A,其分子式为C9H6O2,该芳香内酯A经下列步骤转变为水杨酸和和化合物E。

已知:
请回答下列问题:
(1)A中官能团的名称为_____________;化合物C的结构简式为______________。
(2)B生成C的反应类型为__________________,化合物E的化学名称是_________。
(3)写出A→B的化学方程式__________________________________________________。
(4)化合物D有多种同分异构体,其中一类同分异构体是苯的二元取代物,且水解后生成的产物之一能发生银镜反应。这类同分异构体共有________种;写出其中核磁共振氢谱有5种峰,且其信号强度之比为1 :1 :2 :2 :2的任一种同分异构体的结构简式___________。
 合成
合成
(其他无机原料自选,用反应流程图表示,并注明反应条件)。_________
示例:原料![]() ……产物
……产物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室通常用氧化剂+浓盐酸―→金属氯化物+水+氯气的原理制取少量Cl2。现将一定质量的NaClO放入50 mL 12.00 mol·L-1的浓盐酸中,生成的Cl2在标准状况下的体积为1.12 L。试计算(反应前后溶液的体积变化忽略不计):
(1)反应过程中,被氧化的HCl的物质的量为________ mol。
(2)反应后溶液中HCl的物质的量浓度为______mol·L-1。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某校化学学习小组利用右图装置来制取乙酸乙酯。
I.实验过程:向试管a中加入碎瓷片、3 mL乙醇,然后边振荡试管边慢慢加入2mL 浓硫酸、最后加入2mL乙酸,按右图连接好装置,用酒精灯缓慢加热,将产生的蒸气经导管通到b试管中的液面上。

II.已知化学方程式:CH3COOH+CH3CH2OH![]() CH3COOCH2CH3+H2O。
CH3COOCH2CH3+H2O。
III.查阅资料得知:乙酸乙酯不溶于水,密度比水小,且有香味。
请回答下列问题:
(l)试管a中加人碎瓷片,其作用是__________。
(2)试管b中的溶液是饱和__________溶液。
(3)实验完毕后,将b试管中的液体充分振荡,静置后,溶液分为两层。乙酸乙酯在____层,常用________操作将两层液体分离。
(4)实验中加人乙酸的质量为2.1g,其中60%的乙酸发生酯化反应,则得到乙酸乙酯的质量为_____g (计算结果保留两位小数)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】能正确表示下列反应的离子方程式的是( )
A. Ca(HCO3)2溶液与过量NaOH溶液反应:HCO![]() +Ca2++OH-===CaCO3↓+H2O
+Ca2++OH-===CaCO3↓+H2O
B. 等物质的量的MgCl2、Ba(OH)2和HCl溶液混合:Mg2++2OH-===Mg(OH)2↓
C. 氢氧化钡溶液与稀硫酸混合:Ba2+ + OH- + H++ SO![]() === Ba SO4↓+H2O
=== Ba SO4↓+H2O
D. FeBr2溶液中通入少量的Cl2:2Fe2++Cl2===2Fe3++2Cl-
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com