
| A. | NH4+、Fe2+、Cl-、SO42- | B. | Na+、K+、Cl-、SO42- | ||
| C. | Mg2+、AlO2-、Cl-、SO42- | D. | K+、Ca2+、HCO3-、Cl- |
分析 无色时可排除 Cu2+、Fe2+、Fe3+、MnO4-等有色离子的存在,与铝反应放出氢气的溶液中存在大量氢离子或氢氧根离子,
A.亚铁离子为有色离子,铵根离子、亚铁离子与氢氧根离子反应;
B.四种离子之间不反应,都是无色离子,都不与氢离子、氢氧根离子反应;
C.镁离子与偏铝酸根离子反应,镁离子与氢氧根离子反应,偏铝酸根离子与氢离子反应;
D.碳酸氢根离子与氢离子、氢氧根离子反应.
解答 解:无色溶液可排除 Cu2+、Fe2+、Fe3+、MnO4-等有色离子的存在,与铝反应放出氢气的溶液中存在大量氢离子或氢氧根离子,
A.Fe2+为有色离子,NH4+、Fe2+与氢氧根离子反应,在碱性溶液中不能大量共存,故A错误;
B.Na+、K+、Cl-、SO42-之间不反应,都不与氢离子和氢氧根离子反应,且都是无色离子,在溶液中能够大量共存,故B正确;
C.Mg2+、AlO2-之间发生双水解反应,Mg2+与氢氧根离子反应,AlO2-与氢离子反应,在溶液中不能大量共存,故C错误;
D.HCO3-与氢离子、氢氧根离子反应,在溶液中一定不能大量共存,故D错误;
故选B.
点评 本题考查离子共存的判断,为高考的高频题,属于中等难度的试题,注意明确离子不能大量共存的一般情况:能发生复分解反应的离子之间;能发生氧化还原反应的离子之间等;还应该注意题目所隐含的条件,如:溶液的酸碱性,据此来判断溶液中是否有大量的 H+或OH-;溶液的颜色,如无色时可排除 Cu2+、Fe2+、Fe3+、MnO4-等有色离子的存在;溶液的具体反应条件,如“氧化还原反应”、“加入铝粉产生氢气”;是“可能”共存,还是“一定”共存等.


 品学双优卷系列答案
品学双优卷系列答案 小学期末冲刺100分系列答案
小学期末冲刺100分系列答案 期末复习检测系列答案
期末复习检测系列答案 超能学典单元期中期末专题冲刺100分系列答案
超能学典单元期中期末专题冲刺100分系列答案科目:高中化学 来源: 题型:选择题
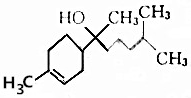
| A. | 分子式为C15H26O | B. | 能和NaHCO3溶液反应生成CO2 | ||
| C. | 不能使酸性高锰酸钾溶液褪色 | D. | 能与乙酸发生取代反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题


查看答案和解析>>
科目:高中化学 来源: 题型:解答题
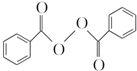 )过去常用作面粉增白剂,但目前已被禁用.合成过氧化苯甲酰的流程图如图:
)过去常用作面粉增白剂,但目前已被禁用.合成过氧化苯甲酰的流程图如图: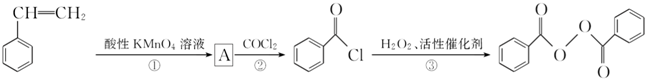
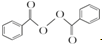 +2H2O→2
+2H2O→2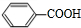 +H2O2;
+H2O2;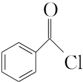 )能与水反应生成苯甲酸,同样也能与乙醇反应,写出其与乙醇反应生成的有机产物的名称苯甲酸乙酯;
)能与水反应生成苯甲酸,同样也能与乙醇反应,写出其与乙醇反应生成的有机产物的名称苯甲酸乙酯;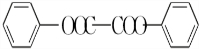 (或
(或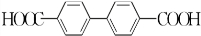 或
或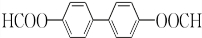 .;
.;查看答案和解析>>
科目:高中化学 来源: 题型:选择题
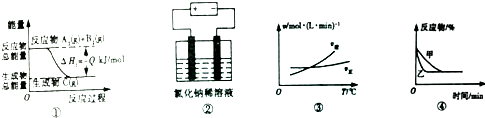
| A. | 图①表示可逆反应A2(g)+B2(g)?C(g)的△H1大于0 | |
| B. | 图②是电解氯化钠稀溶液的电解池,其中阴、阳极产生气体的体积之比一定为1:1 | |
| C. | 图③表示可逆反应A2(g)+3B2(g)?2AB3(g)的△H小于0 | |
| D. | 图④表示压强对可逆反应2A(g)+2B(g)?3C(g)+D(s)的影响,乙曲线对应的压强大 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | MgCl2 的物质的量浓度为0.5mol•L-1 | |
| B. | Cl-的个数为3.01×1023 | |
| C. | Mg2+的物质的量为2mol | |
| D. | Cl-的物质的量浓度为2mol•L-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
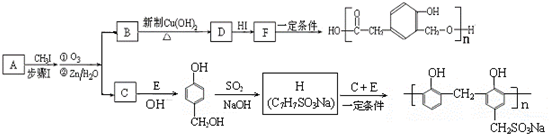
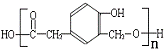 )和某合成鞣剂(
)和某合成鞣剂( 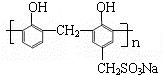 )
)
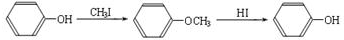
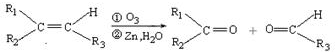 (R1、R2、R3代表烃基)
(R1、R2、R3代表烃基)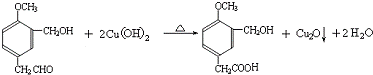 .
. .
.
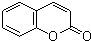 ,写出 X可能的结构简式为
,写出 X可能的结构简式为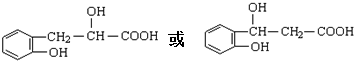 .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com