
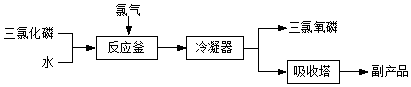
分析 (1)氯化水解法产物是三氯氧磷和盐酸,结合原子守恒分析;
(2)①H3PO3是一种淡黄色晶体,且易溶于水的二元弱酸,酸和碱反应生成盐和水,根据酸碱物质的量的关系进行分析盐;
②H3PO3可以将溶液中的Ag+还原,银离子是氧化剂、H3PO3是还原剂,银由+1价降低为0价,磷元素化合价由+3价升高为+5价,据此书写方程式;
③根据次氯酸钙的氧化性解答;
④根据Ksp[Ca3(PO4)2]=c3(Ca2+)×c2(PO43-)=2.0×10-29计算;
(3)①当滴定达到终点时NH4SCN过量,Fe3+与SCN-反应溶液变红色,半分钟内不褪色,即可确定滴定终点;
②由于AgSCN沉淀的溶解度比AgCl小,可加入硝基苯用力摇动,使AgCl沉淀表面被有机物覆盖,避免在滴加NH4SCN时,将AgCl沉淀转化为AgSCN沉淀;若无此操作,NH4SCN标准液用量偏多.
解答 解:(1)氯化水解法是用三氯化磷、氯气与水反应生成三氯氧磷和盐酸,其化学方程式为:PCl3+H2O+Cl2=POCl3+2HCl,
故答案为:PCl3+H2O+Cl2=POCl3+2HCl;
(2)①酸和碱反应生成盐和水,亚磷酸属于二元酸,含有2个羟基,20mL H3PO3溶液需要同浓度的NaOH溶液40mL,则亚磷酸和氢氧化钠的反应方程式为:H3PO3+2NaOH=Na2HPO3+2H2O,Na2HPO3为亚磷酸的正盐,
故答案为:Na2HPO3;
②H3PO3可以将溶液中的Ag+还原,反应中Ag+→Ag,银元素化合价由+1价降低为0价,降低1价,H3PO3→H3PO4,磷元素化合价由+3价升高为+5价,升高2价,根据得失电子守恒、电荷守恒,离子方程式为:H3PO3+2Ag++H2O=H3PO4+2Ag↓+2H+,
故答案为:H3PO3+2Ag++H2O=H3PO4+2Ag↓+2H+;
③处理废水时,先在其中加入适量漂白粉,将废水中的H3PO3氧化为磷酸,加入生石灰调节pH,使其转化为磷酸钙,发生的反应为:2H3PO3+Ca(ClO)2+2Ca(OH)2=Ca3(PO4)2+2HCl+4H2O,
故答案为:将废水中的H3PO3氧化为H3PO4;
④处理后的废水中c(PO43-)=4×10-7 mol•L-1,Ksp[Ca3(PO4)2]=c3(Ca2+)×c2(PO43-)=c3(Ca2+)×(4.0×10-7)2=2.0×10-29,c(Ca2+)=5×10-6mol•L-1,
故答案为:5×10-6;
(3)①用c mol•L-1NH4SCN溶液滴定过量Ag+至终点,当滴定达到终点时NH4SCN过量,加NH4Fe(SO4)2作指示剂,Fe3+与SCN-反应溶液会变红色,半分钟内不褪色,即可确定滴定终点;
故答案为:b;
②已知:Ksp(AgCl)=3.2×10-10,Ksp(AgSCN)=2×10-12,则AgSCN沉淀的溶解度比AgCl小,可加入硝基苯用力摇动,使AgCl沉淀表面被有机物覆盖,避免在滴加NH4SCN时,将AgCl沉淀转化为AgSCN沉淀,若无此操作,NH4SCN与AgCl反应生成AgSCN沉淀,则滴定时消耗的NH4SCN标准液的体积偏多,即银离子的物质的量偏大,则与氯离子反应的银离子的物质的量偏小,所以测得的氯离子的物质的量偏小,
故答案为:避免在滴加NH4SCN时,将AgCl沉淀转化为AgSCN沉淀;偏小.
点评 本题考查了三氯氧磷的制备方案设计,题目涉及化学方程式的书写、滴定原理的应用、图象分析以及难溶电解质的溶度积常数的应用等,题目综合性较强,难度中等,侧重于考查学生的分析能力和对基础知识的综合应用能力.


 互动英语系列答案
互动英语系列答案 名牌学校分层周周测系列答案
名牌学校分层周周测系列答案 黄冈海淀全程培优测试卷系列答案
黄冈海淀全程培优测试卷系列答案科目:高中化学 来源: 题型:选择题
| A | B | C | |
| 起始浓度(mol/L) | 3.0 | 2.0 | 0 |
| 2s末浓度(mol/L) | 0.6 | 0.4 | 0.8 |
| A. | 3:1:2 | B. | 3:2:1 | C. | 2:1:3 | D. | 9:3:4 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 实验目的 | 选用试剂或条件 | 解释 |
| A | 鉴别SO2和CO2 | 溴水 | 利用SO2的漂白性 |
| B | 鉴别Fe3+和Fe2+ | KSCN | 利用Fe3+的氧化性 |
| C | 鉴别硝酸钾和碳酸钠溶液 | 酚酞 | 碳酸钠溶液显碱性 |
| D | 鉴别食盐和氯化铵 | 加热 | 利用熔点不同 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
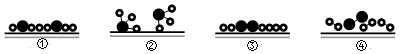
| A. | ④③①② | B. | ③④①② | C. | ③④②① | D. | ④③②① |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 向 NaAlO2溶液中滴加 NaHCO3 溶液,有沉淀和气体生成 | |
| B. | Na、Mg、Fe 等金属在一定条件下与水反应都生成 H2和对应的碱 | |
| C. | 同主族元素的简单阴离子还原性越强,水解程度越大 | |
| D. | 符合通式 CnH2n+2的不同烃不一定互为同系物 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氢气在在氯气中燃烧 | B. | Ba(OH)2•8H2O与NH4Cl反应 | ||
| C. | CaCO3与稀盐酸反应制取CO2 | D. | CaO溶于水 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①② | B. | ③④ | C. | ①②③④ | D. | ①②③ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 自然界中不存在游离态的碳 | B. | 碳的化合物数量众多,分布极广 | ||
| C. | 向空气中排放二氧化碳会形成酸雨 | D. | 煤、石油、天然气属于可再生碳资源 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com