
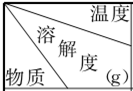
 | 20�� | 60�� | 100�� |
| Na2Cr2O7 | 73.2 | 82.0 | 91.4 |
| K2Cr2O7 | 13.1 | 50.5 | 96.2 |
| NaCl | 36 | 37 | 39 |
| KCl | 34 | 45.5 | 56.7 |
���� ��1���ٸ��ݷ�Ӧ��Ԫ�ػ��ϼ۵����������ƽ���ӷ���ʽ��K2Cr2O7�е�Cr���ϼ���+6�۱�ΪCr3+�е�+3�ۣ����ϼ۱仯3��Cl�Ļ��ϼ���-1�۱�Ϊ0�ۣ����ϼ۱仯1������K2Cr2O7��Cr����ĿΪ2����������2����ԭ�ӣ���K2Cr2O7�ļ�����Ϊ1��Cl-�ļ�����Ϊ6��
�����Cr2O72-�����ʵ���������Cr2O72-��6Fe2+��6FeSO4•7H2O�����FeSO4•7H2O�����ʵ�����������������ɣ�
��2���ٸ���ƽ����ƶ����ж�����Cr2O72-����ɫ������2CrO4-����ɫ�����������ǵ���ɫ�жϣ�
�ڼ������������ᣬƽ�����ƣ�����������Cr2O72-�����K2Cr2O7���ʣ�����Һ���ܽ�����ʶ����ܽ��ʱ���г���������
������BaCrO4��PbCrO4���ֳ�������Һ�д���BaCrO4 +Pb2+=PbCrO4+Ba2+������ܶȻ��������㣮
��� �⣺��1����K2Cr2O7�ڼ��������¿�������Ũ��������������仹ԭ����ΪCr3+��K2Cr2O7�е�Cr���ϼ���+6�۱�ΪCr3+�е�+3�ۣ����ϼ۱仯3��Cl�Ļ��ϼ���-1�۱�Ϊ0�ۣ����ϼ۱仯1������K2Cr2O7��Cr����ĿΪ2����������2����ԭ�ӣ���K2Cr2O7�ļ�����Ϊ1��Cl-�ļ�����Ϊ6����Ӧ�����ӷ���ʽΪCr2O72-+14H++6Cl-$\frac{\underline{\;\;��\;\;}}{\;}$2Cr3++3Cl2��+7H2O��
�ʴ�Ϊ��Cr2O72-+14H++6Cl-$\frac{\underline{\;\;��\;\;}}{\;}$2Cr3++3Cl2��+7H2O��
��10L�÷�ˮ��Һ�к���Cr2O72-�����ʵ���=0.005mol/L��10L=0.050mol������Cr2O72-��6Fe2+��6FeSO4•7H2O��֪FeSO4•7H2O�����ʵ���=6��0.050mol=0.300mol��FeSO4•7H2O������=0.300mol��278g/mol=83.4g��
�ʴ�Ϊ��83.4��
��2������ƽ����ϵ��pH=2������Һ�����ԣ�ƽ�����ƣ����ɵ�Cr2O72-����ɫ��������Һ�ʳ�ɫ���ʴ�Ϊ���ȣ�
�ڼ������������ᣬH2SO4���������H+ʹCr2O72-+H2O?2CrO42-+2H+�����ƶ����Ӷ�������c��Cr2O72-�������K2Cr2O7���ʣ�
����KCl������½��»�����K2Cr2O7��������Ϊ��Һ���ܽ�����ʴ����ܽ��ʱ���г���������K2Cr2O7���ܽ�����¶Ƚ��ͼ�С�ķ��ȴ�ʹ�ø��ֽⷴӦNa2Cr2O7+KCl=K2Cr2O7��+NaCl ���Է������Ӷ�����K2Cr2O7���壻
�ʴ�Ϊ��H2SO4���������H+ʹCr2O72-+H2O?2CrO42-+2H+�����ƶ����Ӷ�������c��Cr2O72-�������K2Cr2O7���ʣ�K2Cr2O7���ܽ�����¶Ƚ��ͼ�С�ķ��ȴ�ʹ�ø��ֽⷴӦNa2Cr2O7+KCl=K2Cr2O7��+NaCl ���Է������Ӷ�����K2Cr2O7���壻
������BaCrO4��PbCrO4���ֳ�������Һ�д���BaCrO4 +Pb2+=PbCrO4+Ba2+��
$\frac{c��P{b}^{2+}��}{c��B{a}^{2+}��}$=$\frac{Ksp��PbCr{O}_{4}��}{Ksp��BaCr{O}_{4}��}$=$\frac{2.8��1{0}^{-13}}{1.2��1{0}^{-10}}$=2.3��10-3��
�ʴ�Ϊ��2.3��10-3��
���� ���⿼�������ܵ���ʵ��ܽ�ƽ�⡢������ԭ��Ӧ�ļ����Լ�ˮ�ⷴӦ��Ӧ�õȣ������ܽ�ƽ�����������㣬���ջ����ǹؼ�����Ŀ�Ѷ��еȣ�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ����þ���۵�ߣ��������ͻ���� | |
| B�� | ̼���ƾ��������ԣ�������θ���кͼ� | |
| C�� | �����������Ư���ԣ�������Ư��ֽ�� | |
| D�� | �Ȼ�����Һ�ܸ�ʴͭ������������ӡˢ��·�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �������������ķ�Ӧ | B�� | �Ȼ�茶�����Ba��OH��2•8H2O�ķ�Ӧ | ||
| C�� | ����صķֽⷴӦ | D�� | �����ˮ�ⷴӦ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 ij��ѧС��Ϊ��֤��SO2��Cl2��Ư���ԣ��������ͼ��ʾ��ʵ��װ�ã�
ij��ѧС��Ϊ��֤��SO2��Cl2��Ư���ԣ��������ͼ��ʾ��ʵ��װ�ã��鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 ��
�� ��
��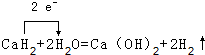 ��
���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �����������ƹ��� | B�� | ��ˮ | ||
| C�� | ͨ�������̼���� | D�� | ���뱥��ʯ��ˮ��Һ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
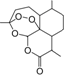 �ҹ�Ů��ѧ�������ϵ����ֳ��ԡ�ʫ��•С�š���������¹����ʳҰ֮����мα����������ѡ������������Ϳ�űҩ---�����أ��ṹ��ͼ����˫�������صĹ��ף��ٻ�2015��ŵ�������������й������ص�����������ǣ�������
�ҹ�Ů��ѧ�������ϵ����ֳ��ԡ�ʫ��•С�š���������¹����ʳҰ֮����мα����������ѡ������������Ϳ�űҩ---�����أ��ṹ��ͼ����˫�������صĹ��ף��ٻ�2015��ŵ�������������й������ص�����������ǣ�������| A�� | ����ʽΪC15H20O5 | B�� | ������C2H5OC2H5 | ||
| C�� | ���������Ѽ������� | D�� | ����NaOH��Һ��Ӧ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ����ú���ʱ�û������ | |
| B�� | ʵ������ͨ������Ʊ����� | |
| C�� | ��ˮ����Ũ��������ϡ���� | |
| D�� | �õ�ȼ�Ļ����Һ������ƿ�ڼ����Ƿ�©�� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com