
【题目】25 C时,H2SO3的pKa1、pKa2(pK= -lgK)分别为1.89、7.20, NH3·H2O的pKb为4.72。常温时,下列指定溶液中粒子物质的量浓度关系正确的是
A.pH=3的H2SO3溶液中,c(HSO3 -) +2c(SO3-)=1 ×10-3 mol·L-1
B.0.1 mol·L-1H2SO3溶液用NaOH溶液滴定至pH =7.20, c( HSO3 ) =2c(SO3- )
C.0.1 mol.L-1H2SO3溶液用氨水滴定至pH=7.0, c(NH4+) =c(HSO3-) +c(SO32- )
D.0.1 mol·L-1NH4HSO3溶液中: c(NH4+ ) >c(H+) >c( NH3·H2O)
【答案】D
【解析】
A. pH=3的H2SO3溶液中,根据电荷守恒可知c(H+)= c(HSO3 -) +2c(SO3-)+ c(OH-)=1 ×10-3 mol·L-1,故A错误;
B. pH =7.20,即溶液中c(H+)=1×10-7.20 mol·L-1,H2SO3的Ka2=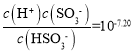 ,则
,则 ,即c( HSO3 ) =c(SO3-),故B错误;
,即c( HSO3 ) =c(SO3-),故B错误;
C. 溶液中存在电荷守恒c(H+)+c(NH4+)= c(HSO3-)+2c(SO3-)+ c(OH-),pH=7.0,则c(H+)=c(OH-),所以c(NH4+)= c(HSO3 -) +2c(SO3-),故C错误;
D. 0.1 mol·L-1NH4HSO3溶液中存在:NH4++H2O NH3·H2O+ H+,水解是微弱的,所以c(NH4+)> c(NH3·H2O);同时存在亚硫酸氢根的水解和电离,亚硫酸氢根的水解平衡常数为![]() ,则亚硫酸氢根的电离程度大于水解程度,所以由于亚硫酸氢根的存在会使溶液显酸性,铵根的水解平衡常数为
,则亚硫酸氢根的电离程度大于水解程度,所以由于亚硫酸氢根的存在会使溶液显酸性,铵根的水解平衡常数为![]() ,小于HSO3-的电离常数,所以c(NH4+ ) >c(H+) >c( NH3·H2O),故D正确;
,小于HSO3-的电离常数,所以c(NH4+ ) >c(H+) >c( NH3·H2O),故D正确;
故答案为D。


 中考解读考点精练系列答案
中考解读考点精练系列答案 各地期末复习特训卷系列答案
各地期末复习特训卷系列答案 小博士期末闯关100分系列答案
小博士期末闯关100分系列答案科目:高中化学 来源: 题型:
【题目】实验室用燃烧法测定某种氨基酸(CxHyOzNm)的分子组成。取Wg该种氨基酸放在纯氧中充分燃烧,生成二氧化碳、水和氮气。按下图所示装置进行实验。

回答下列问题:
(1)实验开始时,首先通入一段时间的氧气,其理由是__________________。
(2)以上装置中需要加热的仪器有_______ (填写字母),操作时应先点燃_____处的酒精灯。
(3)A装置中发生反应的化学方程式是____________________________。
(4)D装置的作用是____________________________。
(5)读取氮气的体积时,应注意①_________________;②_________________。
(6)实验中测得氮气的体积为VmL(标准状况),为确定此氨基酸的分子式,还需要的有关数据有____________________。
A.生成二氧化碳气体的质量
B.生成水的质量
C.通人氧气的体积
D.氨基酸的相对分子质量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学称取9.00g淀粉溶于水,测定淀粉的水解百分率.其程序如下:
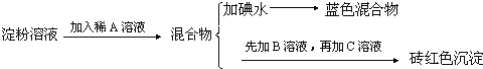
试回答下列问题:
(1)各步加入的试剂为:A_________,B_________,C_________;
(2)加入A溶液而不加入B溶液是否可以_________,其理由是_________;
(3)写出淀粉水解的方程式_________;
(4)当析出1.44g砖红色沉淀时,淀粉水解率是_________;[已知葡萄糖与Cu(OH)2反应的化学方程式为:CH2OH(CHOH)4CHO+2Cu(OH)2![]() CH2OH(CHOH)4COOH+Cu2O↓+2H2O]。
CH2OH(CHOH)4COOH+Cu2O↓+2H2O]。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用电渗析法处理含Na2SO4废水,原理如图所示,两膜中间的Na+和SO42-可通过离子交换膜,而两端隔室中离子不能进入中间隔室。

下列叙述正确的是( )。
A.当电路中通过2 mol电子的电量时,会有2mol的H2生成
B.负极区得到NaOH,正极区得到H2SO4
C.负极反应为2H2O-4e-=O2+4H+,负极区溶液pH增大
D.通电后中间隔室的SO42-离子向负极迁移,正极区溶液pH降低
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】过氧化钙在工农业生产中有广泛的用途。
Ⅰ.过氧化钙制备方法很多。
(1)制备方法一:H2O2溶液与过量的Ca(OH)2悬浊液反应可制备CaO2·8H2O,其化学方程式为______________________________________________________________。
(2)制备方法二:利用反应Ca(s)+O2![]() CaO2(s),在纯氧条件下制取CaO2,实验室模拟装置示意图如下:
CaO2(s),在纯氧条件下制取CaO2,实验室模拟装置示意图如下:
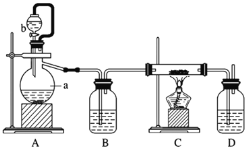
请回答下列问题:
①装置A中反应的化学方程式为________________,仪器a的名称为 ___________。
②装置D中盛有的液体是浓硫酸,其作用一是_________;二是_____________。
Ⅱ.水产运输中常向水中加一定量CaO2·8H2O增加溶氧量(DO),水中溶氧量(DO)是用每升水中溶解氧气的质量来表示,其测定步骤及原理为:
a.固氧:碱性下,O2将Mn2+氧化为MnO(OH)2:2Mn2++O2+4OH=2MnO(OH)2↓;
b.氧化:酸性下,MnO(OH)2将I氧化为I2:MnO(OH)2+2I+4H+=Mn2++I2+3H2O;
c.滴定:用Na2S2O3标准溶液滴定生成的I2:2S2O32-+I2=S4O62-+2I。
某同学向水中加一定量CaO2·8H2O,取此水样100.00mL,按上述方法测定水中溶氧量(DO),消耗0.0100mol·L1 Na2S2O3标准溶液13.50mL。
(1)滴定过程中使用的指示剂是_______________________________;
(2)该水样中的溶解氧量(DO)为__________________mg·L1。
(3)步骤b中加入硫酸溶液反应后,若溶液pH过低,滴定时会产生明显的误差,写出产生此误差的原因________________________(用离子方程式表示,至少写出2个)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化合物DMPG是一种人工合成磷脂,是理想的药用脂质体辅料之一。其合成路线可设计如图所示:
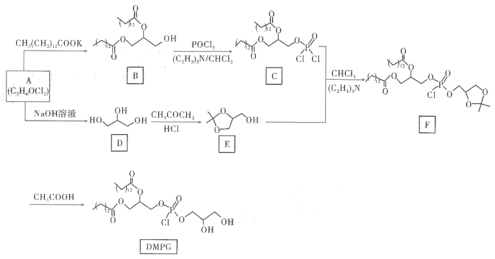
回答下列问题:
(1) D俗称甘油,其化学名称为_______;E的分子式为______,其官能团名称为______。
(2)A生成D的化学方程式为_______,反应类型为_____________。
(3)(C2H5)3N是一种有机碱,可推测其在B生成C、C与E生成F的反应中起到的作用是_____。
(4)X是E的同分异构体,写出符合下列条件的X的结构简式__________、_________。
①能发生银镜反应;②能与金属钠反应生成氢气,且n(X):n( H2) =1:1;③有五种不同化学环境的氢,个数比为4:3:2:2:1。
(5)已知CH3COCH3 (丙酮)与D生成E的反应历程为:
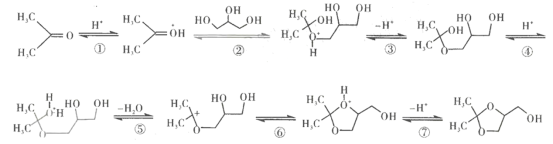
写出CH3COCH3与HOCH2CH2OH反应历程的第④~第⑦步:![]() ____________
____________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知A、B、C、D、E都是周期表中前四周期的元素,它们的核电荷数A<B<C<D<E。其中A、B、C是同一周期的非金属元素。AC2是非极性分子。B、C的氢化物的沸点比它们同族相邻周期元素氢化物的沸点高。E的原子序数为24,ECl3能与B、C的氢化物形成六配位的配合物,且两种配体的物质的量之比为2:1,三个氯离子在外界。根据以上情况,回答下列问题:(答题时,A、B、C、D、E用所对应的元素符号表示)
(1)A、B、C的第一电离能由小到大的顺序为_________;
(2)B的氢化物的分子立体构型是_____;其中心原子采取_______杂化。
(3)写出化合物AC2的电子式为_______;一种由B、C组成的化合物与AC2互为等电子体,其化学式为______。
(4)E的核外电子排布式是______,ECl3形成的配合物的化学式为_____
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】室温下,向20 mL l mol/L的某二元弱酸H2X溶液中逐渐加入NaOH固体(忽略溶液温度及体积变化),测得溶液中的H2X、HX-、X2-的物质的量浓度与溶液pH变化关系如图。下列叙述错误的是( )
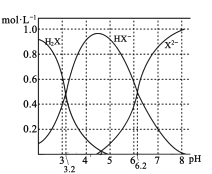
A.NaHX的水溶液呈酸性
B.当加入NaOH固体0.01 mol时,溶液pH= 3.2
C.当加入NaOH固体0.02 mol时,溶液中的离子浓度大小关系为:c(Na+)>c(HX-)>c(H+)>c(X2-)> c(OH-)
D.当加入NaOH固体0.04 mol时,溶液中水的电离程度最大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)铁在元素周期表中的位置为_____,基态铁原子有个未成对电子_____,三价铁离子的电子排布式为_____。
(2)基态Si原子中,电子占据的最高能层符号_____,该能层具有的原子轨道数为_____;铝元素的原子核外共有_____种不同运动状态的电子、_____种不同能级的电子。
(3)处于一定空间运动状态的电子在原子核外出现的概率密度分布可用_____形象化描述。在基态14C原子中,核外存在_____对自旋相反的电子。
(4)中国古代四大发明之一——黑火药,它的爆炸反应为:2KNO3+3C+S![]() K2S+N2↑+3CO2↑,除S外,上述元素的电负性从大到小依次为_____,第一电离能从大到小依次为_____。
K2S+N2↑+3CO2↑,除S外,上述元素的电负性从大到小依次为_____,第一电离能从大到小依次为_____。
(5)有以下物质:①HF,②Cl2,③H2O,④N2,⑤C2H4,⑥CH4,⑦H2,⑧H2O2,⑨HCN(H—C≡N),⑩Ar,既有σ键又有π键的是______;含有由两个原子的s轨道重叠形成的σ键的是______;不存在化学键的是______。
(6)在BF3分子中,F—B—F的键角是______,硼原子的杂化轨道类型为______,BF3和过量NaF作用可生成NaBF4,BF4-的立体构型为______。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com