
【题目】25℃时,向1L c(HA)+c(A-)=0.1mol/L的溶液中滴加盐酸或NaOH溶液,溶液中的H+、OH-、A-及HA的浓度的对数值(lgc)与pH的关系如图所示(不考虑溶液温度变化),下列说法正确的是

A.a表示lgc(A-)与pH的关系曲线
B.K(HA)的数量级为10-5
C.P点溶液中n(Na+)+ n(H+)=0.1mol
D.滴加盐酸或NaOH溶液的过程中c(HA)·c(OH-)均增大
【答案】BC
【解析】
根据图像分析,微粒浓度的对数越大离子浓度越大,随着pH的增大,溶液碱性增强,酸性减弱,则氢离子浓度逐渐减小,氢氧根离子浓度逐渐增大;c的浓度对数值在减小,为c(H+)浓度变化曲线;d的浓度对数值在增大,为c(OH-)浓度变化曲线;pH小于4.75时,a的浓度对数值不变,pH越大,a的浓度对数值减小,应该是c(HA)的变化曲线;b的浓度对数值随pH的增大而增大,b为c(A-)变化曲线;
A. 根据上述分析a表示lg c(HA)与pH的关系曲线,故A错误;
B.K(HA)的表达式为K(HA)=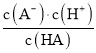 ,pH=4.75时,c(HA)=c(A-),K(HA)=
,pH=4.75时,c(HA)=c(A-),K(HA)=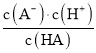 =10-4.75≈1.78×10-5,数量级为10-5,故B正确;
=10-4.75≈1.78×10-5,数量级为10-5,故B正确;
C.P点时,c(OH-)=c(HA),P点的电荷守恒式为c(H+)+ c(Na+)= c(A-) +c(OH-),变式为 c(H+)+ c(Na+)=c(A-)+c(HA),根据题中信息,1Lc(HA)+c(A-)=0.1mol/L的溶液中,n(HA)+n(A-)=0.1mol/L×1L=0.1mol,则溶液中n(Na+)+ n(H+)=0.1mol,故C正确;
D. 滴加盐酸或NaOH溶液的过程中,K(HA)= 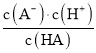 ,c(H+)=
,c(H+)=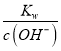 , K(HA)=
, K(HA)= ,K(HA)、Kw只受温度影响,温度不变,平衡常数不变,滴加盐酸,c(A-)在减小,c(OH-)c(HA)在减小,故D错误;
,K(HA)、Kw只受温度影响,温度不变,平衡常数不变,滴加盐酸,c(A-)在减小,c(OH-)c(HA)在减小,故D错误;
答案选BC。


科目:高中化学 来源: 题型:
【题目】某烷烃的结构简式是CH3CH2CH(CH2CH3)CH3,它的正确命名是
A. 2-乙基丁烷 B. 3-乙基丁烷
C. 3-甲基戊烷 D. 2,2-二甲基丁烷
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】今有氧、镁、铝、硫、铬5种元素,试回答下列问题
(1)镁晶体堆积方式为___堆积(选填:“简单立方”、“体心立方”、“面心立方”、“六方”);
(2)用“>”、“<”填写下表
第一电离能 | 电负性 | 晶格能 | 沸点 |
Mg___Al | O___S | MgO___MgS | H2O___H2S |
(3)基态铬原子外围电子轨道表示式为___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期元素a、b、c、d的原子序数依次增大。其中A为d元素组成的单质;甲、乙、丙、丁、戊为上述四种元素组成的二元或三元化合物,常温下乙为液体。下列说法正确的是

A.简单离子半径:c >b
B.反应①为吸热反应
C.②在常温下反应时,氧化剂与还原剂物质的量之比为1:1
D.b、d分别与a形成的化合物中,化学键类型一定完全相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2019年诺贝尔化学奖授予在开发锂离子电池方面做出卓越贡献的三位化学家。锂离子二次电池正极铝钴膜主要含有LiCoO2、A1等,处理该废料的一种工艺如下图所示,下列说法正确的是
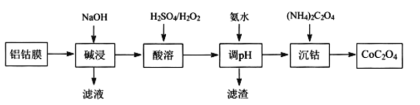
A.酸溶时H2O2做氧化剂,且温度不宜过高
B.加氨水调pH的目的是除铝
C.沉钴的离子方程式为:Co2++C2O42-=CoC2O4↓
D.在空气中加热4.41gCoC2O4得到钴的氧化物2.41g,则该氧化物的化学式为Co3O4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硝酸银是一种无色晶体,易溶于水。用于照相乳剂、镀银、制镜、印刷、医药、染毛发等,也用于电子工业。硝酸银不稳定,易发生如下反应:
①2AgNO3(s)=2Ag(s)+ 2NO2(g)+O2(g) △H1>0
②2NO2(g) ![]() N2O4(g) △H2<0
N2O4(g) △H2<0
(1)实验室配制硝酸银溶液的方法是:将一定量硝酸银固体溶于浓硝酸中,加水稀释至指定体积。“硝酸”的作用是___________________。
(2)2AgNO3(s) =2Ag(s)+N2O4(g)+O2(g) △H=______________ (用含△H1、△H2的式子表示)。
(3)温度T1时,在0.5L的恒容密闭容器中投入3.4 g AgNO3(s)并完全分解测得混合气体的总物质的量(n)与时间(t)的关系如图所示。

①下列情况能说明体系达到平衡状态的是_________(填字母)
a.固体质量不再改变 b.O2的浓度不再改变
c.NO2的体积分数不再改变 d.混合气体的密度不再改变
②若达到平衡时,混合气体的总压强p=0. 3MPa。反应开始到
10min内N2O4的平均反应速率为___________ MPa·min-1。在该温度下2NO2(g)![]() N2O4(g)的平衡常数Kp=___________(MPa)-1(结果保留2位小数)。
N2O4(g)的平衡常数Kp=___________(MPa)-1(结果保留2位小数)。
[提示:用平衡时各组分分压替代浓度计算的平衡常数叫压强平衡常数(Kp),组分的分压(P1) =平衡时总压(p)×该组分的体积分数(![]() )]
)]
③实验测得:υ正=υ(NO2)消耗=k正c2(NO2),υ逆=2υ(N2O4) 消耗=k逆c(N2O4),k正、k逆为速率常数只受温度影响。则化学平衡常数K与速率常数k正、k逆的数学关系是K=___________。若将容器的温度改变为T2时其k正=k逆,则T1______T2(填“>”、“<”或“=")
(4)NO与O2反应生成NO2的反应历程为:第一步NO+NO![]() N2O2 (快速平衡)
N2O2 (快速平衡)
第二步N2O2+O2=2NO2 (慢反应),下列叙述正确的是___________(填标号)。
A. υ(第一步的正反应) <υ(第二步的反应) B.总反应快慢由第二步决定
C. 第二步的活化能比第一步的高 D.第二步中N2O2与O2的碰撞100%有效
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】“臭苏打”是硫化钠的俗名,又称臭碱,黄碱,硫化碱,具有臭味,硫化钠溶解于冷水,极易溶于热水,微溶于醇,是重要的化工产品。
(1)硫化钠水溶液具有臭味是S2-水解产生H2S造成的,用离子方程式解释_____________。
(2)Na2S具有较强的还原性,其水溶液在空气中会缓慢地氧化成硫代硫酸钠,写出化学方程式__________________________________。
(3)某学习小组设计实验探究金属硫化物的性质。
Ⅰ.探究Na2S的还原性
甲同学取少量硫化钠溶液于试管,滴加2滴酚酞溶液,再滴加溴水溶液,观察到溶液颜色变浅。
①酚酞的作用是____________;写出该实验的离子方程式____________________
②乙同学认为甲方案不严密。他设计方案:取少量硫化钠溶液于试管,滴加适量苯,再用长滴管加入溴水。加入“苯”的目的是_________________________
Ⅱ.探究氧化还原反应和沉淀反应的竞争
丙同学设计以下两组实验:
实验1、①在10 mL 2 mol·L-1FeCl3溶液中滴加2 mL 1 mol·L-1Na2S溶液,观察到有浅黄色沉淀生成,溶液黄色变浅。
②在10mL 2 mol·L-1Na2S溶液中滴加2mL1 mol·L-1FeCl3溶液。观察到先产生浅黄色固体,随后生成黑色固体,溶液黄色变无色。
实验2、在2 mol·L-1Na2S溶液中滴加少量AgNO3溶液,立即产生大量黑色沉淀,没有浅黄色沉淀。
实验1 中产生的浅黄色固体是_______(填化学式)。写出实验1 ②中产生黑色沉淀的离子方程式_____________;已知:氧化性有Ag+>Fe3+,实验2中,发生复分解反应,未发生氧化还原反应。
实验结论:若某一溶液中同时存在氧化还原反应和沉淀反应,则_________(填“氧化还原”或“生成更难溶物质”)反应将优先进行。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对于可逆反应N2(g)+3H2(g) ![]() 2NH3(g) △H<0,下列研究目的和示意图相符的是( )
2NH3(g) △H<0,下列研究目的和示意图相符的是( )
A | B | C | D | |
研究目的 | 压强对反应的影响 (p2>p1) | 温度对反应的影响 | 平衡体系中增加N2的浓度对反应的影响 | 催化剂对反应的影响 |
示意图 |
|
|
|
|
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示的C/Na4Fe(CN)6--钠离子电池是一种新型电池。下列有关说法正确的是
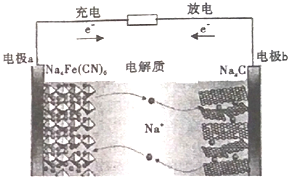
A. 电极a在放电时做正极,充电时做阴极
B. 放电时,电极b上的电极反应为:NaxC-e-=Na++Nax-1C
C. 电池工作时,Na+向电板b移动
D. 该电池通过Na+的定向移动产生电流,不发生氧化还原反应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com