
����Ŀ����ҵ�ϳ�ͨ�����·ֽ�FeSO4�ķ����Ʊ�Fe2O3,�仯ѧ����ʽΪ��2FeSO4![]() Fe2O3+ SO2��+SO3��Ϊ����FeSO4���·ֽ�IJ�������������ʵ����
Fe2O3+ SO2��+SO3��Ϊ����FeSO4���·ֽ�IJ�������������ʵ����
��1��ȡ�����ֽ�õ��Ĺ������ϡ�����ܽ⣬Ϊ������Һ���Ƿ���Fe3+�������Լ���ҩƷ����������� ������ţ���������Լ���ɹ۲������Ϊ ��
A��ϡ���� B������ C��KSCN��Һ D���Ȼ�ͭ��Һ
��2�������·ֽ����������ͨ����ͼ��ʾװ���У��Լ������������ɷ֡�
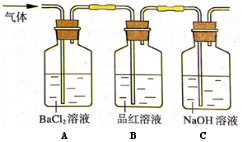
��ش��������⣺
������װ��A�У��۲쵽�а�ɫ�������ɣ���ó���Ϊ �������� ������ڡ�
��װ��C�е�NaOH��Һ�������� ��
���𰸡���1��C����Һ��Ѫ��ɫ��2��BaSO4 ��SO3
��3������SO2���壬��ֹ�ݳ���ɻ�����Ⱦ
��������
�����������1��Fe3����KSCN��Һ��Ѫ��ɫ�����Լ���Fe3������ʵ��Լ���KSCN��Һ����ѡC,����Ϊ��Һ��Ѫ��ɫ����2����װ��A�����۲쵽�а�ɫ�������ɣ���ΪSO2��BaCl2����Ӧ��ֻ����SO3�������ķ�ӦΪSO3+H2O =H2SO4 ��H2SO4+BaCl2 =BaSO4��+2HCl�����Ըó���ΪBaSO4 ����SO3������ڡ�(3)װ��C��NaOH��Һ������������SO2���壬��ֹ�ݳ���ɻ�����Ⱦ��


 ���б�ˢ��ϵ�д�
���б�ˢ��ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪��O2��g��+2H2��g��=2H2O��g����H=��483.6kJmol��1
C��s��ʯī��+O2��g��=CO2��g����H=��393.5kJmol��1
CO2��g��+C��s��ʯī��=2CO��g����H=+172.5kJmol��1
��1����д��CO��ˮ������Ӧ���Ȼ�ѧ����ʽ
��2����һ���Ϊ10L���ܱ������У�ͨ��һ������CO��ˮ��������850��ʱ������Ӧ��������CO��ˮ����Ũ�ȱ仯��ͼ����0��4min��ƽ����Ӧ����v��CO��= �� ������ʱ��ƽ�ⳣ��K= �� 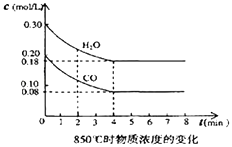
ʱ��/min | CO | H2O | CO2 | H2 |
0 | 0.200 | 0.300 | 0 | 0 |
2 | 0.138 | 0.238 | 0.062 | 0.062 |
3 | c1 | c2 | c3 | c3 |
4 | c1 | c2 | c3 | c3 |
5 | 0.116 | 0.216 | 0.084 | |
6 | 0.096 | 0.266 | 0.104 |
��3��t�棨����850�棩ʱ������ͬ�����з���������Ӧ�������ڸ����ʵ�Ũ�ȱ仯���ұ���
�ٱ���3min��4min֮�䷴Ӧ����״̬��c1��ֵ0.08mol/L ������ڡ�С�ڻ���ڣ���
�ڷ�Ӧ��4min��5min�䣬ƽ�����淽���ƶ������������µ�ԭ��������ĸ��������5min��6min֮����ֵ�����仯�����ܵ�ԭ���� �� ������ĸ��
a������ˮ���� b�������¶� c��ʹ�ô��� d����������Ũ�ȣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��һ�������£�CH4��H2O��g��������Ӧ��CH4��g��+H2O��g��CO��g��+3H2��g������ʼ ![]() =Z���ں�ѹ�£�ƽ��ʱCH4����������գ�CH4����Z��T���¶ȣ��Ĺ�ϵ��ͼ��ʾ������˵��������ǣ� ��
=Z���ں�ѹ�£�ƽ��ʱCH4����������գ�CH4����Z��T���¶ȣ��Ĺ�ϵ��ͼ��ʾ������˵��������ǣ� �� 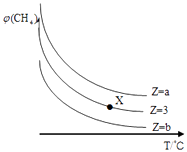
A.�÷�Ӧ���ʱ��H��0
B.ͼ��Z�Ĵ�СΪb��3��a
C.ͼ��X���Ӧ��ƽ�������� ![]() =3
=3
D.�¶Ȳ���ʱ��ͼ��X���Ӧ��ƽ���ڼ�ѹ��գ�CH4������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����ʵ����ͺ���Ԫ�صĻ��ϼ����о��������ʵ�������Ҫ�Ƕȡ��������ͼ���ش���������:
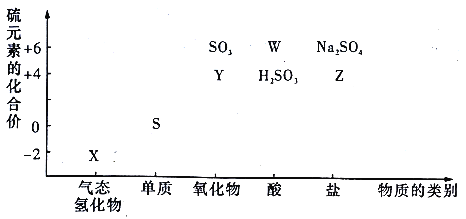
��1������Y���õ��Լ���_________��
��2��W��ϡ��Һ������Ӧ�����ӷ���ʽΪ_________��
��3�����Ʊ�Na2S2O3����������ԭ�Ƕȷ�������������_________(����)��
a.Na2S+S b.Na2SO3+S c.Na2SO3+Na2SO4 d.SO2+Na2SO4
��4����X��Y����Һ��ϣ�����Ϊ_________���÷�Ӧ���������뻹ԭ�������ʵ���֮��Ϊ_________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������ˮ���ܼ����һ�������ǣ� ��
A.�������顢���Ȼ�̼
B.�����Ҵ������Ȼ�̼
C.���������Ҵ������Ȼ�̼
D.���������Ҵ�������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������̬����ɵĻ������0.1mol��ȫȼ�յ�0.16Ħ��CO2��3.6gH2O,����˵����ȷ�ģ� ��
A. һ������ϩB. һ���Ǽ������ϩ
C. һ������ȲD. һ���м���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ù���NaOH�������ʵ���Ũ����Һʱ�����в����ᵼ����ҺŨ��ƫ�͵��ǣ�
A. ���ձ����ܽ�ʱ��������Һ�彦��
B. ��Ʒ�к�������Na2O����
C. ����ƿʹ��ǰ��NaOH��Һ��ϴ
D. ����ʱ��������ƿ�̶���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���Ƚ�1mol������1molһ����̼������˵����ȷ���ǣ� ��
A. ������ͬB. ����������ͬ
C. ԭ��������ͬD. ��ԭ��������ͬ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��14g Cu��Ag�Ͻ�������ijŨ�ȵ����ᷴӦ�����ų���������1.12L O2���������ϣ�ǡ���ܱ�ˮȫ�������������ᣬ��Ͻ���Cu������Ϊ�� ��
A.1.6g
B.3.2g
C.6.4g
D.9.6g
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com