
【题目】非金属元素虽然种类不多,但是在自然界中的丰度却很大,请回答下列问题:
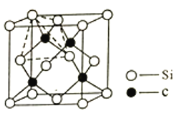
(1)BN(氮化硼,晶胞结构如图)和CO2中的化学键均为共价键,BN的熔点高且硬度大,CO2的晶体干冰却松软且极易升华。由此可以判断:BN可能是______晶体,CO2可能是______晶体,BN 晶体中B原子的杂化轨道类型为______,干冰中C原子的杂化轨道类型为______

(2)分子极性:OF2______H2O,键角:OF2______H2O(填“>””或者“<”)
(3)金刚石和石墨都是碳元素的单质,但石墨晶体熔点比金刚石______,原因是______
(4)单晶硅的结构与金刚石结构相似,若将金刚石晶体中一半的C原子换成Si原子且同种原子不成键,则得如图所示的金刚砂(SiC)结构。在SiC结构中,每个C原子周围距离相等且最近的C原子数目为______,假设C-Si键长为acm,则晶胞密度为______g/cm3。
【答案】原子 分子 sp3 sp < < 高 石墨层内碳碳键的键长比金刚石要短,键能比金刚石大 12 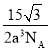
【解析】
本题是对物质结构与性质的考查,涉及晶体类型与性质、杂化方式、分子结构与性质、晶胞计算等,侧重考查学生分析解决问题的能力,分子极性大小及键角的大小判断为易错点、难点,(4)中关键是明确键长与晶胞棱长关系,需要学生具有一定的数学计算能力。
(1)BN由共价键形成的空间网状结构,熔点高、硬度大,属于原子晶体;而干冰松软且极易升华,属于分子晶体;BN 晶体中B原子形成4个B-N键,杂化轨道数目为4,B原子采取sp3杂化,干冰中C原子形成2个σ键,没有孤电子对,杂化轨道数目为2,C原子采取sp杂化,故答案为:原子;分子;sp3;sp;
(2)二者结构相似,均为V形,F与O的电负性相对比较接近,H与O的电负性相差较大,水分子中共用电子对较大地偏向O,所以O-F键的极性较弱,所以整个分子的极性也较弱,水分子中成键电子对之间排斥更大,故水分子中键角也更大,故答案为:<;<;
(3)石墨层内碳碳键的键长比金刚石要短,键能比金刚石大,故石墨晶体熔点比金刚石的高。故答案为:高;石墨层内碳碳键的键长比金刚石要短,键能比金刚石大;
(4)晶胞中每个碳原子与4个Si原子形成正四面体,每个Si原子与周围的4个C原子形成正四面体,晶胞中Si、C的相对位置相同,可以将白色球看作C、黑色球看作Si,互换后以顶点原子研究,与之最近的原子处于面心,每个顶点为8个晶胞共用,每个面心为2个晶胞共用,故每个C原子周围距离相等且最近的C原子数目为![]() ;顶点Si原子与四面体中心C原子连线处于晶胞体对角线上,且距离等于体对角线长度的
;顶点Si原子与四面体中心C原子连线处于晶胞体对角线上,且距离等于体对角线长度的![]() ,而体对角线长度等于晶胞棱长的
,而体对角线长度等于晶胞棱长的![]() 倍,假设C-Si键长为acm,则晶胞棱长=
倍,假设C-Si键长为acm,则晶胞棱长=![]() cm,晶胞中Si原子数目=
cm,晶胞中Si原子数目=![]() 、C原子数目=4,晶胞质量=
、C原子数目=4,晶胞质量=![]() g,晶胞密度=(
g,晶胞密度=(![]() g)÷(
g)÷(![]() cm)3=
cm)3=![]() g/cm3,故答案为:12;
g/cm3,故答案为:12; ![]() 。
。


科目:高中化学 来源: 题型:
【题目】实验室中的下列做法不合理的是( )
①实验室中钠着火时,用泡沫灭火器灭火
②实验室保存氯化亚铁溶液时加入适量铁粉
③用饱和碳酸钠溶液除去二氧化碳气体中的氯化氢
④用水除去一氧化氮气体中的二氧化氮
⑤用浓硫酸干燥硫化氢气体
⑥用氢氧化钠溶液除去氧化铁中的氧化铝
A.①②③B.③④⑤C.①③⑤D.②④⑥
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)常温下将0.01molNH4Cl和0.002molNaOH溶于水配成1L溶液。
①该溶液中除H2O的电离平衡外还存在的平衡体系是___。
②溶液中共有___种不同的微粒。
③这些粒子中浓度为0.01mol·L-1的是___,浓度为0.002mol·L-1的是___。
④物质的量之和为0.01mol的两种微粒是___。
(2)某二元酸(化学式用H2B表示)在水中的电离方程式是H2B=H++HB-;HB-![]() H++B2-,回答下列问题:
H++B2-,回答下列问题:
①已知0.1mol·L-1NaHB溶液的pH=2,则0.1mol·L-1H2B溶液中c(H+)___(填“<”、“>”、“=”)0.11mol·L-1理由是___。
②0.1mol·L-1NaHB溶液中各种离子浓度由大到小的顺序是___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用氯化铁浸出一重铬酸钾(K2Cr2O7)滴定法测定钛精粉试样中单质铁的质量分数[ω(Fe)%],实验步骤如下:
步骤1:称取试样0.100g于250mL洗净的锥形瓶中。
步骤2:加入FeCl3溶液100mL,迅速塞上胶塞,用电磁搅拌器搅拌30min。
步骤3:过滤,用水洗涤锥形瓶和滤渣各3~4次,洗液全部并入滤液中。
步骤4:将滤液稀释至500mL,再移取100mL稀释液于锥形瓶中,加入20mL硫酸和磷酸的混合酸,加0.5%二苯胺磺酸钠指示剂4滴。
步骤5:以K2Cr2O7标准溶液滴定至出现明显紫色为终点。发生的反应:Cr2O72-+6Fe2++14H+=2Cr3++6Fe3++7H2O
步骤6:重复测定两次,数据如下:
第一次 | 第二次 | 第三次 | |
消耗的K2Cr2O7标准溶液体积(mL) | 10.01 | 9.99 | 13.00 |
步骤7:数据处理。
(1)步骤2中加入FeCl3溶液后锥形瓶中发生反应的离子方程式为___,迅速塞上胶塞的原因是___。
(2)步骤3中判断滤纸上残渣已洗净的方法是___。
(3)实验中需用到100mL浓度约为0.01mol·L-1K2Cr2O7标准溶液,配制时用到的玻璃仪器有___;称量K2Cr2O7固体前应先将其烘干至恒重,若未烘干,对测定结果的影响是___(填“偏高”、“偏低”或“无影响”);滴定时,K2Cr2O7溶液应置于___(填仪器名称)中。
(4)利用上表数据,计算出该钛精粉试样中单质铁的质量分数为___(写出必要的计算过程)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D、E是短周期的五种主族元素。A元素的某种原子,其核内没有中子;B元素的基态原子2p轨道上只有一对成对电子;C与B处于同一周期,且原子半径小于B;D与C是同主族元素;E元素的一价阳离子和C元素的阴离子具有相同的电子层结构。根据上述信息回答下列问题:
(1)B元素的原子结构示意图是___,D元素原子的价电子排布式是___,C元素原子核外电子的轨道表示式是___。
(2)A元素分别与C、D两元素形成的化合物的稳定性由强到弱的顺序是___(用化学式表示)。
(3)由B、D、E三种元素组成的某种化合物的水溶液能使pH试纸先变蓝后褪色,写出该化合物的化学式___,用一个离子方程式表明该化合物水溶液使pH试纸先变蓝后褪色的原因___。
查看答案和解析>>
科目:高中化学 来源: 题型:
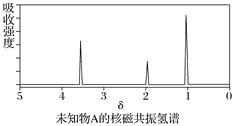
【题目】已知某有机物A的红外光谱和核磁共振氢谱如下图所示,下列说法中错误的有( )
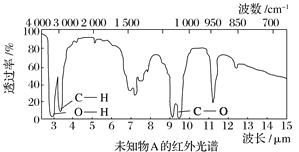
A. 由红外光谱可知,该有机物中至少含有三种不同的化学键
B. 由核磁共振氢谱可知,该有机物分子中有三种不同化学环境的氢原子
C. 若A的化学式为C2H6O,则其结构简式为CH3—O—CH3
D. 仅由其核磁共振氢谱无法得知其分子中的氢原子总数
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】随着我国汽车年销量的大幅增加,给空气环境造成了很大的污染。汽车尾气装置里,气体在催化剂表明吸附与解吸作用的过程如图所示,下列说法正确的是
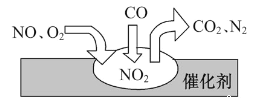
A. 反应中CO为氧化剂,N2为氧化产物
B. 催化转化总反应为2NO+O2+4CO![]() 4CO2+N2
4CO2+N2
C. NO和O2必须在催化剂表面才能反应
D. 汽车尾气的主要污染成分包括CO、NO和N2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于反应与能量的说法正确的是( )
A.Zn(s)+CuSO4(aq)=ZnSO4(aq)+Cu(s) ΔH=-216kJ·mol-1,E反应物<E生成物
B.CaCO3(s)=CaO(s)+CO2(g) ΔH=+178.2kJ·mol-1,E反应物<E生成物
C.2HCl(g)=H2(g)+Cl2(s) ΔH=+92.3kJmol-1,1molHCl在密闭容器中分解后放出92.3kJ的能量
D.将0.5molN2和1.5molH2置于密闭的容器中充分反应后生成NH3(g),放热19.3kJ,其热化学方程式为N2(g)+3H2(g)![]() 2NH3(g) ΔH=-38.6kJ·mol-1
2NH3(g) ΔH=-38.6kJ·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】若用AG表示溶液的酸度,AG的定义为AG=lg![]() 。室温下实验室中用0.01 mol·L-1的氢氧化钠溶液滴定20.00 mL 0.01 mol·L-1醋酸,滴定过程如图所示,下列叙述正确的是
。室温下实验室中用0.01 mol·L-1的氢氧化钠溶液滴定20.00 mL 0.01 mol·L-1醋酸,滴定过程如图所示,下列叙述正确的是
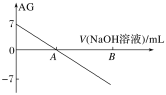
A.室温下,醋酸的电离常数约为10-5
B.A点时加入氢氧化钠溶液的体积为20.00 mL
C.若B点为40 mL,所得溶液中:c(Na+)=c(CH3COO-)+c(CH3COOH)
D.从A到B,水的电离程度逐渐变大
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com