
【题目】某气态烃A,标准状况下的密度为1.25g/L.B和D都是生活中常见的有机物,D能跟碳酸氢钠反应,E有香味.它们之间的转化关系如图1所示: 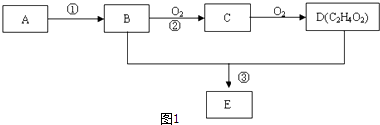
(1)A的电子式为 , D中官能团的名称为 .
(2)以A为原料自身合成高分子化合物的化学方程式为 , 反应类型是 .
(3)反应②在Cu做催化剂的条件下进行,该实验的步骤是将红亮的铜丝置于酒精灯上加热,待铜丝变为黑色时,迅速将其插入到装有B的试管中(如图2所示).观察到的现象是 , 重复操作2﹣3次.写出过程②反应方程式 . 
(4)B、D在浓硫酸的作用下实现反应③,实验装置如图3所示: 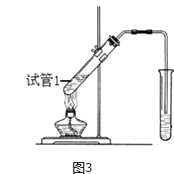
①试管1中实现反应③的化学方程式为 ,
②反应开始时用酒精灯对试管小火加热的原因是: . (已知乙酸乙酯的沸点为77℃;乙醇的沸点为78.5℃;乙酸的沸点为117.9℃)
【答案】
(1)![]() ;羧基
;羧基
(2)![]() ;加聚反应
;加聚反应
(3)铜丝由黑色变红色,产生刺激性气味;CH3CH2OH+CuO ![]() Cu+CH3CHO+H2O
Cu+CH3CHO+H2O
(4)![]() ;防止由于温度过高使反应物来不及充分反应而被蒸出,同时防止副产物乙醚等生成
;防止由于温度过高使反应物来不及充分反应而被蒸出,同时防止副产物乙醚等生成
【解析】解:气态烃A在标准状况下的密度是1.25g/L,其摩尔质量=1.25g/L×22.4L/mol=28g/mol,则A为CH2=CH2;B氧化生成C、C氧化生成D,B和D都是生活中常见的有机物,结合D的分子式可知,B为CH3CH2OH,C为CH3CHO,D为CH3COOH,故反应①是乙烯与水发生加成反应生成CH3CH2OH,CH3CH2OH和CH3COOH在浓硫酸作用下发生酯化反应生成E为CH3COOCH2CH3 . (1)A为CH2=CH2 , A的电子式为 ![]() ,D为CH3COOH,D中官能团的名称为羧基, 所以答案是:
,D为CH3COOH,D中官能团的名称为羧基, 所以答案是: ![]() ;羧基;(2)乙烯发生加聚反应生成聚乙烯,反应方程式为:
;羧基;(2)乙烯发生加聚反应生成聚乙烯,反应方程式为: ![]() ,
,
所以答案是: ![]() ;加聚反应;(3)反应②在Cu做催化剂的条件下进行,该实验的步骤是将红亮的铜丝置于酒精灯上加热,待铜丝变为黑色时,迅速将其插入到装有B的试管中(如图2所示),重复操作2﹣3次,观察到的现象是:铜丝由黑色变红色,产生刺激性气味,
;加聚反应;(3)反应②在Cu做催化剂的条件下进行,该实验的步骤是将红亮的铜丝置于酒精灯上加热,待铜丝变为黑色时,迅速将其插入到装有B的试管中(如图2所示),重复操作2﹣3次,观察到的现象是:铜丝由黑色变红色,产生刺激性气味,
过程②反应方程式:CH3CH2OH+CuO ![]() Cu+CH3CHO+H2O,
Cu+CH3CHO+H2O,
所以答案是:铜丝由黑色变红色,产生刺激性气味;CH3CH2OH+CuO ![]() Cu+CH3CHO+H2O;(4)①试管1中实现反应③的化学方程式为:
Cu+CH3CHO+H2O;(4)①试管1中实现反应③的化学方程式为: ![]() ,
,
所以答案是: ![]() ;
;
②加热的目的是加快反应速率,小火加热而不是大火的目的是:防止由于温度过高使反应物来不及充分反应而被蒸出,同时防止副产物乙醚等生成,
所以答案是:防止由于温度过高使反应物来不及充分反应而被蒸出,同时防止副产物乙醚等生成.


科目:高中化学 来源: 题型:
【题目】化学与生活密切相关,学好化学终生有益。如人体正常的血红蛋白中含有Fe2+,若误食NaNO2,则使血红蛋白中Fe2+转化为Fe3+而丧失其生理功能,临床证明服用维生素C可以解毒,这说明维生素C 具有
A. 酸性 B. 碱性 C. 还原性 D. 氧化性
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列分散系最不稳定的是
A. 向NaOH溶液中通入CO2得到的无色溶液
B. 向碘水溶液中滴加四氯化碳充分振荡后,静置后的下层液体
C. 向沸水中滴入饱和的FeCl3溶液得到的红褐色液体
D. 向CuSO4溶液中加入NaOH溶液得到的分散系
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如表为元素周期表的一部分.
碳 | 氮 | Y | |
X | 硫 | Z |
回答下列问题:
(1)Z元素在周期表中的位置为 .
(2)表中元素原子半径最大的是(填元素符号) .
(3)下列事实能说明Y元素的非金属性比S元素的非金属性强的是 . a.Y单质与H2S溶液反应,溶液变浑浊
b.在氧化还原反应中,1molY单质比1molS得电子多
c.Y和S两元素的简单氢化物受热分解,前者的分解温度高
(4)沸点:H2YH2S(填“>”或“=”或“<”),理由是 .
(5)Y2和Y3互为(填“同位素”或“同分异构体”或“同素异形体”).
(6)其中单质Y2可用做如图所示装置(燃料电池)的氧化剂,请写出Y2在酸性电解质溶液中发生的电极反应方程式 . 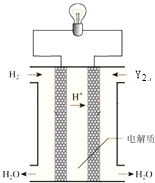
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】元素单质及其化合物有广泛用途,请根据周期表中第三周期元素相关知识回答下列问题:
(1)按原子序数递增的顺序(稀有气体除外),以下说法正确的是 . a.原子半径和离子半径均减小
b.金属性减弱,非金属性增强
c.氧化物对应的水化物碱性减弱,酸性增强d.单质的熔点降低
(2)原子最外层电子数与次外层电子数相同的元素名称为 , 氧化性最弱的简单阳离子是(填离子符号) .
(3)已知:
化合物 | MgO | Al2O3 | MgCl2 | AlCl3 |
类型 | 离子化合物 | 离子化合物 | 离子化合物 | 共价化合物 |
熔点/℃ | 2800 | 2050 | 714 | 191 |
①工业制镁时,电解MgCl2而不电解MgO的原因是
②制铝时,电解Al2O3而不电解AlCl3的原因是; ③写出电解Al2O3反应方程式 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某有机物的结构简式如图,下列叙述不正确的是( ) 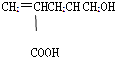
A.1mol该有机物能与足量金属钠反应放出1molH2
B.能与乙醇发生酯化反应
C.1mol该有机物在催化剂作用下最多能与1molH2发生还原反应
D.1mol该有机物能与足量NaHCO3溶液反应放出2 molCO2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某校化学研究性学习小组用浓盐酸与二氧化锰加热反应来制取并收集氯气,装置如下图所示。
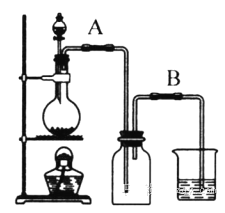
(1) 实验开始前,某学生对装置进行了气密性检查。方法是:连接好装置后,用弹簧夹夹住_____(填“A”或“B”)处橡皮管;向分液漏斗中加水并打开活塞,当加到一定量时,停止加水,静置观察,当观察到分液漏斗中_____时,表明该装置不漏气。
(2) 研究性学生小组的某些同学准备在烧杯中加入下列溶液中的一种来吸收残余氯气,你认为其中错误的是_______(填序号)。
A. 氢氧化钠溶液
B. 碳酸钠溶液
C.浓硫酸
(3)写出浓盐酸与二氧化锰加热反应制取氯气的化学方程式:____________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图是中学化学常见物质间的转化关系图(部分反应条件、产物已省略),G为铝,A 为日常生活中的常见金属。常温下,B、C、E、H、I、J 为气体,C 为黄绿色气体,M 为红褐色胶体。
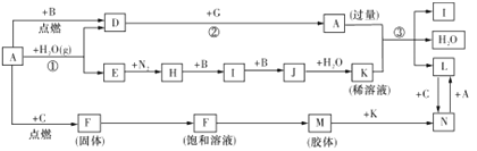
(1)A的元素名称为_________。
(2)D 与G 在高温下反应生成A单质和G的氧化物,请写出其化学方程式:__________。
(3)请写出反应③ 的离子方程式:__________。
(4)请写出H→I的化学方程式:__________。
(5)现将一试管J 气体倒立于水槽中一段时间后,水面上升但不充满;若要使水充满整个试管.应向试管内通入一定量_____(填气体的化学式),此时试管内溶液中溶质的物质的量浓度为_____(气体体积按标准状况计算)(保留两位有效数字)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将镁铝合金溶于100mL稀硝酸中,产生1.12L NO气体(标准状况),向反应后的溶液中加入NaOH溶液,产生沉淀情况如图所示。下列说法不正确的是

A. 可以求出合金中镁的质量 B. 氢氧化钠溶液浓度为3mol/L
C. 可以求出沉淀的最大质量 D. 不能求出硝酸的物质的量浓度
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com