
【题目】(1)已知:肼(N2H4)是一种清洁高效的火箭燃料。 0.25 molN2H4(g)完全燃烧生成氮气和气态水时,放出 133.5 kJ 热量。该反应的热化学方程式:__________。若将上述等量N2H4气体完全燃烧生成氮气和液态水,则放出的热量_____ 133.5 kJ(填“<”、 “>” 或“=”)。
(2)燃料电池是一种高效低污染的新型电池,肼(N2H4)-空气燃料电池(如图)是一种碱性燃料电池。

①电池中通入N2H4 的一极是______极(填“正”或“负”);
②写出该电池正极的电极反应:________。
【答案】 N2H4(g) + O2(g) ==N2(g)+2H2O(g) ΔH=-534 kJ·mol-1 > 负极 O2+2H2O+4e-== 4OH-
【解析】(1)0.25 molN2H4(g)完全燃烧生成氮气和气态水时,放出 133.5 kJ 热量,则1molN2H4(g)完全燃烧生成氮气和气态水时,放出 534kJ 热量,该反应的热化学方程式:N2H4(g) + O2(g) ==N2(g)+2H2O(g) ΔH=-534 kJ·mol-1;若将上述等量N2H4气体完全燃烧生成氮气和液态水,气态水到液态水会放热,则放出的热量 >133.5 kJ;
(2)如图为肼(N2H4)-空气燃料电池,根据上一问中的反应,N2H4发生氧化反应,所以①电池中通入N2H4 的一极是负极;②该电池正极通入氧气,电解质溶液为碱性,故正极的电极反应为:O2+2H2O+4e-== 4OH-。


科目:高中化学 来源: 题型:
【题目】如图是可逆反应:X2+3Y2![]() 2Z2在反应过程中的反应速率(v)与时间(t)的关系曲线,下列叙述正确的是
2Z2在反应过程中的反应速率(v)与时间(t)的关系曲线,下列叙述正确的是

A. t2~t3时,各物质的浓度不再发生变化 B. t2时,反应未达到限度
C. t2~t3时,反应已停止进行 D. t1时,反应只向正反应方向进行
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】元素M、T、U、V、N在元素周期表中的相对位置如图所示,其中M单质在冷暗处与H2剧烈化合并爆炸。回答下列问题:

(1)元素T的原子序数为______,元素U的简单离子结构示意图为_________。
(2)V元素形成的单质中______ (填“存在”或“不存在”)化学键。
(3)M、N两元素分别与氢形成的气态氢化物是甲和乙,其中甲的电子式为______,甲和乙的稳定性强弱顺序为______ (用化学式表示,下同),其水溶液的酸性强弱顺序为______。
(4)写出元素U的单质置换出元素T的单质的离子方程式: ____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在如图所示装置中,石墨电极的电极反应式为 . 如果开始加入的CuSO4足量,则电解一段时间,当电路中转移1.0mol电子时,要使溶液恢复至原浓度,可向其中加入的物质是(填化学式),其质量为g. 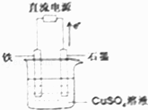
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】淀粉水解的产物(C6H12O6)用硝酸氧化可以制备草酸,装置如图1所示(加热、搅拌和仪器固定装置均已略去):实验过程如图1: 
①将1:1的淀粉水乳液与少许硫酸(98%)加入烧杯中,水浴加热至85℃~90℃,保持30min,然后逐渐将温度降至60℃左右;
②将一定量的淀粉水解液加入三颈烧瓶中;
③控制反应液温度在55~60℃条件下,边搅拌边缓慢滴加一定量含有适量催化剂的混酸(65%HNO3与98%H2SO4的质量比为2:1.5)溶液;
④反应3h左右,冷却,减压过滤后得草酸晶体粗品,再重结晶得草酸晶体.硝酸氧化淀粉水解液过程中可发生下列反应:
C6H12O6+12HNO3→3H2C2O4+9NO2↑+3NO↑+9H2O
C6H12O6+8HNO3→6CO2+8NO↑+10H2O
3H2C2O4+2HNO3→6CO2+2NO↑+4H2O
请回答下列问题:
(1)实验①加入98%硫酸少许的目的是: .
(2)冷凝水的进口是(填a或b);实验中若混酸滴加过快,将导致草酸产量下降,其原因是 .
(3)装置B的作用是 . 为使尾气充分吸收,C中试剂是 .
(4)重结晶时,将草酸晶体粗品经①加热溶解、②趁热过滤、③冷却结晶、④过滤洗涤⑤干燥等实验步骤,得到较纯净的草酸晶体.该过程中可将粗品中溶解度较大的杂质在(填上述步骤序号)时除去;而粗品中溶解度较小的杂质最后留存在(填“滤纸上”或“滤液中”).
(5)将产品在恒温箱内约90℃以下烘干至恒重,得到二水合草酸. 用KMnO4标准溶液滴定,该反应的离子方程式为: , 称取该样品加适量水完全溶解,然后用0.02000molL﹣1的酸性KMnO4溶液滴定至终点(杂质不参与反应),滴定前后滴定管中的液面读数如图2,则消耗KMnO4溶液的体积为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列判断正确的是( )
A. 1LH2O中溶解了0.5molNaCl,则该溶液的物质的量浓度为0.5molL﹣1
B. 从1L1molL﹣1蔗糖(C12H22O11)溶液中取出100mL溶液,其物质的量的浓度仍为1molL﹣1
C. 0.5molL﹣1的NaOH溶液中,含有0.5molNa+
D. 1L H2SO4溶液中含有98g H2SO4,则该溶液的物质的量浓度为98gL﹣1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com