
| A. | 全部 | B. | ②③④ | C. | ①②③ | D. | ①②③⑤ |
分析 ①绿矾中的亚铁离子能被空气氧化为铁离子;
②氢氧化亚铁能被空气氧化为氢氧化铁;
③氯水见光易分解为盐酸;
④亚硫酸钠易被氧化为硫酸钠;
⑤过氧化钠久置于空气中变为碳酸钠.
解答 解:①绿矾中的亚铁离子能被空气氧化为铁离子,颜色会从浅绿色变为淡黄色,会发生颜色变化,故正确;
②氢氧化亚铁能被空气氧化为氢氧化铁,颜色从白色迅速变为灰绿色最终变为红褐色,会发生颜色变化,故正确;
③氯水见光易分解为盐酸,颜色从浅黄绿色变为无色,会发生颜色变化,故正确;
④亚硫酸钠易被氧化为硫酸钠,都是白色固体,颜色无变化,故错误;
⑤过氧化钠久置于空气中变为碳酸钠,颜色从淡黄色变为白色,会发生颜色变化,故正确.
故选D.
点评 本题考查学生物质的化学性质,注意物质颜色的记忆是关键,难度中等.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 重氢、超重氢是制造氢弹的原料 | |
| B. | 氯气可用于农药生产、药物合成 | |
| C. | 钠钾合金可用于中子反应堆作热交换剂 | |
| D. | 碳酸钡可用作检查肠胃的内服药剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 标准状况下,22.4L H2中所含质子数、中子数均为2NA | |
| B. | 32g O2气体和32g O3气体的分子数之比为3:2 | |
| C. | 1L 1mol•L-1的盐酸中所含粒子总数为2NA | |
| D. | 71g氯气与足量铁粉充分反应,转移的电子数为3NA |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
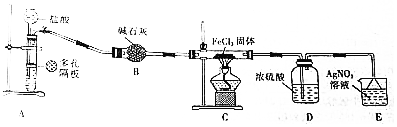
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 10g H2O和10g NH3 | |
| B. | 0.1mol CO和标准状况下2.24L Cl2 | |
| C. | 22g CO2和标准状况下11.2 L N2 | |
| D. | 标准状况下11.2 L O2和11.2 L NH3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 因为Cu可以导电,所以Cu是电解质 | |
| B. | 因为NaHSO4可以电离出H+,所以属于酸 | |
| C. | 武德合金熔点低(70℃),可以做保险丝 | |
| D. | 造成酸雨的主要大气污染物是SO2和CO2 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
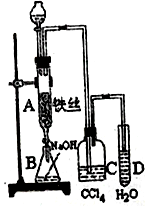 某学生在如图所示的装置中用苯和液溴制取溴苯,请根据下列实验步骤回答有关问题.
某学生在如图所示的装置中用苯和液溴制取溴苯,请根据下列实验步骤回答有关问题. ;
;查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com