
| A. | 在烧瓶中将熟石灰和氯化铵混合,加水调成泥糊状后加热 | |
| B. | 将烧瓶中的浓氨水加热 | |
| C. | 加热试管中的氯化铵固体 | |
| D. | 将分液漏斗中的浓氨水滴入装有浓硫酸的烧瓶中 |
分析 A.将熟石灰和氯化铵混合,加水调成糊状加热,可以制取氨气;
B.加热浓氨水,NH3•H2O分解生成氨气;
C.加热氯化铵生成氨气和氯化氢,氨气和氯化氢遇冷又生成氯化铵,很难制取氨气;
D.利用CaO与H2O剧烈反应,放出大量热,促进NH3.H2O的分解及NH3的挥发逸出.
解答 解:A.熟石灰和氯化铵混合,加水调成泥状后加热可以制取氨气,反应的化学方程式为:2NH4Cl+Ca(OH)2$\frac{\underline{\;\;△\;\;}}{\;}$CaCl2+2NH3↑气体+2H2O,故A错误;
B.加热浓氨水,一水合氨受热分解可以制取氨气,反应的化学方程式为:NH3•H2ONH3↑+H2O,故B错误;
C.氯化铵受热分解成氨气和氯化氢,但氨气和氯化氢一冷却马上又可以化合成氯化铵,该方法很难制氨气,故C正确;
D.利用CaO与H2O剧烈反应,生成Ca(OH)2,放出大量热,促进NH3.H2O的分解及NH3的挥发逸出,又由于Ca(OH)2是强碱,也促进NH3.H2O的分解及NH3的挥发逸出,反应的化学方程式为:NH3.H2O+CaO═NH3↑+Ca(OH)2,故D错误;
故选C.
点评 本题考查氨气的实验室制法,题目难度中等,注意掌握实验室制取氨气的反应原理,C为易错点,注意实验方案的可行性,试题培养了学生的分析能力及化学实验能力.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:多选题
| A. | 32g O2所含的原子数目为NA | |
| B. | 0.5mol H2O所含有的原子数为0.5NA | |
| C. | 1mol H2含有的原子数目为2NA | |
| D. | 0.5NA个氧气分子的物质的量是0.5mol |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
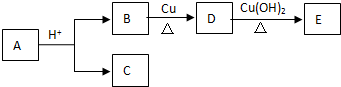
| A. | 符合上述转化关系的有机物A的结构有8种 | |
| B. | C和E一定为同系物 | |
| C. | 1molB完全转化为D转移2mol电子 | |
| D. | D到E发生氧化反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| 选 项 | 操作 | 现象 | 结论 |
| A | 向稀的苯酚水溶液中滴加浓溴水 | 生成白色沉淀 | 产物三溴苯酚不溶于水 |
| B | 淀粉和稀硫酸混合共热后,再加少量新制氢氧化铜悬浊液 | 产生红色沉淀 | 淀粉水解可生成葡萄糖 |
| C | 溴乙烷和氢氧化钠溶液充分反应后,用足量稀硝酸酸化,再加入硝酸银溶液 | 生成淡黄色沉淀 | 溴乙烷中含有溴元素 |
| D | 将溴水加入苯中并充分振荡 | 溴水褪色 | 苯与溴发生了取代反应 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.2mol•(L•s)-1 | B. | 0.2mol•(L•min)-1 | C. | 0.6mol•(L•min)-1 | D. | 0.3mol•(L•min)-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | ① | ② | ||||||
| 3 | ③ | ④ | ⑤ | ⑥ | ⑦ | |||
| 4 | ⑧ | ⑨ |
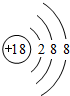 ;
;查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com