
| ʵ����� | 1 | 2 | 3 | 4 |
| �¶�/�� | 35 | 50 | 70 | 95 |
| ��Ʒ��ɫ | ����ɫ | ����ɫ | dz��ɫ | ����ɫ |
| ��Ʒ�м�ʽ̼��ͭ����������/% | 90.9 | 92.7 | x | 92.0 |
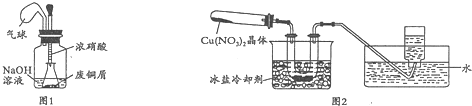
���� I����1��ͭ��Ũ���ᷴӦ��������ͭ������������ˮ��
��2���ٷ�Ӧ���ɵĵ����������Ǵ�����Ⱦ���壬������������Һ���գ���ֹ��Ⱦ��
��ͭ���Ӵ���ˮ��ƽ�⣬���Բ���ֱ�Ӽ��������������ͭ���壬һ���ȡ����Ũ������ȴ�ᾧ�ķ�����������渽�ŵ��������ӣ���Ҫϴ�ӳ�ȥ��
�۸�װ��Ϊ�ܱ���ϵ���ڸ���ϵ�������������������壬���а�ȫ��������������������壬�������ȫ������
��3������ɫ����ΪNO2�����ղ�����ɫ��ĩΪCuO��Cu��NO3��2���ȷֽ���������ͭ������������������
��4������̼������Ӻ����ᷴӦ����ʹ����ʯ��ˮ����ǵ����������̼���ݴ����ʵ����֤��
��5��95��ʱ���Ƶõ���Ʒ��ɫ�����Ŀ���ԭ���Ǻ��к�ɫ������ͭ��
��6����ʽ̼��ͭ��ȫ�ֽ�õ�CuO������Ʒ�м�ʽ̼��ͭ����������Ϊx�����ݼ�ʽ̼��ͭ�ķ���ʽ�����á�������������õ���������
��� �⣺��1��ͭ��Ũ���ᷴӦ��������ͭ������������ˮ����Ӧ���ӷ���ʽΪ��Cu+4H++2NO3-=Cu2++2NO2��+2H2O��
�ʴ�Ϊ��Cu+4H++2NO3-=Cu2++2NO2��+2H2O��
��2���ٷ�Ӧ���ɵĵ����������Ǵ�����Ⱦ���壬������������Һ���գ���ֹ��Ⱦ������װ����NaOH�����������յ������
�ʴ�Ϊ�����յ��������ֹ��Ⱦ������
������ͭ��������Һ�д���ˮ��ƽ�⣬���Դ�����ͭ��Һ�л������ͭ���壬����ֱ�������ᾧ����Ҫͨ������Ũ������ȴ�ᾧ��Ȼ�����ϴ�ӵIJ���������ɣ�
�ʴ�Ϊ����ȴ�ᾧ��
�۸�װ��Ϊ�ܱ���ϵ���ڸ���ϵ�������������������壬ѹǿ��Ȼ�����а�ȫ���������Բ������������������ѹ����ͷ�ιܿ��Ʒ�Ӧ���ʣ�ʹNaOH��Һ��ʱ����NO2����װ���Ǻ�����
�ʴ�Ϊ�����������ܱ���ϵ�����������������壬���а�ȫ���������ߺ�����������ѹ����ͷ�ιܿ��Ʒ�Ӧ���ʣ�ʹNaOH��Һ��ʱ����NO2��
II����3���ٺ���ɫ����ΪNO2��
�ʴ�Ϊ��NO2��
�����ղ�����ɫ��ĩΪCuO��Cu��NO3��2���ȷֽ���������ͭ����������������������ʽΪCu��NO3��2$\frac{\underline{\;\;��\;\;}}{\;}$2CuO+4NO2��+O2����
�ʴ�Ϊ��2Cu��NO3��2$\frac{\underline{\;\;��\;\;}}{\;}$2CuO+4NO2��+O2����
III����4����Һ�п��ܺ���CO32-������CO32-�ķ���Ϊ��ȡ������Һ�����Թ��У���������ϡ���ᣬ������������ͨ�����ʯ��ˮ����Һ����ǣ�˵����̼������ӣ�
�ʴ�Ϊ��ȡ������Һ�����Թ��У���������ϡ���ᣬ������������ͨ�����ʯ��ˮ����Һ����ǣ�˵����̼������ӣ�
��5��CuCO3�ֽ���������ͭ��Cu��OH��2�ֽ���������ͭ���¶Ƚϸ�ʱ��95��ʱ���Ƶõ���Ʒ��ɫ�����Ŀ���ԭ���ǣ����зֽ����ɵĺ�ɫ������ͭ��
�ʴ�Ϊ�����к�ɫ������ͭ��
��6����ʽ̼��ͭ��ȫ�ֽ�õ�CuO������Ʒ�м�ʽ̼��ͭ����������Ϊx�����ݼ�ʽ̼��ͭ�ķ���ʽ��Cu2��OH��2CO3$\frac{\underline{\;\;��\;\;}}{\;}$2CuO+CO2��+H2O�����á�������������ɵã�222��62=2.38x����2.38-1.76�������x=0.933=93.3%��
�ʴ�Ϊ��93.3%��
���� ���⿼�����Ʊ�ʵ�鷽������������ۡ���������ʵ�鷽������ƣ���Ŀ�Ѷ��еȣ�ע�����ճ���Ԫ�ص��ʼ��仯�������ʣ���ȷ��������ʵ�鷽������������۷���������������ѧ���ķ������������������Ӧ����ѧ֪ʶ���ʵ�������������


 ȫ�ſ��䵥Ԫ�����������ܸ�ϰϵ�д�
ȫ�ſ��䵥Ԫ�����������ܸ�ϰϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | Na+��OH-��Cu2+ | B�� | H+��SO42-��HCO3- | C�� | SO42-��Cl-��Na+ | D�� | Ca2+��Cl-��CO32- |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

| ���� |  |
| ����Ҫ�� | Զ�������ĩ���������ࡢ�������ʣ�������������� |
| й©���� | NaOH��NaHSO3��Һ���� |
| ��װ | ��ƿ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
 �����£�H3PO4��NaOH��Һ��Ӧ����ϵ�У��������ֵķֲ�������ƽ��ʱij���ֵ�Ũ��ռ������Ũ��֮�͵ķ�������pH �Ĺ�ϵ��ͼ��ʾ[��֪Ca3��PO4��2������ˮ]�������й�˵������ȷ���ǣ�������
�����£�H3PO4��NaOH��Һ��Ӧ����ϵ�У��������ֵķֲ�������ƽ��ʱij���ֵ�Ũ��ռ������Ũ��֮�͵ķ�������pH �Ĺ�ϵ��ͼ��ʾ[��֪Ca3��PO4��2������ˮ]�������й�˵������ȷ���ǣ�������| A�� | H3PO4��Ka1=10-2.1��HPO42-��ˮ��ƽ�ⳣ��Ϊ10-6.8 | |
| B�� | pH=13ʱ����Һ�и���Ũ�ȴ�С��ϵΪ��c��Na+����c��HPO42-����c��PO43-����c��OH-����c��H+�� | |
| C�� | Na2HPO4 ��Һ�Լ��ԣ�������Һ�м���������CaCl2 ��Һ����Һ�������� | |
| D�� | Ϊ��þ����ܴ���NaH2PO4��pHӦ������4��5.5���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
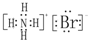 ��
���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ����к͵ζ����յ����ʱ�����ֵζ��ܼ��촦����һ����Һ������ʵ����ƫ�� | |
| B�� | ij��Һ�еμ�HNO3�����������ٵμ�Ba��NO3��2��Һ���ְ�ɫ������˵��ԭ��Һ�к���SO42- | |
| C�� | �Ʊ�����������ʵ���У��ñ���ʳ��ˮ���� | |
| D�� | ���������м�������AlCl3���Եõ������ʵĹ��� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
 ��1����֪�缫���ϣ�����ͭ������ʯī��п�������������Һ��CuCl2��Һ��Fe2��SO4��3��Һ�����ᣮ��Ҫ��ش��������⣺
��1����֪�缫���ϣ�����ͭ������ʯī��п�������������Һ��CuCl2��Һ��Fe2��SO4��3��Һ�����ᣮ��Ҫ��ش��������⣺�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ����ת������һ��ʵ�֣��ֹ�$��_{����}^{Cl_{2}}$SiCl4$��_{����}^{H_{2}}$Si | |
| B�� | Ԫ��C�ĵ���ֻ���ڽ��ʯ��ʯī����ͬ�������� | |
| C�� | Ӳ�ȣ�����裼���ʯ | |
| D�� | �������ý�̿��ԭSiO2��ȡ�ֹ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ���� | B�� | ���� | C�� | ��ȡ | D�� | �ܽ� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com