

分析 (1)根据能量变化图,合成1mol NH3(l)则放出的热量等于(b+c-a)KJ;
(2)上图中的a等于断裂0.5mol氮气和1.5mol氢气所吸收的热量;1mol N2(g) 完全反应生成NH3(g)产生的能量变化为反应物的键能之和-生成物的键能之和;
(3)根据液体氨气转化为气态还要吸热判断.
解答 解:(1)由能量变化图,合成1mol NH3(l)则放出的热量等于(b+c-a)KJ,故答案为:放出;b+c-a;
(2)上图中的a等于断裂0.5mol氮气和1.5mol氢气所吸收的热量,即946×0.5+436×1.5=1127KJ;1mol N2(g) 完全反应则消耗3mol氢气生成2molNH3(g)产生的能量变化为946+436×3-391×6=-92KJ,故答案为:1127;92;
(3)因为合成 NH3则放出热量,所以氨气分解则吸收热量,又液体氨气转化为气态还要吸热,所以液态氨分解吸收的热量比气态氨吸收的热量多,故答案为:吸收;多.
点评 本题考查反应热与能量变化,侧重于考查学生的分析能力和自学能力,题目难度不大,注意把握题给图象信息,答题时注意仔细审题.


科目:高中化学 来源: 题型:选择题
| A. | 最外层只有1个电子的元素一定是金属元素 | |
| B. | 最外层只有2个电子的元素一定是金属元素 | |
| C. | 原子核外各层电子数相等的元素一定是金属元素 | |
| D. | 核电荷数为17的元素的原子的质量数一定是35 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 100 | B. | 90 | C. | 88 | D. | 80 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 科学家最近研究出一种环保、安全的储氢方法,其原理可表示为:NaHCO3+H2═HCOONa+H2O.储氢、释氢过程均无能量变化 | |
| B. | 2SO2(g)+O2(g)═2SO3(g)和4SO2(g)+2O2(g)═4SO3(g)的热效应相同 | |
| C. | 利用太阳能在催化剂参与下分解水制氢是把光能转化为化学能的绿色化学方法 | |
| D. | 过程N2(g)-→2N(g)放出能量 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 纳米TiO2在涂料、光催化、化妆品等领域有着极其广泛的应用,制备纳米TiO2的方法之一是TiCl4水解生成TiO2•xH2O,经过滤、水洗除去其中的Cl-,再烘干、焙烧除去水分得到粉体TiO2.用现代分析仪器测定TiO2粒子的大小.用氧化还原滴定法测定TiO2的质量分数:一定条件下,将TiO2溶解并还原为Ti3+,再以KSCN溶液作指示剂,用NH4Fe(SO4)2标准溶液滴定Ti3+至全部生成Ti4+.
纳米TiO2在涂料、光催化、化妆品等领域有着极其广泛的应用,制备纳米TiO2的方法之一是TiCl4水解生成TiO2•xH2O,经过滤、水洗除去其中的Cl-,再烘干、焙烧除去水分得到粉体TiO2.用现代分析仪器测定TiO2粒子的大小.用氧化还原滴定法测定TiO2的质量分数:一定条件下,将TiO2溶解并还原为Ti3+,再以KSCN溶液作指示剂,用NH4Fe(SO4)2标准溶液滴定Ti3+至全部生成Ti4+.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 同周期元素的原子半径随着核电荷数的增大而增大 | |
| B. | 同主族元素的原子半径随着核电荷数的增大而增大 | |
| C. | 同周期元素的第一电离能随着核电荷数的增大而增大 | |
| D. | 同主族元素的第一电离能随着核电荷数的增大而增大 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
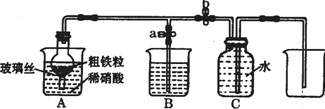 (1)如图所示是实验室中制取气体的一种简易装置.
(1)如图所示是实验室中制取气体的一种简易装置.| 实验步骤 | 操作 | 现象与结论 |
| 第一步 | 取少量液体装于试管,向试管中滴入几滴KSCN溶液 | |
| 第二步 | 若溶液紫色褪去,则说明含有Fe2+,若无明显变化,则说明不含Fe2+ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com