
| A. | NH4+、CH3COO-、Cl-、NO3- | B. | Ba2+、Al3+、HCO3-、NO3- | ||
| C. | Fe2+、H+、S2O32-、NO3- | D. | Na+、Al3+、AlO2-、SO42- |
科目:高中化学 来源: 题型:选择题
| A. | MgCl2与BaO2都是既含有离子键又含有共价键的离子化合物 | |
| B. | 16O2和18O2互为同素异形体 | |
| C. | 氯化氢分子的电子式: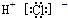 | |
| D. | 质子数为17、中子数为20的氯原子:${\;}_{17}^{37}$Cl |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 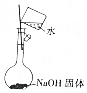 配制0.1mol•L-1的NaOH溶液 | B. | 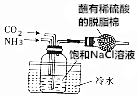 制取NaHCO3 | ||
| C. | 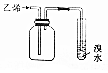 收集乙烯并检验乙烯与溴水的反应 | D. | 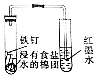 证明铁钉析氢腐蚀 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | SO2通入Ba(NO3)2溶液中有白色沉淀:SO2+Ba2++H2O=BaSO3↓+2H+ | |
| B. | 0.1mol/L氨水的pH为11:NH3•H2O?NH4++OH- | |
| C. | “84”消毒液和“洁厕灵”(主要成分为盐酸)混合使用会产生有毒气体:ClO3-+5Cl-+6H+=3Cl2+3H2O | |
| D. | 氯化铁溶液中滴加氢硫酸溶液:2Fe3++H2S=2Fe2++S+2H+ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 甲烷分子中的4个氢原子都可以被取代,若甲烷分子中的4个氢原子分别被苯基和氯原子取代得到的分子如图所示,对该分子的描述正确的是( )
甲烷分子中的4个氢原子都可以被取代,若甲烷分子中的4个氢原子分别被苯基和氯原子取代得到的分子如图所示,对该分子的描述正确的是( )| A. | 此分子可以产生两种同分异构体 | B. | 所有碳原子都在同一平面内 | ||
| C. | 此分子属于极性分子 | D. | 此物质属芳香烃内物质 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com