
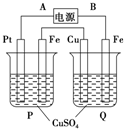
 在如图装置中,通电后可观察到Cu极溶解,则下列说法中不正确的是( )
在如图装置中,通电后可观察到Cu极溶解,则下列说法中不正确的是( )| A、直流电源中,A是正极 |
| B、两池内CuSO4溶液浓度均不改变 |
| C、两池中的铁电极上最初析出物质相同 |
| D、P池内溶液的质量逐渐减小 |


科目:高中化学 来源: 题型:
| A、-(4Q-2M-N)KJ/mol |
| B、-(4Q-M-2N)KJ/mol |
| C、-(2Q-M-2N)KJ/mol |
| D、-(2Q-2M-N)KJ/mol |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Al3+、Mg2+、Cl-、SO42- |
| B、K+、Na+、Cl-、HCO3- |
| C、Fe2+、K+、NO3-、SO42- |
| D、K+、Ba2+、NO3-、Cl- |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、NH4++Al3++2SO42-+2Ba2++5OH-=2BaSO4↓+AlO2-+NH3?H2O+2H2O |
| B、Al3++SO42-+Ba2++3OH-→BaSO4↓+Al(OH)3↓ |
| C、Al3++SO42-+Ba2++4OH-→BaSO4↓+AlO2-+H2O |
| D、2Al3++3SO42-+3Ba2++6OH-=3BaSO4↓+2Al(OH)3↓ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、澄清石灰水与盐酸反应 |
| B、氢氧化钡溶液和稀硫酸反应 |
| C、氢氧化镁和稀硝酸反应 |
| D、氢氧化铁与盐酸反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 室温下,单质A、B、C分别为固体、黄绿色气体、无色气体,在合适的反应条件下,它们可按框图进行反应.又知D溶液为黄色,E溶液是无色的,请回答:
室温下,单质A、B、C分别为固体、黄绿色气体、无色气体,在合适的反应条件下,它们可按框图进行反应.又知D溶液为黄色,E溶液是无色的,请回答:查看答案和解析>>
科目:高中化学 来源: 题型:
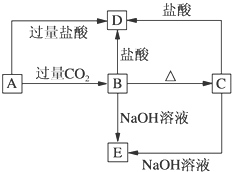 A、B、C、D、E五种化合物,均含有某种常见金属元素,它们的转化关系如图所示,其中A为澄清溶液,B为白色胶状沉淀,C为难熔的白色固体,E则易溶于水,若取A溶液灼烧,焰色反应为浅紫色(透过蓝色钴玻璃).请回答下列问题:
A、B、C、D、E五种化合物,均含有某种常见金属元素,它们的转化关系如图所示,其中A为澄清溶液,B为白色胶状沉淀,C为难熔的白色固体,E则易溶于水,若取A溶液灼烧,焰色反应为浅紫色(透过蓝色钴玻璃).请回答下列问题:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com