
 H、
H、 H、
H、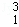 H、H+、H2是()
H、H+、H2是()
A. 氢的五种同位素 B. 五种氢元素
C. 氢的五种同素异形体 D. 氢元素的五种不同粒子
科目:高中化学 来源: 题型:
关于Na2O和 Na2O2的叙述中错误的是()
A. Na2O是白色固体,Na2O2是淡黄色固体
B. 两物质都是碱性氧化物,其中氧元素的化合价都是﹣2价
C. 两者都能和水、二氧化碳、盐酸发生反应
D. Na2O2比Na2O稳定,Na2O在一定条件下可转化为Na2O2
查看答案和解析>>
科目:高中化学 来源: 题型:
设NA表示阿伏加德罗常数的数值,下列叙述中正确的是()
A. 28g以任意比组成的CO与N2混合气体中含有原子数为2NA
B. 22.4L H2中含有氢原子的个数为2NA
C. 在H2O2+Cl2=2HCl+O2反应中,每生成32g氧气,则转移4NA个电子
D. 1L 1 mol/L 的盐酸中有NA 个HCl分子
查看答案和解析>>
科目:高中化学 来源: 题型:
下列溶液中,跟100mL 0.5mol•L ﹣1NaCl溶液所含的Cl﹣物质的量浓度相同的是()
A. 100mL 0.5mol•L﹣1MgCl2溶液
B. 200mL 1mol•L﹣1CaCl2溶液
C. 50mL 1mol•L﹣1NaCl溶液
D. 25mL 0.5mol•L﹣1HCl溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
用20g烧碱配制成500mL其物质的量浓度为1mol/L,从中取出1mL,其物质的量浓度为 mol/L;含溶 质 g.若将这1mL溶液用水稀释到100mL,所得溶液中溶质的物质的量浓度为 mol/L,其中含Na+ .
查看答案和解析>>
科目:高中化学 来源: 题型:
如图是部分短周期元素化合价与原子序数的关系图,下列说法正确的是()
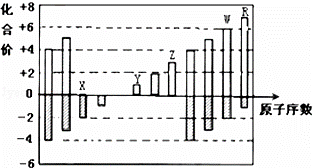
A. 原子半径:Z>Y>X
B. 气态氢化物的稳定性:R<W
C. WX3和水反应形成的化合物是离子化合物
D. Y和Z两者最高价氧化物对应的水化物能相互反应
查看答案和解析>>
科目:高中化学 来源: 题型:
根据反应式:(1)2Fe3++2I﹣=2Fe2++I2,(2)Br2+2Fe2+=2Fe3++2Br﹣,判断下列离子的还原性由强到弱的顺序是()
A. Br﹣、Fe2+、I﹣ B. I﹣、Fe2+、Br﹣ C. Br﹣、I﹣、Fe2+ D. Fe2+、I﹣、Br﹣
查看答案和解析>>
科目:高中化学 来源: 题型:
下表是元素周期表的一部分,表中所列的字母分别代表一种化学元素.
| a |
| ||||||||||||||||
| b | c | d | e | f |
| ||||||||||||
| g | h | i | j | k | l | m |
| ||||||||||
| n | o |
试回答下列问题:
(1)请写出字母O代表的元素符号 ,该元素在周期表中的位置 .
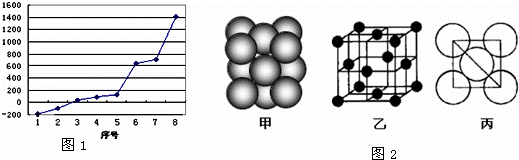
(2)第三周期8种元素按单质熔点高低的顺序如右图,其中序号“8”代表 (填元素符号);其中电负性最大的是 (填如图1中的序号).
(3)由j原子跟c原子以1:1相互交替结合而形成的晶体,晶型与晶体j相同.两者相比熔点更高的是 (填化学式),试从结构角度加以解释: .
(4)k与l形成的化合物kl2的电子式是 ,它在常温下呈液态,形成晶体时,属于 晶体.
(5)i单质晶体中原子的堆积方式如图2(甲)所示,其晶胞特征如图2(乙)所示,原子之间相互位置关系的平面图如图2(丙)所示.若已知i的原子半径为d,NA代表阿伏加德罗常数,i的相对原子质量为M,请回答:
一个晶胞中i原子的数目为 ,该晶体的密度_ (用M、NA、d表示).
(6)a与d构成的阳离子和i的阳离子可与硫酸根形成一种复盐,向该盐的浓溶液中逐滴加入浓氢氧化钡溶液,产生的现象有:①溶液中出现白色沉淀并伴有有刺激性气味气体放出,②沉淀逐渐增多后又逐渐减少直至最终沉淀的量不变.写出沉淀的量不变时发生反应的离子方程式 .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com