
【题目】1999年比利时发生奶粉受二噁英污染事件。二噁英是一类芳香族化合物的多氯代衍生物的总称,结构稳定,难以被自然分解,是公认的最危险的致癌物质之一,2,3,7,8-四氯二苯并二噁英是其中的一种,结构如图,下列说法中不正确的是 ( )
![]()
A. 它的分子式为C12H4O2Cl4B. 它不能发生加成反应
C. 它的一溴取代物有一种D. 此分子中共平面的原子最多有22个
科目:高中化学 来源: 题型:
【题目】如图是中学化学中常用于混合物的分离和提纯的装置。
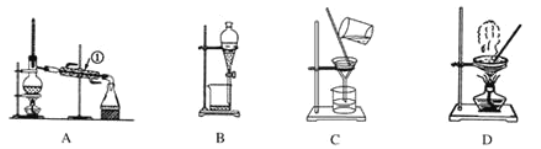
利用以上装置,可以按以下实验方案从海洋动物柄海鞘中提取具有抗肿瘤活性的天然产物。(已知甲苯和甲醇均为有机溶剂,有机物大多能互溶)
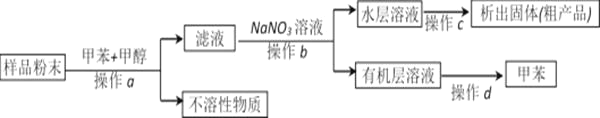
(1)装置A中仪器①的冷却水下进上出的目的是________________________________,使用装置A的操作是__________(填“a”、“b”、“c”或“d”,下同)。
(2)使用装置B的操作是_______(填“a”、“b”、“c”或“d”),使用分液漏斗前应该先_________。
(3)装置C的玻璃棒作用是___________,若所得沉淀不溶于水且需要洗涤,则洗涤的具体操作是________________________________________________________________________________。
(4)使用装置D的操作是_________(填“a”、“b”、“c”或“d”),该操作中玻璃棒的作用是_____________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室欲配制480mL0.2mol·L-1的NaOH溶液。
(1)通过计算可知,应用托盘天平称量_____克NaOH固体。
(2)本实验所需要的玻璃仪器除量筒、胶头滴管、烧杯外还有_____。
(3)从下面选出所需的操作并写出正确的顺序_____(填字母)。
A.洗涤 B.冷却 C.量取 D.称量 E.定容 F.转移溶液 G.稀释 H.溶解
(4)在实验过程中出现如下情况对所配溶液的浓度有何影响(填“偏高”或“偏低”或“无影响”)。
①定容时加蒸馏水不慎超过了刻度_____;
②容量瓶不干燥,有一定的水分_____;
③定容时仰视观察到液面刚好到达刻度线_____。
(5)该NaOH溶液与2.24L氯气(STP)下恰好完全反应,需氢氧化钠溶液_____mL。
(6)用18mol·L-1的硫酸配制100mL1.0 mol·L-1硫酸,实验时应选用的仪器是_____(填编号)。
A.100mL量筒 B.托盘天平 C.玻璃棒 D.50mL容量瓶
E.10mL量筒 F.胶头滴管 G.50mL烧杯 H.100mL容量瓶
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】我国政府为消除碘缺乏病,规定在食盐中必须加入适量的碘酸钾,现实验室需要配制480mL 0.1mol/LKIO3溶液,实际操作步骤有:
(1)需称量碘酸钾的质量为___g。
(2)配制溶液时下列仪器中:
A.锥形瓶 B.托盘天平 C.烧杯 D.胶头滴管 E.药匙 F.量筒
不需要用到的是__(填序号),尚缺的玻璃仪器有___和___(写名称)。
(3)人们常将配制过程简述为以下各步骤:
A.冷却 B.称量 C.洗涤 D.定容 E.溶解 F.摇匀 G.转移 H.装入试剂瓶
其正确的操作顺序应是___(填序号)。
①B E A G C G D F H ②B E G A C G F D H
③B E F G C G D H A ④B E A G C G D H F
(4)在此配制过程中,下列情况会使配制结果偏高的是____ (填序号)。
①转移时未洗涤烧杯和玻璃棒 ②定容时俯视刻度线观察液面
③定容时仰视刻度线观察液面 ④容量瓶用蒸馏水洗干净后未干燥
⑤摇匀后静置,发现液面低于刻度线,再加蒸馏水补至刻度线
(5)检验食盐中是否加碘,可利用如下反应:KIO3+KI+H2SO4─ K2SO4+I2+H2O(未配平)
①配平该方程式,并且用双线桥法表示该方程式电子转移的方向和数目:___。
②该反应中氧化剂和还原剂的物质的量之比为___。
③如果反应中转移0.5mol电子,则生成I2的物质的量为____mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,恒容密闭容器中可逆反应H2(g)+I2(g) ![]() 2HI (g)达到平衡状态的标志是 ( )
2HI (g)达到平衡状态的标志是 ( )
A. 混合气体的压强不再变化
B. 反应速率v(H2) =![]()
C. 混合气体的颜色不再变化
D. c(H2):c (I2):c(HI)= 1:1:2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机物X的蒸气相对氢气的密度为51,X中氧元素的质量分数为31.7%,则能在碱性溶液中发生反应的X的同分异构体有(不考虑立体异构)( )
A. 12种B. 13种C. 14种D. 15种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在标准状况下,由CO和CO2组成的混合气体为6.72 L,质量为12 g。则:
(1)混合气体的密度是_______。(结果保留两位小数)
(2)CO和CO2的物质的量之比是________。
(3)CO的体积分数是________,CO的质量分数是________。
(4)混合气体中所含氧原子的物质的量是_________,所含碳原子的物质的量是_________。
(5)混合气体的平均摩尔质量是_________,对氢气的相对密度是__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列物质的检验,其结论一定正确的是( )
A. 用铂丝蘸取少量某溶液进行焰色反应,火焰呈黄色,该溶液一定是钠盐溶液
B. 向某溶液中加盐酸产生无色气体,该气体能使澄清的石灰水变浑浊,说明该溶液中一定含有CO32-或SO32-
C. 取少量久置的Na2SO3样品于试管中加水溶解,再加盐酸酸化,然后加BaCl2溶液,若加盐酸有气体产生,加BaCl2有白色沉淀产生。说明Na2SO3样品已部分被氧化
D. 将某气体通入品红溶液中,品红溶液褪色,该气体一定是SO2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知过氧化铬(CrO5)的结构式如下图所示,过氧化铬不稳定,溶于水生成过氧铬酸;溶于酸生成铬(III)盐(绿色)并放出氧气,反应方程式为:4CrO5+12H+=4Cr3++7O2+6H2O)。下列有关说法正确的是( )
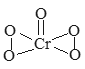
A. CrO5中Cr元素的化合价为+10
B. 过氧化铬中含有极性共价键、非极性共价键和离子键
C. 过氧化铬具有较强的氧化性
D. 上述反应每转移0.2mol电子就能生成2.24LO2
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com