
下列各组中的离子,能在溶液中大量共存的是()
A. Mg2+、H+、Cl﹣、OH﹣ B. Na+、Ba2+、CO32﹣、NO3﹣
C. Na+、H+、Cl﹣、CO32﹣ D. K+、Cu2+、NO3﹣、SO42﹣
 欣语文化快乐暑假沈阳出版社系列答案
欣语文化快乐暑假沈阳出版社系列答案科目:高中化学 来源: 题型:
在一定温度不同压强(P1<P2)下,可逆反应2X(g)⇌2Y(g)+Z(g)中,生成物Z在反应混合物中的体积分数(ψ)与反应时间(t)的关系有以下图示,正确的是( )
|
| A. |
| B. |
| C. |
| D. |
|
查看答案和解析>>
科目:高中化学 来源: 题型:
金属钛性能优越,被誉为继Fe、Al后应用广泛的“第三金属”。
(1)Ti基态原子的电子排布式为
(2)钛能与B、C、 N、 O等非金属元素形成稳定的化合物。电负性:C (填“>”或“<”下同)B;第一电离能: N O。
(3)月球岩石——玄武岩的主要成分为钛酸亚铁(FeTiO3) 。 FeTiO3与80%的硫酸反应可 生成TiOSO4。SO42-的空间构型为 形,其中硫原子采用 杂化.
(4)磷酸钛〔Ti3 (PO4 )4]锂离子电池能量密度大、安全性高。Ti3 (PO4 )4可由TiOSO4与
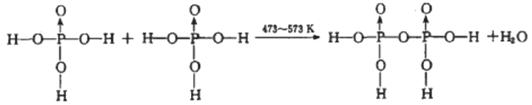 H3PO4反应制得。两分子H3PO4发生脱水生成焦磷酸;
H3PO4反应制得。两分子H3PO4发生脱水生成焦磷酸;
则三分子H3PO4脱去两分子H2O生成三磷酸,其结构式为 ,四分子H3PO4 脱去四分子H2O生成的四偏磷酸属于 元酸。
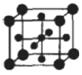
(5)Ti的氧化物和CaO相互作用能形成钛酸盐CaTiO3,CaTiO3的晶体结构如图所示(Ti4+位于立方体的顶点)。该晶体中,Ti4+和周围 个O2-相紧邻.
(6)Fe能形成多种氧化物,其中FeO晶胞结构为NaCI型。晶体中实际上存在空位、错位、杂质原子等缺陷,晶体缺陷对晶体的性质会产生重大影响。由于晶体缺陷,在晶体中Fe和O的个数比发生了变化,变为FexO(x<1)中,若测得某FexO晶体密度为5.71 g·cm-3,晶胞边长为4.28X10-10 m,则FexO中x=_。
查看答案和解析>>
科目:高中化学 来源: 题型:
能正确表示下列化学反应的离子方程式的是()
A. 氢氧化钡溶液与盐酸的反应 2OH﹣+2H+=2H2O
B. 澄清的石灰水与稀盐酸反应 Ca(OH)2+2H+=Ca2++2H2O
C. 铜片插入硝酸银溶液中 Cu+Ag+=Cu2++Ag
D. 碳酸钙溶于稀盐酸中 CaCO3+2H+=Ca2++H2O+CO2↑
查看答案和解析>>
科目:高中化学 来源: 题型:
下列反应中铁元素被还原的是()
A. 2Fe(OH)3 Fe2O3+3H2O B. Fe+CuSO4=Cu+FeSO4
Fe2O3+3H2O B. Fe+CuSO4=Cu+FeSO4
C. Fe(OH)3+3HCl=FeCl3+3H2O D. 2Fe2O3+3C 4Fe+3CO2↑
4Fe+3CO2↑
查看答案和解析>>
科目:高中化学 来源: 题型:
有甲、乙、丙三种试液,在氢氧化钡溶液中加入甲有白色沉淀生成,在沉淀中加入乙,沉淀完全溶解并产生气泡,最后向所得溶液中加入丙又产生白色沉淀,则甲、乙、丙依次是()
A. K2CO3、HCl、CaCl2 B. Na2CO3、HNO3、MgSO4
C. Na2CO3、HCl、Ba(NO3)2 D. H2SO4、Na2CO3、AgNO3
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法不正确的是()
A. 英国科学家道尔顿发现了元素周期律
B. 研究物质性质的基本方法有实验法、观察法、分类法、比较法
C. 化学的特征是认识分子和制造分子
D. 我国科学家合成的结晶牛胰岛素是世界上首次人工合成的具有生物活性的蛋白质
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com