
【题目】化学与生产、生活、社会密切相关,下列说法中不正确的是( )
A.合金材料中可能含有非金属元素
B.铁在潮湿的空气中放置,易发生化学腐蚀而生锈
C.马口铁(镀锡)的表面一旦破损,铁腐蚀加快
D.神舟10号飞船所用太阳能电池板可将光能转换为电能,所用转换材料是单晶硅
 特高级教师点拨系列答案
特高级教师点拨系列答案科目:高中化学 来源: 题型:
【题目】在一定温度下的某容积可变的密闭容器中,建立下列化学平衡:C(s)+H2O(g)![]() CO(g)+H2(g)。可认定上述可逆反应在一定条件下已达到化学平衡状态的是
CO(g)+H2(g)。可认定上述可逆反应在一定条件下已达到化学平衡状态的是
A. 体系的压强不再发生变化
B. 2v正(CO)=v逆(H2O)
C. 生成n molCO的同时生成n mol H2
D. 1 mol H-H键断裂的同时断裂2 mol H-O键
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表是生活生产中常见的物质,表中列出了它们的(主要)成分。
编号 | ① | ② | ③ | ④ | ⑤ | ⑥ | ⑦ |
名称 | 酒精 | 醋酸 | 火碱 | 食盐 | 铜导线 | 亚硫酸酐 | 苏打 |
主要成分 | CH3CH2OH | CH3COOH | NaOH | NaCl | Cu | SO2 | Na2CO3 |
(1)请你对表中①~⑦的主要成分进行分类(填编号):属于电解质的是______,属于非电解质_______。
(2)过量②的水溶液与⑦反应的离子方程式______________________。
(3)某同学用⑤和浓硫酸共热来制备⑥,化学方程式为:Cu+2H2SO4(浓)![]() CuSO4+SO2↑+2H2O
CuSO4+SO2↑+2H2O
①请用单线桥标出电子转移的情况____________;
②浓H2SO4表现出来的性质是:_______;当电子转移0.1mol时,消耗氧化剂的物质的量为_______。
(4)如图表示某同学配制480mL 0.5mol/L 的NaOH溶液的部分操作示意图,其中有错误的是_______,这样操作所配制的溶液比要求的浓度要_________ (填“偏高”、“偏低”、“不影响”)。配制应称取NaOH________g。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用下图装置制取、提纯并收集表中的四种气体(a、b、c表示相应仪器中加入的试剂),其中可行的是( )

气体 | a | b | c | |
A | NO2 | 浓硝酸 | 铜片 | NaOH溶液 |
B | SO2 | 浓硫酸 | Cu | 酸性KMnO4溶液 |
C | NH3 | 浓氨水 | 生石灰 | 碱石灰 |
D | O2 | 双氧水 | MnO2 | 浓硫酸 |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图所示是晶体结构中具有代表性的最小重复单元(晶胞)的排列方式,其对应的化学式正确的是(图中:O-X,●-Y,⊕-Z。C选项中Y原子在面上。)( )
A. X2Y B. XY3
B. XY3 C. XY3Z
C. XY3Z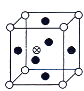 D. XYZ
D. XYZ
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学与生产和生活密切相关。下列说法错误的是
A.铁粉作食品袋内的脱氧剂,起还原作用
B.大量排放二氧化碳可导致温室效应
C.从海水中提取物质都必须通过化学反应才能实现
D.“冬月灶中所烧薪柴之灰,令人以灰淋汁,取碱浣衣”中的“碱”是K2CO3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氧化还原反应是一类重要的反应。
①用铝与软锰矿(主要成分为MnO2)冶炼锰的原理是________________(用化学方程式来表示)。
②MnO2在H2O2分解反应中作催化剂。若将适量MnO2加入酸化的H2O2的溶液中,MnO2溶解产生Mn2+,该反应的离子方程式是____________________。
③某温度下将氯气通入KOH溶液里,反应后得到KCl、KClO、KClO3的混合溶液,经测定ClO-与ClO3-的物质的量浓度之比为1:1,则氯气与KOH反应时,被还原的氯元素和被氧化的氯元素的质量之比为___________。
④12mL 0.lmol/L Na2SO3溶液恰好与4mL 0.lmol/L K2Cr2O7溶液反应,则元素Cr在还原产物中的化合价为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某氯化铁与氯化亚铁的混合物,现要测定其中铁元素的质量分数,实验按以下步骤进行:

Ⅰ.请根据上面流程,回答以下问题:
(1)操作Ⅰ所用到的玻璃仪器除烧杯、玻璃棒外,还必须有________、________(填仪器名称)。
(2)请写出加入溴水发生的离子反应方程式:_______________________________________。
(3)将沉淀物加热,冷却至室温,用天平称量其质量为b1g,再次加热并冷却至室温称量其质量为b2g,若b1-b2=0.3 g,则接下来还应进行的操作是______________________________。若蒸发皿质量是W1g,蒸发皿与加热后固体总质量是W2g,则样品中铁元素的质量分数是____________。
Ⅱ.有同学提出,还可以采用以下方法来测定:

(4)溶解样品改用了硫酸,而不再用盐酸,为什么? ______________________________。
(5)选择的还原剂是否能用铁________(填“是”或“否”),原因是:___________________。
(6)若滴定用掉cmol·L-1KMnO4溶液bmL,则样品中铁元素的质量分数是________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上利用无机矿物资源生产部分材料的流程示意图如下。下列说法正确的是( )

(注:铝土矿中含有A12O3、SiO2、Fe2O3)
A. 在铝土矿制备较高纯度A1的过程中只用到NaOH溶液、CO2气体、冰晶石
B. 石灰石、纯碱、石英、玻璃都属于盐,都能与盐酸反应
C. 在制粗硅时,氧化剂与还原剂的物质的量之比为1∶2
D. 黄铜矿(CuFeS2)与O2反应产生的Cu2S、SO2均是还原产物
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com