
【题目】0.1mol以CnHmCOOH所表示的羧酸加成时需50.8g碘,0.1mol该羧酸完全燃烧时,产生CO2和H2O共3.4mol,该羧酸是( )
A. C15H27COOHB. C15H31COOH
C. C17H31COOHD. C17H33COOH
【答案】C
【解析】
0.1mol加成时需50.8g碘,即n(I2)=![]() =0.2mol,说明分子中含有2个C=C键;
=0.2mol,说明分子中含有2个C=C键;
A.C15H27COOH中含有2个C=C键,0.1mol该羧酸完全燃烧,产生CO2和H2O共(1.6+1.4)mol=3.0mol,故A错误;
B.C15H31COOH为饱和酸,不含C=C键,故B错误;
C.C17H31COOH中含有2个C=C键,0.1mol该羧酸完全燃烧,产生CO2和H2O共(1.8+1.6)mol=3.4mol,故C正确;
D.C17H33COOH中含有1个C=C键,0.1mol该羧酸完全燃烧,产生CO2和H2O共(1.8+1.7)mol=3.5mol,故D错误;
故答案为C。


科目:高中化学 来源: 题型:
【题目】已知有机物之间能发生如下反应:
CH3CHO+CH3CHO![]() CH3CH(0H)CH2CHO
CH3CH(0H)CH2CHO![]() CH3CH=CHCHO;
CH3CH=CHCHO;
![]() +CO
+CO![]()
![]()
下列有机化合物A~H有如图所示的转化关系:
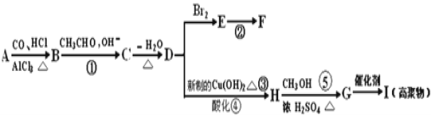
其中,化合物B苯环上的一氯代物只有两种;化合物D的分子式为C10H10O;F的分子式为C10H8O,且所有碳原子在同一平面上。请回答下列问题:
(1)写出下列物质的结构简式:A___________;I_____________
(2)写出E所含官能团的名称____________________
(3)反应①的反应类型为_________;反应③的反应类型为________;反应②的条件为_______________________;化合物F的核磁共振氢谱的谱图上吸收峰的面积之比为_________________。
(3)写出下列反应的化学方程式:
反应③_____________________________________________。
反应⑤___________________________________________________。
(4)写出满足下列条件的F的所有同分异构体(不考虑顺反异构):______。
①遇FeCl3溶液显紫色;
②结构中除苯环外无其他环;
③苯环上只有两种互为对位的取代基.
提示:一个碳原子上不可能同时连有两个碳碳双键或三键。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将足量的CO2不断通入NaOH、Ca(OH)2、NaAlO2的混合溶液中〔已知NaAlO2与CO2反应生成Al(OH)3〕,则生成沉淀的物质的量与通入CO2的体积的关系可表示为( )
A. 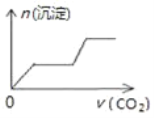 B.
B. 
C. 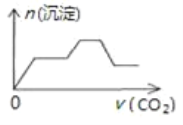 D.
D. 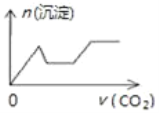
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各物质是中学化学中常见的物质,甲为常见金属单质,乙、丙、丁是非金属单质,其它为化合物,B、D分别为黑色粉末和黑色晶体,G为淡黄色固体,J为生活中常见的调味品,I为红褐色固体,①是实验室制取丁的反应之一,F为棕黄色溶液。各物质间的转化如下图所示,回答下列各问题(部分生成物未列出):

(1)A的电子式:___________________;
(2)写出甲与C反应的化学方程式:________________________________;
(3)在F和E的混合溶液中用___________试剂(填化学式)检验E中阳离子;
(4)整个转换过程中属于氧化还原反应的有___________个;
(5)写出反应③E与G按物质的量之比2:1的反应的离子方程式___________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氮是地球上含量比较丰富的一种元素,氮的化合物在工业生产和生活中有重要的作用。
I.已知298K时,发生反应:N2O4(g) ![]() 2NO2(g)
2NO2(g)
(1)反应达到平衡后,压缩容器的体积,再次达到平衡时混合气体的颜色 ____(填“变深”、“变浅”或“不变”)。
(2)恒容密闭容器中发生上述反应,已知v正=k正·p(N2O4),v逆=k逆·p2(NO2),Kp=___________(用k正、k逆表示)。若初始压强为100kPa,k正=2.8×104s-1,当NO2的体积分数为40%时,v正=__________kPa·s-1。[其中p(N2O4)和p(NO2)分别是N2O4和NO2的分压,分压=p总×气体体积分数,k正、k逆为速率常数]
Ⅱ.在催化剂作用下,H2可以还原NO消除污染,反应为:2NO(g)+2H2(g)![]() N2(g)+2H2O(g) △H=akJ·mol-1
N2(g)+2H2O(g) △H=akJ·mol-1
(3)若每生成7g N2放出166kJ的热量,则a=____。
(4)该反应分两步进行:
①2NO(g)+H2(g)![]() N2(g)+H2O2(g) △H1
N2(g)+H2O2(g) △H1
②H2O2(g)+H2(g)![]() 2H2O(g) △H2
2H2O(g) △H2
已知:i.总反应分多步进行时,较慢的一步决定总反应速率;
III.总反应的速率表达式v=kc2(NO)·c(H2)(k为速率常数,只和温度有关)。由上述信息可知,正反应的活化能较低的是____(填“①”或“②”)。
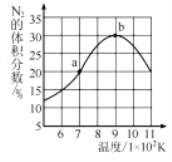
(5)将2molNO和1molH2充入一个恒容的密闭容器中,经相同时间测得N2的体积分数与温度的关系如图所示。低于900K时,N2的体积分数_____(填“是”或“不是”)对应温度下平衡时的体积分数,原因是_____。高于900K时,N2的体积分数降低的可能原因是____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定量的Na2CO3和NaHCO3的均匀混合物分成质量不等的三份,分别与50mL相同浓度的盐酸反应,得到气体的质量与固体混合物的质量关系如下表所示:
组 别 | 1 | 2 | 3 |
固体质量/g | 3.80 | 6.20 | 7.20 |
气体质量/g | 1.76 | 2.64 | 2.64 |
(1)上表中_______组数据表明盐酸参加反应后有剩余,理由是______________。
(2)上表中第2组数据中盐酸____________(填“过量”、“适量”、“不足量”)。
(3)通过计算求Na2CO3和NaHCO3的质量分数各为_________、____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】W、Y、Z为常见短周期元素,三种元素分属不同周期不同主族,且与X能形成如图结构的化合物。已知W、Y、Z的最外层电子数之和等于X的核外电子数,W、X对应的简单离子核外电子排布相同。下列叙述正确的是( )
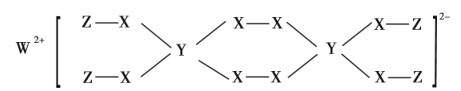
A.对应元素形成的气态氢化物稳定性:Y>X
B.W、X对应的简单离子半径顺序为:X>W
C.Y的氧化物对应水化物为强酸
D.该化合物中各元素均满足8电子稳定结构
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法中正确的是( )
A. NO2、SO2、BF3、NCl3分子中没有一个分子的原子最外层电子都满足8电子稳定结构
B. P4和CH4都是正四面体分子且键角都为109°28′
C. NH4+的电子式为 ,离子呈平面正方形结构
,离子呈平面正方形结构
D. 用CCl4提取碘水中的碘单质
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】磷酸亚铁锂LiFePO4是一种新型汽车锂离子电池的电极材料。某化工厂以铁红、锂辉石LiAl(SiO3)2(含少量Ca2+、Mg2+的盐)、碳粉等原料来生产磷酸亚铁锂。其主要工艺流程如图:

已知:2LiAl(SiO3)2+H2SO4(浓)![]() Li2SO4+Al2O3·4SiO2·H2O↓
Li2SO4+Al2O3·4SiO2·H2O↓
温度/℃ | 20 | 40 | 60 | 80 | |
溶解度(Li2CO3)/g | 1.33 | 1.17 | 1.01 | 0.85 | |
溶解度(Li2SO4)/g | 34.2 | 32.8 | 31.9 | 30.7 |
(1)从滤渣Ⅰ中可分离出Al2O3,如图所示。请写出生成沉淀的离子方程式___。
![]()
(2)滤渣Ⅱ的主要成分是:___(填化学式)。
(3)向滤液Ⅱ中加入饱和Na2CO3溶液,过滤后,用“热水洗涤”的原因是___。
(4)写出在高温下生成磷酸亚铁锂的化学方程式:___。
(5)磷酸亚铁锂电池总反应为:FePO4+Li![]() LiFePO4,电池中的固体电解质可传导Li+。试写出该电池放电时的正极反应:___。若用该电池电解饱和食盐水(电解池电极均为惰性电极),当电解池两极共有4480mL气体(标准状况)产生时,该电池消耗锂的质量为___。
LiFePO4,电池中的固体电解质可传导Li+。试写出该电池放电时的正极反应:___。若用该电池电解饱和食盐水(电解池电极均为惰性电极),当电解池两极共有4480mL气体(标准状况)产生时,该电池消耗锂的质量为___。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com