
| A. | Fe3O4与稀硝酸反应:Fe3O4+8H+═2Fe3++Fe2++4H2O | |
| B. | 盐酸与醋酸钠溶液反应:H++CH3COO-═CH3COOH | |
| C. | 向FeI2溶液中通少量氯气:2Fe2++Cl2═2Fe3++2Cl- | |
| D. | 向NH4Al(SO4)3溶液中加入少量氢氧化钠溶液:NH4++OH-═NH3•H2O |
分析 A.发生氧化还原反应生成硝酸铁、NO和水;
B.反应生成氯化钠和醋酸;
C.少量氯气,只氧化碘离子;
D.少量氢氧化钠,只发生铝离子转化为沉淀的反应.
解答 解:A.Fe3O4与稀硝酸反应的离子反应为3Fe3O4+28H++NO3-=9Fe3++NO↑+14H2O,故A错误;
B.盐酸与醋酸钠溶液反应的离子反应为H++CH3COO-═CH3COOH,故B正确;
C.向FeI2溶液中通少量氯气的离子反应为2I-+Cl2═2Cl-+I2,故C错误;
D.向NH4Al(SO4)3溶液中加入少量氢氧化钠溶液的离子反应为Al3++3OH-═Al(OH)3↓,故D错误;
故选B.
点评 本题考查离子反应方程式书写的正误判断,为高频考点,把握发生的反应及离子反应的书写方法为解答的关键,侧重与量有关的离子反应及氧化还原反应的考查,题目难度不大.


科目:高中化学 来源: 题型:解答题

 .
.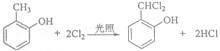 .
. .
. 既可发生酯化反应生成香豆素,可发生加聚反应.该物质加聚产物的结构简式为
既可发生酯化反应生成香豆素,可发生加聚反应.该物质加聚产物的结构简式为 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 合成氨技术的创立开辟了人工固氮的重要途径,其研究来自正确的理论指导,合成氨反应的平衡常数K值和温度的关系如下:
合成氨技术的创立开辟了人工固氮的重要途径,其研究来自正确的理论指导,合成氨反应的平衡常数K值和温度的关系如下:| 温 度(℃) | 360 | 440 | 520 |
| K值 | 0.036 | 0.010 | 0.0038 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 乙烯、油脂、天然橡胶和蛋白质分子中均含有双键 | |
| B. | 相同物质的量的甲基、羟基或氨基所含的电子数目相同 | |
| C. | 常温常压下,3.0g葡萄糖和冰醋酸的混合物中含有的原子总数不为定值 | |
| D. | 利用红外光谱仪记录的红外光谱图可以初步推测有机化合物中官能团的类别 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 溶液 | CH3COONa | Na2CO3 | Na2CO3 | HClO | C6H5ONa |
| PH | 8.8 | 9.7 | 11.6 | 10.3 | 11.3 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
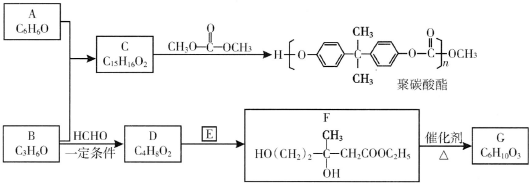
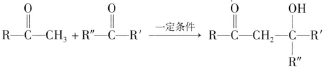 (R、R′、R″为氢原子或烃基)
(R、R′、R″为氢原子或烃基) ,E的分子式是C4H8O2,F生成G的反应类型是取代反应?
,E的分子式是C4H8O2,F生成G的反应类型是取代反应? .G的同分异构体有多种,其中和G具有完全相同环状结构的同分异构体有23种(不包含G,不考虑立体异构).
.G的同分异构体有多种,其中和G具有完全相同环状结构的同分异构体有23种(不包含G,不考虑立体异构).查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 凡AB2型的共价化合物,其中心原子A均采用sp杂化轨道成键 | |
| B. | 25℃时,在Mg(OH)2的悬浊液中加入少量的NH4Cl固体,c(Mg2+)增大 | |
| C. | 反应2A(g)+B(g)═3C(s)+D(g)在一定条件下能自发进行,说明该反应的△H>0 | |
| D. | SO2与SiO2的晶体中,化学键种类和晶体类型均相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
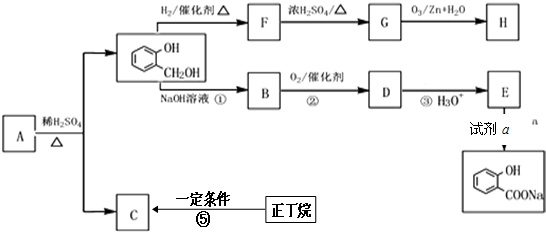
 ,由F到G的反应类型为消去反应.
,由F到G的反应类型为消去反应.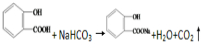 .
.
 的反应是否进行完全,设计一个简单实验加以证明并写出实验操作、现象及结论:取少量反应后的溶液于试管中,加入氯化铁溶液,若溶液变紫色,则反应不完全,反应物有剩余,反之则完全反应.
的反应是否进行完全,设计一个简单实验加以证明并写出实验操作、现象及结论:取少量反应后的溶液于试管中,加入氯化铁溶液,若溶液变紫色,则反应不完全,反应物有剩余,反之则完全反应.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Y一定是氯元素 | |
| B. | R一定是离子化合物 | |
| C. | R中每个原子都达到了8个电子的稳定结构 | |
| D. | 常温下,R可能是液态物质,也可能是固态物质 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com