
【题目】下列分散系属于胶体的是( )
A.豆浆
B.食盐水
C.油水混合物
D.冰水混合物
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】芳香化合物在催化剂催化下与卤代烃发生取代反应称为Friedel-Crafts烷基化反应。某科研小组以苯和氯代叔丁烷[ClC(CH3)3]为反应物,无水AlCl3为催化剂条件下制备叔丁基苯(![]() )。反应如下:
)。反应如下:
![]() 。
。
已知:
(1)AlCl3:熔点:190 C,沸点:180 C,遇水极易潮解并产生白色烟雾,微溶于苯。
(2)苯:M=78g/mol,ρ:0.88g/cm3,沸点:80.1 C,难溶于水,易溶于乙醇。
(3)氯代叔丁烷M=92.5g/mol,ρ:1.84g/cm3,沸点:51.6 C,难溶于水,可溶于苯。
(4)叔丁基苯:M=134g/mol,ρ:0.87g/cm3,沸点:169 C,难溶于水,易溶于苯。
I、如图是实验室制备无水AlCl3的实验装置:
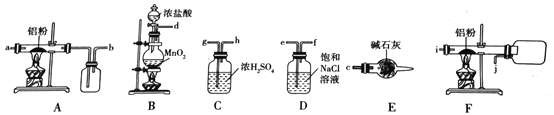
(1)选择合适的装置制备无水AlCl3正确的连接顺序为:_____________________(写导管口标号)。
(2)写出B装置中发生反应的离子方程式:______________。
(3)能否将E装置替换成C装置:______(填“能”或“不能”)理由:__________。
II、实验室制取叔丁基苯装置如图:

在三颈烧瓶中加入50mL的苯和适量的无水AlCl3,由恒压漏斗滴加氯代叔丁烷[ClC(CH3)3]10mL,一定温度下反应一段时间,将反应后的混合物依次用稀盐酸、5%Na2CO3溶液、H2O洗涤分离,在所得产物中加入少量无水MgSO4固体,静置,过滤,蒸馏得叔丁基苯20g。
(4)仪器A的名称为_______,B中试剂是碱石灰,其作用是_____________________,使用恒压漏斗的优点是__________________________。
(5)用H2O洗涤的目的是______________,加无水MgSO4固体的作用是______________。
(6)叔丁基苯的产率为____________。(保留3位有效数字)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某气态烃在标准状况下密度为2.59 g·L-1。
(1)其相对分子质量等于________。
(2)该烃的含碳量为82.8%,则分子中碳、氢原子的个数比是________,分子式是________。
(3)可能的结构简式及名称是______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X,Y均得1个电子达到8e﹣的稳定结构,且X得电子放出的能量大于Y得电子放出的能量,则下列说法不正确的是( )
A.X,Y同主族
B.X原子的半径大于Y原子的半径
C.X的非金属性强于Y的非金属性
D.X﹣的还原性弱于Y﹣的还原性
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某液态烃的球棍模型为: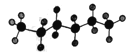 ,有机物R与该烃分子式相同,且结构中有四个甲基。下列有关R的说法中正确的是
,有机物R与该烃分子式相同,且结构中有四个甲基。下列有关R的说法中正确的是
A. R能使溴的四氯化碳溶液褪色 B. R一定是2,2-二甲基丁烷
C. R不溶于水且密度比水大 D. R的一氯代物可能有2种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】近年来,我国的电子工业迅速发展,造成了大量的电路板蚀刻废液的产生和排放。蚀刻液主要有酸性的(HCl-H2O2)、传统的FeCl3型(HCl-FeCl3)等方法.蚀刻废液中含有大量的Cu2+,废液的回收利用可减少铜资源的流失.几种蚀刻废液的常用处理方法如下:
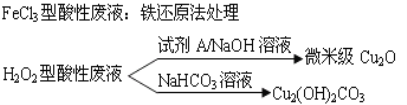
(1)FeCl3型酸性废液用还原法处理是利用Fe和Cl2分别作为还原剂和氧化剂,可回收铜并使蚀刻液再生。发生的主要化学反应有:Fe+Cu2+=Fe2++Cu、Fe+2H+=Fe2++H2↑,还有_______________、__________________.(用离子方程式表示)。
(2)HCl-H2O2型蚀刻液蚀刻过程中发生的化学反应用化学方程式可表示为:__________。
(3)处理H2O2型酸性废液回收Cu2(OH)2CO3的过程中需控制反应的温度,当温度高于80℃时,产品颜色发暗,其原因可能是____________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化合物的化学式为(NH4)2Fe(SO4)2 ,它在水溶液里电离时生成两种阳离子和一种酸根离子
(1)写出硫离子的结构示意图________________;
(2)若向该化合物的水溶液中通入氯气,一种离子很容易被氧化,该离子将变成______;(用离子符号表示)
(3)若向该化合物的水溶液中加入过量一种碱溶液,只能发生一个离子反应,则该反应的离子方程式为__________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】钾、氟及锌的相关化合物用途非常广泛。回答下列问题:
(1)基态锌原子的价电子排布式为___________;K、F、Zn的电负性从大到小的顺序为___________。
(2)Zn与Ca位于同一周期且最外层电子数相等,钙的熔点与沸点均比锌高,其原因是_______________。
(3)OF2分子的几何构型为___________(1分),中心原子的杂化类型为___________。
(4)KOH 与O3反应可得到KO3(臭氧化钾),KO3中除σ键外,还存在___________。
(5)K、F、Zn组成的一种晶体结构如图所示,其晶胞参数为a=0.4058 nm。

①晶胞中Zn2+的配位数为___________个。
②该晶体的密度为___________(列出算式即可,用NA表示阿伏加德罗常数的数值)g·cm-3。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】298K时,在20.0mL0.10mol·L-1氯水中滴入0.10mol·L-1的盐酸,溶液的pH与所加盐酸的体积关系如图所示。己知0.10mol·L-1氨水的电离度为1.32%,下列有关叙述正确的是

A. 该滴定过程应该选择酚酞作为指示剂
B. M点对应的盐酸体积为20.0mL
C. M点处的溶液中c(NH4+)=c(Cl-)=c(H+)=c(OH-)
D. N点处的溶液中pH<12
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com