
【题目】短周期元素X、Y、Z、W的原子序数依次增大,且四种元素分别位于不同的主族,它们的单质常温下均呈气态。X、Y、W处于不同周期,且在一定条件下其单质能发生反应:X2+Y2→甲,X2+W2→乙,已知,甲、乙常温下均为气态,且两者在空气中相遇时可化合成丙。试回答下列问题:
⑴ Y和Z对应的氢化物比较稳定的是:_______________。(填化学式)
⑵ 化合物丙属于_____________晶体(填晶体类型),其水溶液显酸性,用离子方程式表示其原因:_________________________________________。
⑶ X、Z可组成四原子化合物丁,丁中所含的化学键类型为:____________键,请说出化合物丁的一种常见用途:___________________________________ ;
⑷ X、Y组成的液态化合物Y2X4 16 g与足量丁反应生成Y2和液态水,放出QkJ的热量,写出该反应的热化学方程式:______________________________;
Y2X4还可以和Z2构成清洁高效的燃料电池,若电解质溶液为NaOH溶液,则负极的电极反应式为:________________________________________ 。
⑸ 一定条件下,取 3.4 g甲气体置于1 L恒容的容器中,4分钟后,容器内的压强变为原来的1.2倍,且不再变化,该反应中甲气体的转化率为:__________。
【答案】H2O 离子 NH4+ + H2O NH3·H2O + H+ 共价 做生氧剂、杀菌剂、消毒剂、漂白剂等 N2H4(l) + H2O2(l) = N2(g) + 2H2O(l) △H = - 2Q kJ·mol-1 N2H4 - 4e- + 4OH- = N2↑+ 4H2O 20.0 %
【解析】
短周期元素X、Y、Z、W的原子序数依次增大,且四种元素分别位于不同的主族,它们的单质常温下均呈气态,X、Y、W处于不同周期,则X为H元素,由X2+Y2→甲,X2+W2→乙,甲、乙常温下均为气态,且两者在空气中相遇时可化合成丙,则丙为氯化铵,即Y为氮,W为氯,结合⑶ 中X、Z可组成四原子化合物丁,则Z为O元素,丁为H2O2。
(1)Y是N,Z是O,氧元素的非金属性强于氮元素,所以H2O比NH3稳定,故答案为:H2O。
(2)丙为氯化铵,属于离子晶体,是强酸弱碱盐,其水溶液显酸性, 水解的离子方程式为:
NH4+ + H2O NH3·H2O + H+,故答案为:离子;NH4+ + H2O NH3·H2O + H+。
(3)X、Z可组成四原子化合物丁,丁为H2O2,所含的化学键类型为:共价键,双氧水可做生氧剂、杀菌剂、消毒剂、漂白剂等,故答案为:共价键;做生氧剂、杀菌剂、消毒剂、漂白剂等。
(4)液态化合物N2H4 16 g与足量H2O2反应生成N2和液态水,放出QkJ的热量,则1mol N2H4反应放出的热量=QkJ×[(1mol×32g/mol)/16g]=2QkJ,该反应的热化学方程式:N2H4(l) + H2O2(l) = N2(g) + 2H2O(l) △H = - 2Q kJ·mol-1 ;N2H4还可以和O2构成清洁高效的燃料电池,若电解质溶液为NaOH溶液,负极发生氧化反应,N2H4在负极上失去电子,碱性条件下生成氮气和水,负极的电极反应式为N2H4 - 4e- + 4OH- = N2↑+ 4H2O,故答案为:N2H4(l) + H2O2(l) = N2(g) + 2H2O(l) △H = - 2Q kJ·mol-1 ;N2H4 - 4e- + 4OH- = N2↑+ 4H2O。
(5)3.4 g 氨气的物质的量为0.2mol,恒容条件下,气体的物质的量之比等于压强之比,
容器内的压强变为原来的1.2倍,即气体的物质的量变为原来的1.2倍,
2NH3(g) ![]() N2(g)+3H2(g),
N2(g)+3H2(g),
起始(mol) 0.2 0 0
转化(mol) x 0.5x 1.5x
平衡(mol)0.2-x 0.5x 1.5x
(0.2-x+0.5x+1.5x)/ 0.2=1.2,x=0.04mol,所以氨气的转化率为0.04mol/0.2mol×100%=20.0 %,故答案为:20.0 %。


 口算小状元口算速算天天练系列答案
口算小状元口算速算天天练系列答案科目:高中化学 来源: 题型:
【题目】根据SO2通入不同溶液中的实验现象,所得结论错误的是( )
选项 | 溶液 | 现象 | 结论 |
A | H2O2溶液 | 无明显现象 | SO2与H2O2不反应 |
B | H2S溶液 | 产生淡黄色沉淀 | SO2有氧化性 |
C | 酸性KMO4溶液溶液 | 紫色褪去 | SO2有还原性 |
D | 滴有酚酞的NaOH溶液 | 溶液红色褪去 | SO2有酸性氧化物的性质 |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】科学家已获得了极具理论研究意义的N4分子,其结构为正四面体(如图所示),与白磷分子相似,已知断裂1molN—N键吸收193kJ热量,断裂1molN≡N键吸收941kJ热量,则下列说法不正确的是( )

A. N4与N2互为同素异形体 B. 1molN4气体转化为N2时要放出724kJ能量
C. N4变成N2是化学变化 D. N4与N2互为同位素
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定条件下进行反应:COCl2(g) ![]() Cl2(g)+CO(g),向2.0 L恒容密闭容器中充入1.0 mol COCl2(g),反应过程中测得的有关数据见下表:
Cl2(g)+CO(g),向2.0 L恒容密闭容器中充入1.0 mol COCl2(g),反应过程中测得的有关数据见下表:
t/s | 0 | 2 | 4 | 6 | 8 |
n(Cl2)/mol | 0 | 0.30 | 0.39 | 0.40 | 0.40 |
下列说法不正确的是( )
A. 生成Cl2的平均反应速率,0~2s比2~4s快B. 0~2s COCl2的平均分解速率为0.15mol·L-1·s-1
C. 6s时,反应达到最大限度D. 该条件下,COCl2的最大转化率为40%
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氮及其化合物在人们的生活经常出现
(1)汽车尾气中NO生成过程的能量变化示意图如下:

该条件下,1mol N2和1molO2完全反应生成NO,会_______________(填“吸收”或“放出”)________kJ能量。
(2)一定温度下,在体积为0.5 L的恒容密闭容器中,氮的气态氧化物X和Y之间反应过程中各物质的物质的量与时间的关系如图所示。
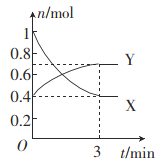
①该反应的化学反应方程式:______________________。
②在0~3 min内,用Y表示的反应速率为____________。
③下列叙述能说明该反应已达到化学平衡状态的是________(填字母)。
a.容器内压强不再发生变化
b.X的体积分数不再发生变化
c.容器内原子总数不再发生变化
d.相同时间内消耗nmolY的同时生成2nmol X
④反应达到平衡后,若降低温度,则υ(正)______,υ(逆)________。(填“增大”“减小”或“不变”)。
(3)反应 A(g)+3B(g)═2C(g)+3D(g)在四种不同情况下的反应速率分别为:
①υ (A)=0.015mol (Ls)﹣1 ②υ (B)=0.09mol (Ls)﹣1
③υ (C)=2.4mol (Lmin )﹣1 ④υ (D)=0.045mol (Ls)﹣1
该反应在四种不同情况下速率由大到小的顺序为(用序号填空)________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对于可逆反应:mA(g)+nB(g) ![]() xC(g) ΔH=?,在不同温度及压强(P1,P2)条件下,反应物A的转化率如下图所示,下列判断正确的是
xC(g) ΔH=?,在不同温度及压强(P1,P2)条件下,反应物A的转化率如下图所示,下列判断正确的是

A. ΔH>0,m+n>x
B. ΔH<0,m+n>x
C. ΔH>0,m+n<x
D. ΔH<0,m+n<x
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】.在一定温度下的恒容容器中,当下列物理量不再发生变化时,不能表明反应: A(s)+3B(g)![]() 2C(g)+D(g)已达平衡状态的是
2C(g)+D(g)已达平衡状态的是
A. 混合气体的压强B. 混合气体的密度
C. 3v逆(C)=2v正(B)D. 气体的平均相对分子质量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定量的乙醇在氧气不足的情况下燃烧,得到CO、CO2和水的总质量为27.6g,若其中水的质量为10.8g,则CO的质量是( )
A. 1.4gB. 2.2gC. 4.4gD. 在2.2g和4.4g之间
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,把 2.5 mol A 和 2.5 mol B混合盛入容积为 2 L的密闭容器里,发生如下反应: 3A(g)+B(g) ![]() x C(g) + 2D(g), 经 5 s反应达平衡,在此 5 s 内 C的平均反应速率为 0.2 mol·L-1·s-1,同时生成1 mol D,下列叙述中不正确的是
x C(g) + 2D(g), 经 5 s反应达平衡,在此 5 s 内 C的平均反应速率为 0.2 mol·L-1·s-1,同时生成1 mol D,下列叙述中不正确的是
A. x=4
B. 达到平衡状态时 A 的物质的量浓度为 c(A)=1.0 mol·L-1
C. 5s 内 B的反应速率 v(B)=0.05 mol·(L·s)-1
D. 达到平衡状态时容器内气体的压强与起始时压强比为 6:5
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com