
常温下,将等体积,等物质的量浓度的NH4HCO3与NaCl溶液混合,析出部分NaHCO3晶体,过滤,所得滤液pH<7。下列说法中正确的是
A.该现象说明了NaHCO3难溶于水
B.滤液中的c(Na+)>c(HCO3-)>c(CO32-)>c(H2CO3)
C.滤液中c(Na+)+c(H+)+c(NH4+)= c(OH-)+ c(HCO3-)+c(CO32-)
D.滤液中c(Cl-)>c(NH4+)> c(HCO3-)> c(H+)>c(OH-)
 口算题卡加应用题集训系列答案
口算题卡加应用题集训系列答案 综合自测系列答案
综合自测系列答案科目:高中化学 来源:2015-2016学年江西省高二下期中化学试卷(解析版) 题型:实验题
某校学生用如图所示装置进行实验,以探究苯与溴发生反应的原理并分离提纯反应的产物,请回答下列问题:

请回答下列问题:
(1)冷凝管所起的作用为冷凝回流和导气,冷凝水从 口进入(填“a”或“b”)。
(2)实验开始时,关闭K2、开启K1和分液漏斗活塞,滴加苯和液溴的混合液,反应开始。III中小试管内苯的作用是 。
(3)能说明苯与液溴发生了取代反应的现象是 。
(4)反应结束后,要让装置Ⅰ中的水倒吸入装置Ⅱ中,这样操作的目的是 ,简述这一操作的方法: 。
(5)将三颈烧瓶内反应后的液体依次进行下列实验操作就可得到较纯净的溴苯。
①用蒸馏水洗涤,振荡,分液;②用5%的NaOH溶液洗涤,振荡,分液;
③用蒸馏水洗涤,振荡,分液;④加入无水CaCl2粉末干燥;⑤ (填操作名称)。
查看答案和解析>>
科目:高中化学 来源:2016届江西省、临川二中高三下联考理综化学试卷(解析版) 题型:填空题
氧元素和卤族元素都能形成多种物质,我们可以利用所学物质结构与性质的相关知识去认识和理解。
(1)溴的价电子排布式为 ;PCl3的空间构型为
(2)已知CsICl2不稳定,受热易分解,倾向于生成晶格能更大的物质,则它按下列 式发生。
A. CsICl2=CsCl+ICl B. CsICl2=CsI+Cl2
(3)根据下表提供的第一电离能数据判断:最有可能生成较稳定的单核阳离子的卤素原子是___________。
氟 | 氯 | 溴 | 碘 | |
第一电离能(kJ•mol﹣1) | 1681 | 1251 | 1140 | 1008 |
(4)下列分子既不存在s﹣pσ键,也不存在p﹣pπ键的是
A. HCl B.HF C. SO2 D. SCl2
(5)已知COCl2为平面形,则COCl2中心碳原子的杂化轨道类型为 ,写出CO的等电子体的微粒 (写出1个)。
(6)钙在氧气中燃烧时得到一种钙的氧化物晶体,其结构如图所示:由此可判断该钙的氧化物的化学式为 .已知该氧化物的密度是ρg•cm﹣3,则晶胞离得最近的两个钙离子间的距离为 cm(只要求列算式,不必计算出数值,阿伏加德罗常数为NA)。

查看答案和解析>>
科目:高中化学 来源:2016届福建省高三下学期周考五理科综合化学试卷(解析版) 题型:选择题
乙醛酸(HOOC-CHO)是有机合成的重要中间体.工业上用“双极室成对电解法”生产乙醛酸,原理如图所示.该装置中阴、阳两极为惰性电极,两极室均可产生乙醛酸,其中乙二醛与M电极的产物反应生成乙醛酸.下列说法不正确的是( )

A.N电极上的电极反应式:HOOC-COOH+2e-+2H+═HOOC-CH0+H2O
C.M电极上的电极反应式为:2Cl--2e-═Cl2↑
B.若有2molH+通过质子交换膜并完全参与反应,则该装置中生成的乙醛酸为1mol
D.乙二醛与M电极的产物反应生成乙醛酸的化学方程式:Cl2+OHC-CHO+H2O═HOOC-CHO+2HCl
查看答案和解析>>
科目:高中化学 来源:2016届安徽省六安市高三下综合训练十理综化学试卷(解析版) 题型:填空题
[化学·选修3:物质结构与性质]请完成下列问题:
(1)某处于激发态的s原子,其中1个3s电子跃迁到3p轨道中,该激发态S原子的核外电子排布式为__________。
(2) Fe的基态原子共有__________种能量不同的电子。
(3)第二周期第一电离能介于B和N之间的元素有__________种。
(4)甲醇(CH3OH)中的羟基被硫羟基取代生成甲硫醇(CH3SH)。甲硫醇分子中S原子杂化轨道类型是__________。
(5) ZnS在荧光体、光导体材料、涂料、颜料等行业中应用广泛。立方ZnS晶体结构如右图所示,其晶胞边长为apm,a位置S2-与b位置Zn2+之间的距离为__________pm(列式表示)。
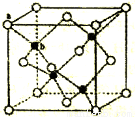
(6)磷酸盐分为直链多磷酸盐、支链状超磷酸盐和环状聚偏磷酸盐三类。某直链多磷酸钠的阴离子呈如下图所示的无限单链状结构,其中磷氧四面体通过共用顶角氧原子相连。则该多磷酸钠的化学式为__________。
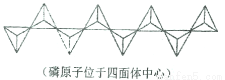
(7)碳化硅的晶胞结构(如下图)与金刚石类似(其中“●”为碳原子,“○”为硅原子),图中“●”点构成的堆积方式与下列图式中__________所表示的堆积方式相同。

(其中C为AB型D为ABC型)
查看答案和解析>>
科目:高中化学 来源:2016届安徽省六安市高三下综合训练十理综化学试卷(解析版) 题型:选择题
设NA为阿伏加罗常数的值,下列说法正确的是( )
A.3.1g由白磷和红磷组成的混合物中含有磷原子的数目为0.1NA
B.0.1mol丙烯醛中含有双键的数目为0.1NA
C.标准状况下,2.24L乙醇中含有的分子数目为0.1NA
D.1molNaHSO4固体中阳离子的数目为2NA
查看答案和解析>>
科目:高中化学 来源:2015-2016学年辽宁鞍山一中高二下期中化学试卷(解析版) 题型:选择题
对三联苯是一种有机合成中间体,工业上合成对三联苯的化学方程式为3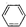
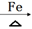
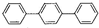 +2H2↑。下列说法不正确的是( )
+2H2↑。下列说法不正确的是( )
A.上述反应属于取代反应
B.对三联苯分子中至少有16个原子共平面
C.对三联苯的一氯取代物有4种
D.0.2 mol对三联苯在足量的氧气中完全燃烧消耗5.1 mol O2
查看答案和解析>>
科目:高中化学 来源:2015-2016学年辽宁鞍山一中高二下期中化学试卷(解析版) 题型:选择题
除去下列物质中的杂质(括号中为杂质),采用的试剂和除杂方法错误的是
选项 | 含杂质的物质 | 试剂 | 除杂方法 |
A | CH4(C2H4) | Br2水 | 洗气 |
B | C6H6(Br2) | Fe粉 | 蒸馏 |
C | C6H5NO2(HNO3) | NaOH溶液 | 分液 |
D | C2H2(H2S) | CuSO4溶液 | 洗气 |
查看答案和解析>>
科目:高中化学 来源:2015-2016学年甘肃会宁一中高一下期中文科化学试卷(解析版) 题型:选择题
元素性质呈周期性变化的决定因素是( )
A.元素原子半径大小呈周期性变化 B.元素原子量依次递增
C.元素原子核外电子排布呈周期性变化 D.元素的最高正化合价呈周期性变化
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com