
配制200ml0.1mol/L稀硫酸溶液时,下列实验操作使得所配溶液浓度偏小的是
A.用量筒量取所需的浓硫酸时仰视读数
B.定容后摇匀,发现液面最低点低于刻度线,再补加几滴蒸馏水至刻度线
C.定容时,俯视刻度线
D.用量筒量取浓硫酸倒入烧杯,再用蒸馏水洗量筒2~3次,洗液倒入烧杯中
科目:高中化学 来源:2014-2015学年河南省南阳市上学期10月月考高二化学试卷(解析版) 题型:选择题
①②③④四种金属片两两相连浸入稀硫酸中都可组成原电池,①②相连时,外电路电流从②流向①;①③相连时,③为正极;②④相连时,②上有气泡逸出;③④相连时,③的质量减少.据此判断这四种金属活动性由强到弱的顺序是( )
A.①③②④ B. ①③④② C. ③④②① D. ③①②④
查看答案和解析>>
科目:高中化学 来源:2014-2015学年河北省高一上学期第二次月考化学试卷(解析版) 题型:选择题
下列各组物质,按化合物、单质、混合物顺序排列的是
A、烧碱、液态氧、碘酒
B、生石灰、白磷、纯碱
C、干冰、铁、氯化氢
D、空气、氦气、胆矾
查看答案和解析>>
科目:高中化学 来源:2014-2015学年河北省高一上学期期中化学试卷(解析版) 题型:选择题
已知 2Fe3+ +2I- =2Fe2+ +I2;2Fe2+ +Cl2 =2Fe3+ +2Cl-,则有关离子的还原性由强到弱的顺序为
A.Cl->Fe2+>I- B.Fe2+>I->Cl-
C.I->Fe2+>Cl- D.Fe2+>Cl->I-
查看答案和解析>>
科目:高中化学 来源:2014-2015学年河北省高一上学期期中化学试卷(解析版) 题型:选择题
下列各组物质,前者属于电解质,后者属于非电解质的是
A.NaCl晶体、BaSO4 B.铜、二氧化硫
C.硫酸、酒精 D.熔融的KNO3、硫酸溶液
查看答案和解析>>
科目:高中化学 来源:2014-2015学年河北省高一上学期期中化学试卷(解析版) 题型:选择题
下列说法正确的是
A.在标准状况下,1mol水的体积是22.4L
B.1molH2所占的体积一定是22.4L
C.在标准状况下,NA个任何分子所占的体积约为22.4L
D.在标准状况下, 28g的N2体积约为22.4L
查看答案和解析>>
科目:高中化学 来源:2014-2015学年河北省高二上学期第三次月考化学试卷(解析版) 题型:填空题
(13分)碳、硫的含量影响钢铁性能。碳、硫含量的一种测定方法是将钢样中的碳、硫转化为气体,再用测碳、测硫装置进行测定。
(1)采用装置A,在高温下将x g钢样中的碳、硫转化为CO2、SO2。
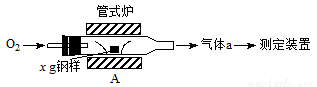
①气体a的成分是______。
②若钢样中硫以FeS形式存在,A中反应:3FeS+5O2 1________+3________。
1________+3________。
(2)将气体a通入测硫装置中(如图),采用滴定法测定硫的含量。
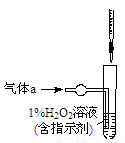
①H2O2氧化SO2的化学方程式:__________________。
②用NaOH溶液滴定生成的H2SO4,消耗z mL NaOH溶液。若消耗1 mL NaOH溶液相当于硫的质量为y g,则该钢样中硫的质量分数:________。
(3)为了减少空气中SO2的排放,常采取的措施有:
①将煤转化为清洁气体燃料。已知:2H2(g)+O2(g)=2H2O(g) ΔH1=-d kJ·mol-1;
2C(s)+O2(g)=2CO(g) ΔH2=-e kJ·mol-1;
碳的燃烧热为f kJ·mol-1(d、e、f均大于0);
写出CO与水蒸气反应生成CO2和H2的热化学方程式:_______________________。
②将含SO2的烟气通过洗涤剂Y,再加入稀硫酸,既可以回收SO2,同时又可以得到化肥,上述洗涤剂Y可以是_______(填序号)。
a.Ca(OH)2 b.CaCl2 c.K2CO3 d.NaHSO3 e.NH3·H2O
查看答案和解析>>
科目:高中化学 来源:2014-2015学年河北省高二上学期第三次月考化学试卷(解析版) 题型:选择题
足量的铁与一定量的稀硫酸充分反应,共收集到标准状况下气体为3.36 L,则参加反应的铁的质量为
A.5.6 g B.8.4 g C.11.2 g D.无法计算
查看答案和解析>>
科目:高中化学 来源:2014-2015学年河北省唐山市高一上学期第一次月考化学试卷(解析版) 题型:填空题
(16分)实验室需要0.1 mol/L NaOH溶液450 mL和0.5 mol/L硫酸溶液450 mL.根据这两种溶液的配制情况回答下列问题:
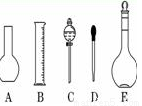
(1)根据计算得知,所需质量分数为98%、密度为1.84 g/cm3的浓硫酸的体积为 ____ mL(计算结果保留一位小数,下同)。
(2)如图所示的仪器中配制溶液肯定不需要的是 (填序号),仪器C的名称是 ,本实验所需玻璃仪器E的名称为
(3)在配制NaOH溶液实验中,其他操作均正确。若定容时仰视刻度线,则所配制溶液浓度 ______0.1 mol/L(填“大于”“等于”或“小于”,下同)。若NaOH溶液未冷却即转移至容量瓶定容,则所配制溶液浓度__ 0.1 mol/L。
(4)下列操作不正确的是 (填序号)。
A.使用容量瓶前检查它是否漏水
B.容量瓶用蒸馏水洗净后,再用待配液润洗
C.将氢氧化钠固体放在天平托盘的滤纸上,准确称量并放入烧杯中溶解后,立即注入容量瓶中
D.将准确量取的18.4 mol·L-1的硫酸,注入已盛有30 mL水的100 mL的容量瓶中,加水至刻度线
E.定容时不小心水加多了少许,立即用胶头滴管吸出即可
F.定容后塞好瓶塞,用食指顶住瓶塞,用另一只手的手指托住瓶底,把容量瓶倒转摇匀
(5)右图为实验室某浓盐酸试剂瓶标签上的有关数据,试根据标签 上的有关数据回答下列问题:

①将________升氯化氢(标准状况)通入1.00L水中可得到36.5﹪的浓盐酸,该浓盐酸中HCl的物质的量浓度为
②取用任意体积的该盐酸溶液时,下列物理量中不随所取体积的多少而变化的是 。
A.溶液中HCl的物质的量 B.溶液的浓度
C.溶液中Cl-的数目 D.溶液的密度
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com