
【题目】下表为元素周期表的一部分,请参照元素①-⑧在表中的位置,用化学用语回答下列问题:
族 周期 | IA | 0 | ||||||
1 | ① | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |
2 | ② | ③ | ④ | |||||
3 | ⑤ | ⑥ | ⑦ | ⑧ | ||||
(1)④、⑤、⑥的原子半径由大到小的顺序为_________________________。
(2)②、③、⑦的最高价含氧酸的酸性由强到弱的顺序是_________________________。
(3)①、④、⑤、⑧中的某些元素可形成既含离子键又含极性共价键的化合物,写出其中一种化合物的电子式:____________________。
(4)由表中两种元素的原子按1:1组成的常见液态化合物的溶液易被催化分解,写出其化学方程式_________________。
(5)由表中元素形成的常见物质X、Y、Z、M、N可发生以下反应:

X溶液与Y溶液反应的离子方程式为_______________________________,
N→⑥的单质的化学方程式为______________________________________。
【答案】 Na>Al>O HNO3>H2CO3>H2SiO3 ![]() 或
或![]() 2H2O2====2H2O+O2↑ Al3++3NH3H2O═Al(OH)3↓+3NH4+ 2Al2O3(熔融)
2H2O2====2H2O+O2↑ Al3++3NH3H2O═Al(OH)3↓+3NH4+ 2Al2O3(熔融)![]() 4Al+3O2↑
4Al+3O2↑
【解析】本题分析:本题主要考查元素的性质。①②③④⑤⑥⑦⑧分别是H、C、N、O、Na、Al、Si、Cl。
(1)同周期元素的原子半径随着原子序数的增大而减小,所以原子半径Na>Al>Si。同主族元素原子半径随着电子层数增大而增大,所以原子半径O<Si。总之,④、⑤、⑥的原子半径由大到小的顺序为Na>Al>O。
(2)非金属性N>C>Si,所以最高价含氧酸的酸性由强到弱的顺序是HNO3>H2CO3>H2SiO3。
(3)①、④、⑤、⑧中的某些元素可形成既含离子键又含极性共价键的化合物氢氧化钠和次氯酸钠,其中一种化合物的电子式:![]() 。
。
(4)由表中两种元素的原子按1:1组成的常见液态化合物的溶液易被催化分解,其化学方程式为2H2O2![]() 2H2O+O2↑ 。
2H2O+O2↑ 。
(5)X溶液与Y溶液反应的离子方程式为![]() 。
。
N→⑥的单质的化学方程式为![]() 。
。


科目:高中化学 来源: 题型:
【题目】现有A、B、C、D四种第一、二周期元素,A分别与B、C、D结合生成甲、乙、丙三种化合物,且甲、乙、丙3分子中含相同数目的质子数,C、D结合生成化合物丁。有关元素的单质和甲、乙、丙、丁四种化合物的转化关系如下图:

(1)写出B+乙→甲+C的化学反应方程式__________________。
(2)根据以上条件可以确定A、B、C、D四种元素中的三种,分别是_______、_______、_______(元素符号)
(3)依据下列条件可以进一步确定上述第四种元素:
①甲与丙以及乙与丙均能够发生反应,②甲、丙、丁都是无色有刺激性气味的物质。据此,请回答下列问题:
A.写出上述第四种元素在周期表中的位置______________。
B.写出C+丙→乙+丁的化学反应方程式___________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】草酸钴用途广泛,可用于指示剂和催化剂制备。一种利用水钴矿[主要成分为Co2O3,含少量Fe2O3、Al2O3、MnO、MgO、CaO等]制取CoC2O4·2H2O工艺流程如下:

已知:①浸出液含有的阳离子主要有H+、Co2+、Fe2+、Mn2+、Ca2+、Mg2+、Al3+等;
②部分阳离子以氢氧化物形式沉淀时溶液的pH见下表:
沉淀物 | Fe(OH)3 | Fe(OH)2 | Co(OH)2 | Al(OH)3 | Mn(OH)2 |
完全沉淀的pH | 3.7 | 9.6 | 9.2 | 5.2 | 9.8 |
(1)浸出过程中加入Na2SO3的目的是将_____________还原(填离子符号)以便固体溶解。该步反应的离子方程式为 (写一个)。
(2)NaClO3的作用是将浸出液中的Fe2+氧化成Fe3+,氯元素被还原为最低价。该反应的离子方程式为 。
(3)利用平衡移动原理分析:加Na2CO3能使浸出液中Fe3+、Al3+转化成氢氧化物沉淀的原因是 。
(4)萃取剂对金属离子的萃取率与pH的关系如图所示。滤液Ⅱ中加入萃取剂的作用是 ;使用萃取剂适宜的pH=____(填序号)左右:

A.2.0 B.3.0 C. 4.0
(5)滤液Ⅰ“除钙、镁”是将溶液中Ca2+与Mg2+转化为MgF2、CaF2沉淀。已知Ksp(MgF2)=7.35×10-11、Ksp(CaF2)=1.05×10-10。当加入过量NaF后,所得滤液c(Mg2+)/c(Ca2+)= 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以淀粉为主要原料合成一种具有果香味有机物C和高分子化合物E的合成路线如下图所示。
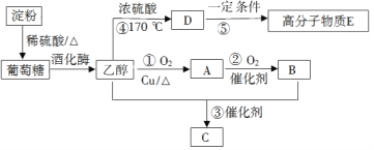
请回答下列问题:
(1)写出C的结构简式:__________________,A分子内含有的官能团是_______(填名称)。
(2)写出下列反应的反应类型:①________________,③________________。
(3)写出下列反应的化学方程式:①________________________;⑤________________________。
(4)某同学欲用下图装置制备物质C,将试管B中的物质C分离出来,用到的主要玻璃仪器有:烧杯、________,插入试管B的导管接有一个球状物,其作用为________________________。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上利用无机矿物资源生产部分材料的流程示意图如下。下列说法不正确的是
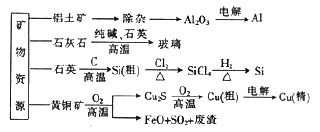
A. 在铝土矿制备较高纯度A1的过程中常用到NaOH溶液、CO2气体、冰晶石
B. 石灰石、纯碱、石英、玻璃都属于盐,都能与盐酸反应
C. 在制粗硅时,氧化剂与还原剂的物质的量之比为1∶2
D. 黄铜矿(CuFeS2)与O2反应产生的Cu2S、FeO均是还原产物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】丁苯酞是我国自主研发的一类用于治疗急性缺血性脑卒的新药。合成丁苯酞(J)的一种路线如下:


(1)A的名称是_______________,A分子中最多有_____个原子共平面。
(2)B生成A的化学方程式______________________。
(3)D生成E的反应类型为_________,试剂a是_________。
(4)F的结构简式_____________________。
(5)J是一种酯,分子中除苯环外还含有一个五元环。写出H生成J的化学方程式_____(注明反应条件)。
(6)![]() ,X的同分异构体中:①能发生银镜反应;②能与氯化铁溶液发生显色反应。满足上述条件的X的同分异构体共有______种,写出其中核磁共振氢谱有五组吸收峰的结构简式___________________。
,X的同分异构体中:①能发生银镜反应;②能与氯化铁溶液发生显色反应。满足上述条件的X的同分异构体共有______种,写出其中核磁共振氢谱有五组吸收峰的结构简式___________________。
(7)利用题中信息和所学知识,写出以甲烷和化合物D为原料,合成 ![]() 的路线流程图____________________(其它试剂自选)。
的路线流程图____________________(其它试剂自选)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列事实不能说明非金属性C1>I的是
A. C12+2I-=2C1-+I2 B. 稳定性:HC1>HI
C. 酸性:HC1O4>HIO4 D. 酸性:HC1O3>HIO3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】气态烃X在标准状态下的密度为1.16gL-1,D能发生银镜反应,E为聚氯乙烯,有关物质的转化关系如下:请回答下列问题:

(1)反应②的反应类型为_____________,一定条件下X能发生类似于⑤的反应,
所得高分子化合物的结构简式为_________________。
(2)A与F在催化剂作用下直接生成G的化学方程式为___________________________。
(3)下列说法正确的是_________。
A.A、B、E均能使酸性高锰酸钾溶液褪色
B.G的同分异构体中能与碳酸氢钠反应生成CO2气体的物质有4种
C.F、G都能与NaOH溶液反应,且都生成钠盐
D.X先后与F、H2反应也可以制得G
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com