
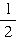 O2(g)=H2O(g) ΔH(298K)=akJ?mol-1
O2(g)=H2O(g) ΔH(298K)=akJ?mol-1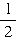 O2(g)=H2O(l) ΔH(298K)=bkJ?mol-1
O2(g)=H2O(l) ΔH(298K)=bkJ?mol-1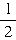 mol气态O2反应,生成1mol水蒸气,放出241.8kJ的热量;同样是1mol气态H2与
mol气态O2反应,生成1mol水蒸气,放出241.8kJ的热量;同样是1mol气态H2与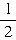 mol气态O2反应,生成1mol液态水则放出285.8kJ的热量。显然,该题中的a不等于b,故C项错误;热化学方程式的ΔH与化学方程式中各物质的化学式的系数是相对应的。当热化学方程式中各物质的化学式的系数同时扩大或缩小若干倍时,相应的ΔH也扩大或缩小同样的倍数。因此,c=2b。
mol气态O2反应,生成1mol液态水则放出285.8kJ的热量。显然,该题中的a不等于b,故C项错误;热化学方程式的ΔH与化学方程式中各物质的化学式的系数是相对应的。当热化学方程式中各物质的化学式的系数同时扩大或缩小若干倍时,相应的ΔH也扩大或缩小同样的倍数。因此,c=2b。 

科目:高中化学 来源: 题型:013
今有如下3个热化学方程式:
①![]() D△H=a kJ·
D△H=a kJ·![]() ;
;
②![]() D△H=b kJ·
D△H=b kJ·![]() ;
;
③![]() D△H=c kJ·
D△H=c kJ·![]() .
.
关于它们的表述正确的是( )
A.它们都是吸热反应
B.a、b和c均为正值
C.a=b
D.2b=c
查看答案和解析>>
科目:高中化学 来源:物理教研室 题型:013
①![]() D△H=a kJ·
D△H=a kJ·![]() ;
;
②![]() D△H=b kJ·
D△H=b kJ·![]() ;
;
③![]() D△H=c kJ·
D△H=c kJ·![]() .
.
关于它们的表述正确的是( )
A.它们都是吸热反应
B.a、b和c均为正值
C.a=b
D.2b=c
查看答案和解析>>
科目:高中化学 来源: 题型:013
今有如下3个热化学方程式:
H2(g)+1/2O2(g)══H2O(g),DH=a(kJ/mol);H2(g)+1/2O2(g)══H2O(l),DH=b(kJ/mol);
2H2(g)+O2(g)══2H2O(l),DH=c(kJ/mol)。
关于它们的叙述中正确的是( )
A.它们都是吸热反应 B.a,b,c均为正值
C.a=b D.2b=c
查看答案和解析>>
科目:高中化学 来源: 题型:
H2(g)+![]() O2(g)=H2O(g) ΔH=a kJ·mol-1
O2(g)=H2O(g) ΔH=a kJ·mol-1
H2(g)+![]() O2(g)=H2O(l) ΔH=b kJ·mol-1
O2(g)=H2O(l) ΔH=b kJ·mol-1
2H2(g)+O2(g)=2H2O(l) ΔH=c kJ·mol-1
关于它们的下列表述正确的是( )
A.它们都是吸热反应
B.a、b和c均为正值
C.a=b
D.2b=c
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com