
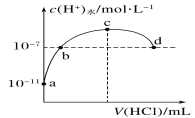
【题目】常温下,向20 mL 0.1 mol·L-1氨水中滴加0.1 mol·L-1盐酸,溶液中由水电离出的c(H+)随加入盐酸体积的变化如图所示。则下列说法正确的是( )
A.c点溶液中,c(NH![]() )=c(Cl-)
)=c(Cl-)
B.a、b之间的任意一点:c(Cl-)>c(NH![]() )>c(H+)>c(OH-)
)>c(H+)>c(OH-)
C.b、d两点溶液pH均为7
D.b、c、d任意一点都有: c(NH![]() )+c(H+)=c(OH-)+ c(Cl-)
)+c(H+)=c(OH-)+ c(Cl-)
【答案】D
【解析】
向20 mL 0.1 mol·L-1氨水中滴加0.1 mol·L-1盐酸,根据图象可知,水的电离程度由小逐渐变大,后又逐渐变小,则a点溶液中溶质只有氨水,b点溶质为一水合氨和氯化铵,c点NH4+的水解程度达到最大,也是恰好完全反应点,溶质为氯化铵;再继续加入盐酸,盐酸过量抑制水的电离,溶质为氯化铵和盐酸。
A.根据分析,c点为氨水与盐酸完全反应点,溶液中溶质为氯化铵,铵根离子会水解,所以c(NH4+)<c(Cl),故A错误;
B.a到b过程中,水电离程度不断增大,氨水不断被中和生成氯化铵,b点溶质应为氯化铵与氨水混合溶液,溶液中存在电荷守恒:c(Cl-)+ c(OH-)=c(H+)+ c(NH4+),溶液从碱性到中性,则a-b之间任意一点有c(H+)<c(OH-),结合电荷守恒得c(Cl)<c(NH4+),故B错误;
C.b点溶质为氯化铵与氨水,溶液呈中性,d点溶质为氯化铵与过量的盐酸,溶液显酸性,故C错误;
D.根据分析,b点溶质为一水合氨和氯化铵,c点NH4+的水解程度达到最大,也是恰好完全反应点,溶质为氯化铵;d点溶质为氯化铵和盐酸,b、c、d任意一点对应的溶液中都存在电荷守恒,电荷守恒式都为c(NH![]() )+c(H+)=c(OH-)+ c(Cl-),故D正确;
)+c(H+)=c(OH-)+ c(Cl-),故D正确;
答案选D。


科目:高中化学 来源: 题型:
【题目】铜板上铁铆钉处的吸氧腐蚀原理如图所示,下列有关说法中,不正确的是

A. 正极电极反应式为:2H++2e—→H2↑
B. 此过程中还涉及到反应:4Fe(OH)2+2H2O+O2=4Fe(OH)3
C. 此过程中铜并不被腐蚀
D. 此过程中电子从Fe移向Cu
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】汽车剧烈碰撞时,安全气囊中发生反应![]() 。若有2 mol N2生成,则下列判断正确的是( )
。若有2 mol N2生成,则下列判断正确的是( )
A.N2的体积为44. 8 L
B.有 0. 125 mol KNO3被氧化
C.N2既是氧化产物又是还原产物
D.转移电子的物质的量为10 mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2019年10月1日是中华人民共和国成立70周年,国庆期间对大量盆栽鲜花施用了S-诱抗素制剂以保证鲜花盛开,S-诱抗素的分子结构简式如图。下列关于该物质的说法正确的是
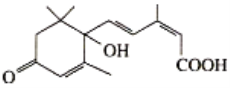
A.该有机物的分子式为C15H20O4
B.该有机物能发生取代、加成和水解反应
C.1mol的该有机物与足量的钠反应产生2molH2
D.1mol该有机物含有4mol双键
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于下图所示的原电池,下列说法正确的是( )
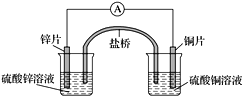
A. 电子从锌电极通过电流表流向铜电极
B. 盐桥中的阴离子向硫酸铜溶液中迁移
C. 铜电极发生还原反应,其电极反应是2H++2e-===H2↑
D. 取出盐桥后,电流表仍会偏转,铜电极在反应前后质量不变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学小组为了研究外界条件对化学反应速率的影响,进行了酸性高锰酸钾与草酸的反应,记录以下实验数据(已知![]() 为阿伏伽德罗常数的值):
为阿伏伽德罗常数的值):
试管中所加试剂及其用量/mL | 溶液退至无色所需时间/min | |||||
实验编号 | 实验温度/℃ | 0.6 mol/LH2C2O4溶液 | H2O | 3 mol/LH2SO4溶液 | 0.05 mol/LKMnO4溶液 | |
① | 25 | 3.0 | v1 | 2.0 | 3.0 | 1.5 |
② | 25 | 2.0 | 3.0 | 2.0 | 3.0 | 2.7 |
③ | 50 | 2.0 | v2 | 2.0 | 3.0 | 1.0 |
(1)请写出该反应的离子方程式:___,当该反应以实验①中数据反应完全时转移电子数为_____![]() 。
。
(2)实验①②是探究浓度对反应速率的影响,实验②③时探究温度对反应速率的影响,则表中V1=_______,V2=__________。
(3)根据实验①、②的数据,可以得到的结论是____。
(4)该小组同学根据经验绘制了n(Mn2+)随时间变化的趋势如图1所示,但有同学查阅已有的实验资料发现,该实验过程中n(Mn2+)随时间变化的实际趋势如图2所示。

该小组同学根据上述信息提出了新的假设,并设计一下实验方案继续进行实验探究。
实验编号 | 实验温度/℃ | 试管中所加试剂及其用量/ml | 再加入某种固体 | 溶液退至无色所需时间/min | |||
0.6 mol/LH2C2O4溶液 | H2O | 3 mol/LH2SO4溶液 | 0.05 mol/L KMnO4 溶液 | ||||
④ | 25 | 3.0 | 2.0 | 2.0 | 3.0 | MnSO4 | t |
①该小组同学提出的新假设是__________。
②若该小组同学提出的假设成立,应观察到__________(填实验现象)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】a~n10中元素在周期表中的位置如图所示,请回答下列问题:
a | ||||||||
b | c | d | e | |||||
f | g | h | m | n | ||||
…… |
(1)m的阴离子的结构示意图为___。
(2)b的最高价氧化物的化学式为___;用化学方程式表示f、d的单质形成f2d2的过程___。
(3)d、g、n形成的简单离子的半径由大到小的顺序为___(用离子符号表示)。
(4)以上元素组成的物质有下列框图中的转化关系,其中甲为10电子微粒。
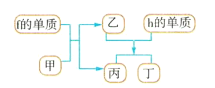
请写出h的单质与乙反应的化学方程式:___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列图示内容的对应说明正确的是
编号 | A | B | C | D |
图示 |
食盐水 |
片刻后在Fe 电极附近滴入K3[Fe(CN)6]溶液 |
|
|
说明 | 验证铁钉发生 吸氧腐蚀 | 验证 Fe 电极被保护 | 该装置是牺牲阳极的阴极保护法 | 该化学反应为放热反应 |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关 2 个电化学装置的叙述不正确的是
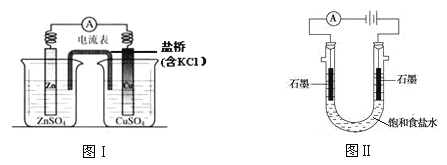
A.图Ⅰ,在不改变总反应的前提下,可用 Na2SO4 替换 ZnSO4,用石墨替换 Cu 棒
B.图Ⅰ,电流形成的完整过程是:负极 Zn-2e-=Zn2+,电子经导线流向正极,正极 Cu2++2e-=Cu
C.图Ⅱ,通电后向两极滴加酚酞,左侧变红
D.图Ⅰ,盐桥中 Cl-向左侧移动,图Ⅱ,溶液中 Cl-向右侧移动
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com