
| 滴定次数 | 待测液体积/mL | 标准盐酸体积/mL | |
| 滴定前读数 | 滴定后读数 | ||
| 第1次 | 20.00 | 4.10 | 29.10 |
| 第2次 | 20.00 | 0.00 | 24.90 |
| 第3次 | 20.00 | 4.00 | 29.10 |
分析 (1)锥形瓶不能润洗,用待测液润洗锥形瓶,导致消耗的标准液体积偏高,依据c(待测)=$\frac{V(标准)×c(标准)}{V(待测)}$进行误差分析;
(2)为保证实验准确,标准液浓度需要准确;
(3)酚酞遇到碱显红色,用盐酸滴定滴有酚酞的氢氧化钠溶液,达到滴定终点的标志为溶液颜色由红色突变为为无色,且半分钟不恢复颜色;
(4)酸碱中和反应H++OH-=H2O,分析表格中数据,计算消耗标准液的体积,依据c(待测)=$\frac{V(标准)×c(标准)}{V(待测)}$计算.
解答 解:(1)锥形瓶不能润洗,用待测液润洗锥形瓶,导致消耗的标准液体积偏高,依据c(待测)=$\frac{V(标准)×c(标准)}{V(待测)}$可知溶液浓度偏高;
故答案为:偏高;
(2)为保证实验准确,标准液浓度需要准确,用蒸馏水洗涤后的滴定管,如果不用标准液润洗直接用来盛放标准液,将导致标准液被稀释,所测得溶液浓度不准确,所以步骤②中酸式滴定管用标准酸液润洗2~3次,目的确保标准盐酸溶液的浓度不发生变化;
故答案为:确保标准盐酸溶液的浓度不发生变化;
(3)酚酞遇到碱显红色,用盐酸滴定滴有酚酞的氢氧化钠溶液,达到终点的标志为:溶液颜色突变为红色变为无色,且半分钟内颜色不发生变化;
故答案为:锥形瓶内溶液由红色变为无色,且半分钟内颜色不再改变;
(4)第一次实验消耗标准液的体积为:29.10-4.10=25.00mL;
第二次实验消耗标准液的体积为:24.90mL;
第三次实验消耗标准液的体积为:29.10-4.00=25.10mL;
所以三次消耗标准液体积为:$\frac{25.00+24.90+25.10}{3}$=25.00mL,
则烧碱溶液的浓度为:$\frac{0.1000mol•{L}^{-1}×25.00mL}{20.00mL}$=0.1250 mol•L-1;
故答案为:0.1250 mol•L-1.
点评 本题考查了酸碱中和滴定实验,明确中和滴定的原理,熟悉操作步骤及滴定管使用方法和注意事项,注意误差分析的方法和技巧,题目难度中等.


科目:高中化学 来源: 题型:选择题
| A. | 同温同压下,相同体积的物质,它们的物质的量必相等 | |
| B. | 1 L一氧化碳气体一定比1 L氧气的质量小 | |
| C. | 28 g N2和CO的混合气体在标准状况下的体积约为22.4 L | |
| D. | 常温常压下,1 mol碳完全燃烧消耗22.4 L氧气 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
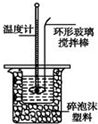 某实验小组用0.50mol/L NaOH溶液和0.50mol/L硫酸溶液进行中和热的测定.
某实验小组用0.50mol/L NaOH溶液和0.50mol/L硫酸溶液进行中和热的测定.| 温度 实验次数 | 起始温度t1/℃ | 终止温度 t2/℃ | 温度差平均值 (t2-t1)/℃ | ||
| H2SO4 | NaOH | 平均值 | |||
| 1 | 26.2 | 26.0 | 26.1 | 30.1 | |
| 2 | 27.0 | 27.4 | 27.2 | 33.3 | |
| 3 | 25.9 | 25.9 | 25.9 | 29.8 | |
| 4 | 26.4 | 26.2 | 26.3 | 30.4 | |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 容器编号 | 起始时各物质物质的量/mol | 达到平衡的时间/min | 达平衡时体系能量的变化/kJ | ||||
| CO | H2O | CO2 | H2 | ||||
| ① | 1 | 4 | 0 | 0 | t1 | 放出热量:32.8kJ | |
| ② | 2 | 8 | 0 | 0 | t2 | 放出热量:Q | |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com